Wie sind modRNA-LNP Produkte als Klasse auf ihre Sauberkeit und Reinheit hin zu überprüfen?
Man sollte doch vermuten, dass man das wüsste, wo doch diese Produkte seit 2021 auf dem Markt sind.
Dem ist aktuell nicht so, aber es gibt mittlerweile immerhin Entwürfe, wie man so etwas machen sollte, über die man diskutiert.
Das muss man aber verstanden haben, um die Probleme, die sich daraus für die Verträge mit dem “Impfstoff-”Herstellern ergeben, bezüglich GMP und dergleichen, zu verstehen.
Galten diese Regeln schon 2020, weil man sie als guten Menschenverstand deklarieren kann, oder gelten sie erst ab dem Zeitpunkt, wo die Guideline in Kraft tritt?
EMA Draft Guideline
Anscheinend hat man im Februar 2025 einen Leitfaden für die Qualitätsmerkmale entworfen und bis 30. September 2025 wurde darüber beraten, bzw. konnte man Vorschläge einbringen. Wer mitgemacht hat, kann man noch nicht einsehen, bisher ist noch nichts veröffentlicht: EUSurvey – Survey unavailable
Problem Nr. 1
Nur die modRNA selbst, die man als mRNA bezeichnet, was chemisch schon mal direkt falsch ist, wird als aktive Substanz in Betracht gezogen. Die Lipide, deren Verunreinigungen oder biologische Aktivität, wird in dieser Guideline NICHT bedacht. Man kann also hochtoxische Lipide verwenden, das ist vollkommen ok, weil diese nicht als aktive Substanz betrachtet werden?
Ganz so ist es nicht. Für die Lipide scheint es eine eigene Guideline zu geben, die ich noch nicht gefunden habe.
Dennoch ist es ein Problem, dass die Lipide als inert angesehen werden.
Problem Nr. 2
Man muss nur die detaillierten Informationen der mRNA-Sequenz (eigentlich modRNA) angeben, nicht die Sequenz des verwendeten Plasmids, welches als Verunreinigung enthalten sein könnte.
Problem Nr. 3
Die linearisierte DNA (nicht das Ausgangsplasmid) muss wie folgt chrakterisiert werden:
Die lineare DNA-Platte muss charakterisiert werden, und die Freigabeprüfung sollte Parameter wie Aussehen, pH-Wert, DNA-Konzentration, Identität und Sequenz, Integrität der kodierenden Region des Poly(A)-Schwanzes (falls zutreffend), prozentualen Anteil an linearisiertem Plasmid (falls zutreffend), Restgehalte an genomischer DNA und RNA (falls zutreffend), Restproteine, Keimbelastung und Endotoxine umfassen.
Leider fehlt hier die Charakterisierung der verwendeten Promotoren. SV40 Promotoren gehören da NICHT rein. Sie sind aber nicht explizit untersagt.
Problem Nr. 4
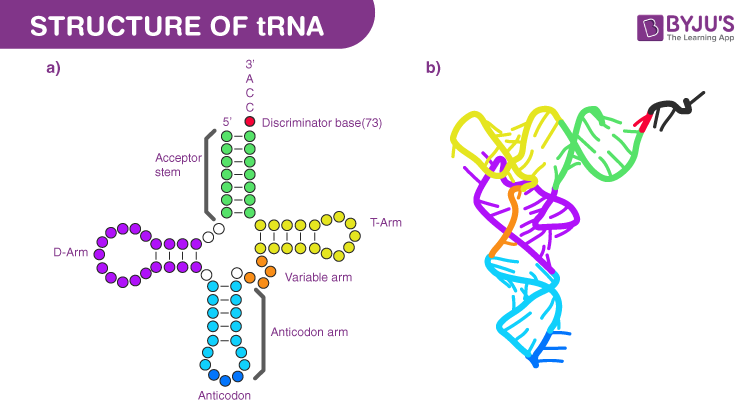
Um den Aufbau von RNA zu verstehen, hilft das Bild einer Halskette:
Primärstruktur: Die Perlenkette
Das ist die einfachste Ebene. Es ist lediglich die Abfolge (Sequenz) der vier Bausteine: Adenin, Guanin, Cytosin und Uracil. Vier verschiedene, bunte Perlen, die nacheinander aufgefädelt werden.
Sekundärstruktur: Die Schlaufen
RNA bleibt selten ein langer, gerader Faden. Da sie meist einzelsträngig ist, klappt sie um und geht mit sich selbst „Paarungen“ ein (A mit U, C mit G). Die Kette bildet lokale Muster wie kleine Schleifen, Haarnadelkurven (Hairpins) oder Blasen.
Tertiärstruktur: Das Knäuel (Der wichtigste Teil)
Das ist die dreidimensionale Gestalt im Raum. Die Sekundärstrukturen (Schleifen) falten sich noch einmal ineinander, verdrehen sich und bilden eine kompakte, feste Form. Die Kette mit ihren Schleifen wird zu einem komplexen 3D-Objekt zusammengeknüllt – wie ein Schlüssel, der nur in ein bestimmtes Schloss passt. Erst durch diese Form kann RNA wie ein Werkzeug (Enzym) arbeiten. Ohne die richtige Tertiärstruktur könnte ein Ribosom keine Proteine bauen und ein Virus könnte keine Zellen infizieren.
Der Unterschied zwischen sekundär a) und tertiär b) Struktur:
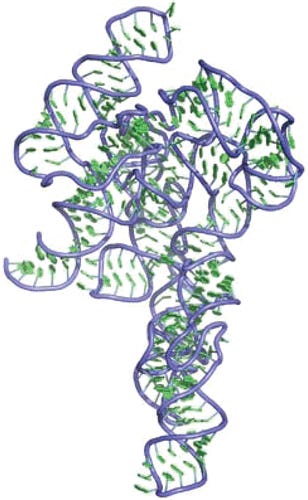
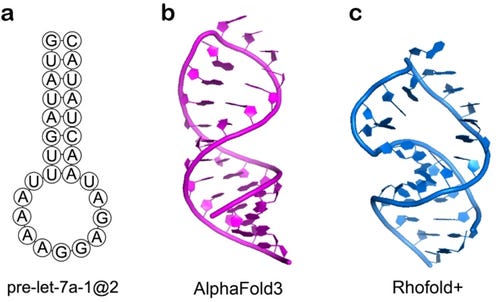
So sieht RNA wahrscheinlichin 3D aus:
Vorhersagen mit Programmen mit Aphafold sind nur bedingt möglich, Kristallstrukturen gibt es nur sehr wenige.
Wie nahe die Vorhersage der Realität kommt, weiß keiner.
Das einzig wahre (für mich, weil ich extrem konservativ in dieser Hinsicht bin), sind Röntgenkristallstrukturen.
Kristallstrukturanalyse eines 26-mer-RNA-Moleküls, das ein neues RNA-Motiv darstellt: den Hook-Turn:
NEU = Kann man nicht simulieren/vorhersagen, weil man die Existenz vor einer Kristallstruktur natürlich nicht kennen kann.
Die Integrität der Primärstruktur soll bestätigt werden.
Die Sekundärstruktur soll mir CD Spektroskopie bestimmt werden.
ABER
Was ist mit der Tertiärstruktur, dem wichtigsten Teil?
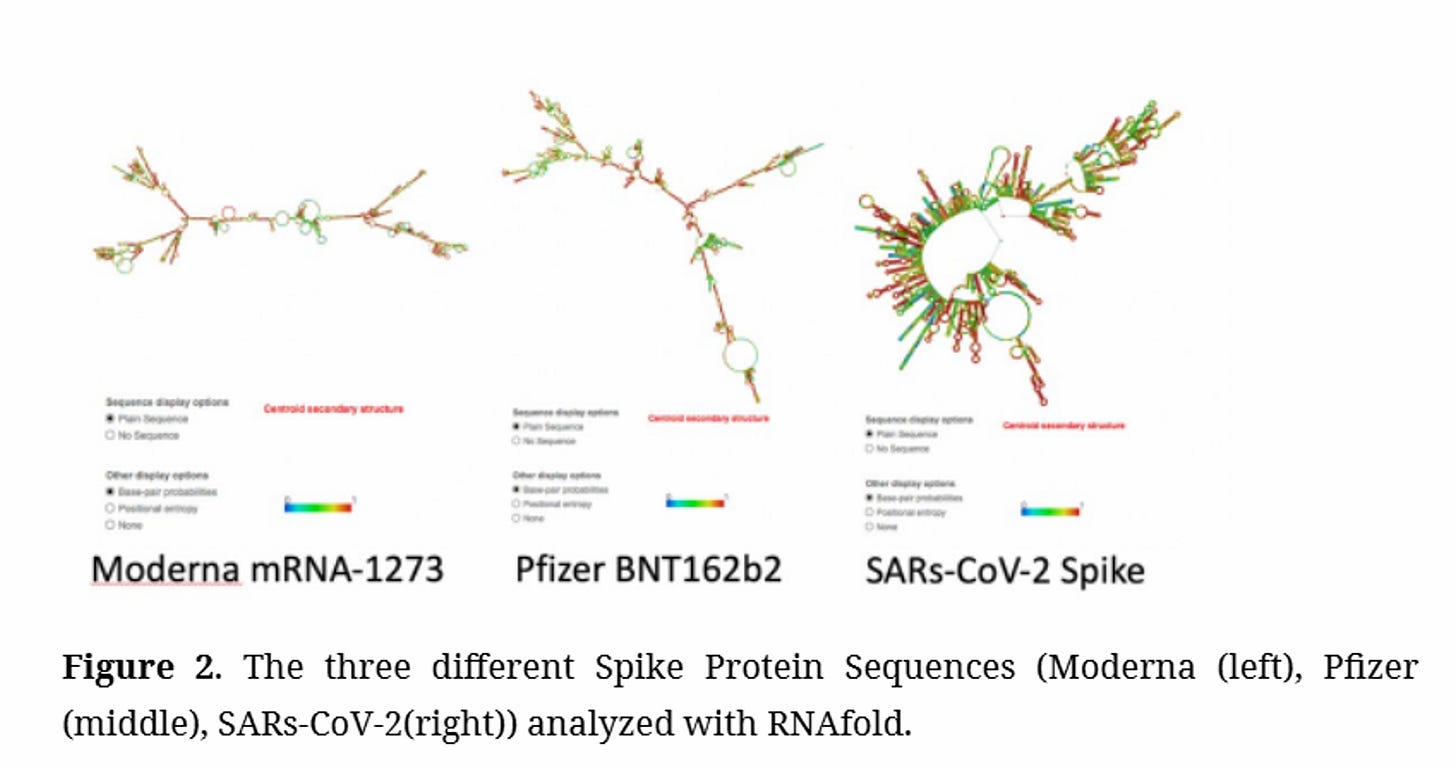
Überhaupt, schon die Sekundärstruktur der modRNA hatte praktisch nichts mehr mit dem Original zu tun beim Spike-Protein.
Was nun? Was, wenn die Struktur des modRNA Konstrukts dermaßen vom Original abweicht. Ist das erlaubt oder nicht?
Problem Nr. 5
Die Fähigkeit der mRNA, in das richtige Protein übersetzt zu werden, sollte mithilfe geeigneter Assays wie zellfreier Translationssysteme oder durch In-vitro-Translation nach Transfektion geeigneter Zelllinien untersucht werden. Die korrekte Größe und Identität des translatierten Proteins sollte bestätigt werden, beispielsweise durch Western-Blot-Analyse.
Nun sind wir bei einem SEHR komplexen Thema, das ich noch gar nicht komplett veröffentlicht habe. Wir müssen an dieser Stelle also oberflächlich bleiben.
Nicht jedes Codon hat überhaupt eine tRNA. Es gibt Codons, die haben gar keine eigene tRNA und werden von anderen tRNAs mit bedient. Das variiert auch noch von Organismus zu Organismus und von möglicherweise innerhalb des Organismus von Organ zu Organ, wie bei der Seidenraupe.
Rot markiert die Codons, die keine eigene tRNA haben und nur über sogenannte wobbel tRNA (also an einer Stelle rumwackelnde tRNA bedient) werden, andere Codons von tRNAs wo sowohl als auch zutrifft. Was passiert wohl, wenn da ein N1-Methylpseudouridin verbaut ist?!
Was wäre also ein geeignetes Testsystem? Welche Zellkultur? Und was passiert, wenn die Ergebnisse von Zelltyp zu Zelltyp variieren.
Die korrekte Größe und Identität des translatierten Proteins sollte bestätigt werden, beispielsweise durch Western-Blot-Analyse.
ABER, wenn durch andere Dekodierung Protein entstehen, die so anders sind, dass sie von den Antikörpern des Western-Blots gar nicht identifiziert werden? Was macht man in so einem Fall?
Problem Nr. 6
Die benannten Verunreinigungen, die getestet werden müssen, zeigen, dass die EMA sehr wohl weiß, dass diese in den Corona modRNA-Produkten ein Problem waren.
Was fehlt ist, dass man die Fragmente testet, ob sie als Oncomir funktionieren könnten.
Ein OncomiR (oder Oncomir) ist eine spezielle Art von MicroRNA (miRNA), die mit der Entstehung und dem Fortschreiten von Krebs in Verbindung steht. Der Begriff ist ein Kofferwort aus „Onkogen“ (ein krebsförderndes Gen) und „MicroRNA“.
Man müsste als bioinformatisch vorher durchrechnen, ob entsprechende Oncomirs entstehen könnten und die entsprechenden Sequenzen abändern, damit das nicht passieren kann. Das geht natürlich nur bei bekannten Oncomir Sequenzen.
DNA:RNA Hybride fehlen auch in der Analyse. Die darf es auch nicht geben.
Zu den prozessbedingten Verunreinigungen zählen restliche DNA-Matrizen und Wirtszell-DNA, Proteinrückstände (z. B. Enzyme, aus Wirtszellen stammend), alle Chemikalien, die im Prozess zur Reinigung oder Stabilisierung verwendet werden könnten, sowie nicht eingebaute Nukleotide. Die Charakterisierung sollte unter Verwendung geeigneter und ausreichend empfindlicher Methoden erfolgen. Das von diesen potenziellen Verunreinigungen ausgehende Risiko sollte gründlich bewertet werden. Zur Quantifizierung und Charakterisierung von Rest-DNA sollten orthogonale Testmethoden verwendet werden. Es wird erwartet, dass eine Analyse der Fragmentgröße der Rest-DNA durchgeführt wird, um die Wirksamkeit der enzymatischen Reaktion und des Reinigungsprozesses nachzuweisen. Während allgemein erwartet wird, dass der Wirkstoff bei der Freigabe routinemäßig auf Restproteine und Rest-DNA-Matrizen getestet wird, kann es akzeptabel sein, Routinetests auf andere prozessbedingte Verunreinigungen wegzulassen, sofern Charakterisierungsstudien und Prozessvalidierungen deren konsistente Entfernung auf akzeptabel niedrige Werte nachweisen. Charakterisierungsstudien sollten auch die Prüfung auf allgemeine sicherheitsrelevante Parameter wie bakterielle Endotoxine und Keimbelastung umfassen.
Gelten diese Regeln auch schon für die Produkte, die auf dem Markt sind? Was genau sind die geeigneten und ausreichend empfindlichen Methoden? Was genau ist eine gründliche Bewertung der Risiken? Reicht es, wenn man sich, wie bei Pfizer, einfach einig ist, dass sie kein Problem darstellen, obwohl die wissenschaftliche Literatur das Gegenteil belegt.
Was Endotoxine angeht, so sind die Messwerte bisher in ALLEN mir bekannten Dokumenten geschwärzt.
Man gibt bei der EMA tatsächlich Messmethoden vor:
Bei den Produktionsrückständen steht aber: “Eine auf einer Risikobewertung basierende Kontrollstrategie”
Wenn Pfizer oder wer auch immer beschließt, dass man sich einig ist, dass es kein Risiko ist, muss man dann eine Kontrollstrategie haben?
Problem Nr. 7
Die Studien zur Formulierungsentwicklung sollten so ausführlich beschrieben werden, dass die Auswahl geeigneter Lipide und anderer Hilfsstoffe für eine robuste LNP-Formulierung des fertigen mRNA-Impfstoffs begründet wird. Das lipidbasierte Nano-Transportsystem des mRNA-Impfstoffs (d. h. LNP) muss ausreichend charakterisiert werden.
Was ist eine ausreichende Charakterisierung? Gehört dazu Chiralität, Toxizität, Genotoxizität, Abbau, Biodistribution, Proteincorona?
LNP surface properties = Proteincorona.
Das dürfte interessant werden. Das Proof-of-Principle Paper dazu ist noch ein Preprint.
Das Zeta Potenial, das bei -3,13 mV liegen sollte, wurde bei den COVID-Produkten nicht gemessen. Das wäre ein Fortschritt, der bedeuten könnte, dass kaum eine Charge durch die Qualitätsprüfung kommen könnte. Nur… wie soll man das messen?
Problem Nr. 8
“Mögliche produkt- und verfahrensbedingte Verunreinigungen im Endprodukt sollten erörtert werden.”
Schön, wir schreiben eine Erörterung wie in der Schule und heften die dann ab.
Mit diskutiert werden sollen dabei Addukte und nicht verkapselte RNA.
Das Hauptproblem der verkapselten Plasmidvorlage wird sicherheitshalber lieber nicht addressiert.
Problem Nr. 9
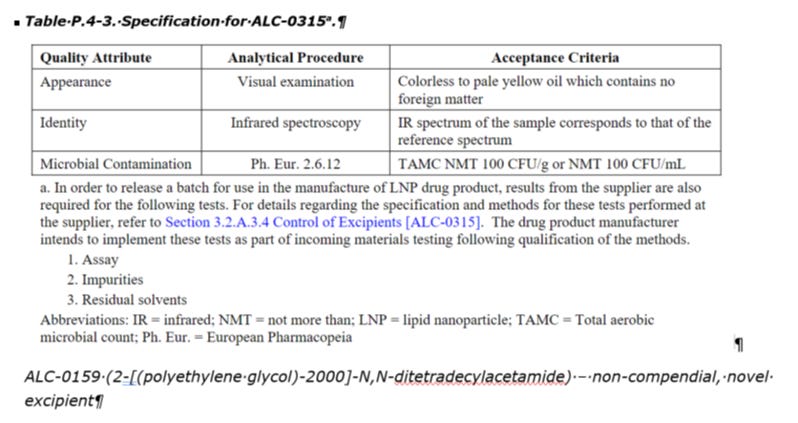
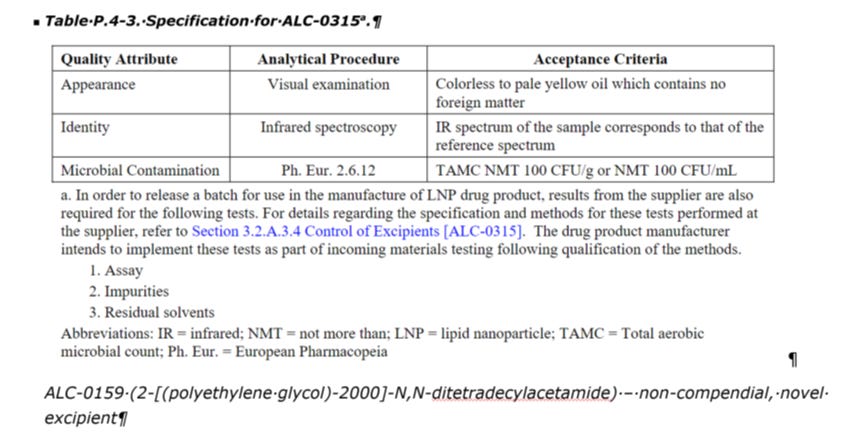
Bei Lipidhilfsstoffen, die in Arzneibüchern aufgeführt sind, müssen unter Umständen zusätzliche Qualitätsmerkmale geprüft werden, um sicherzustellen, dass die Qualität des Materials für die Bildung stabiler LNPs geeignet ist.
Also nicht so, wie man es bisher für die Lipide der COVID-Plörren gemacht hat, nämlich Sichtkontrolle, Infrarotspektroskopie und mikrobielle Untersuchung?
Sondern Massenspektrometrie und HPLC?
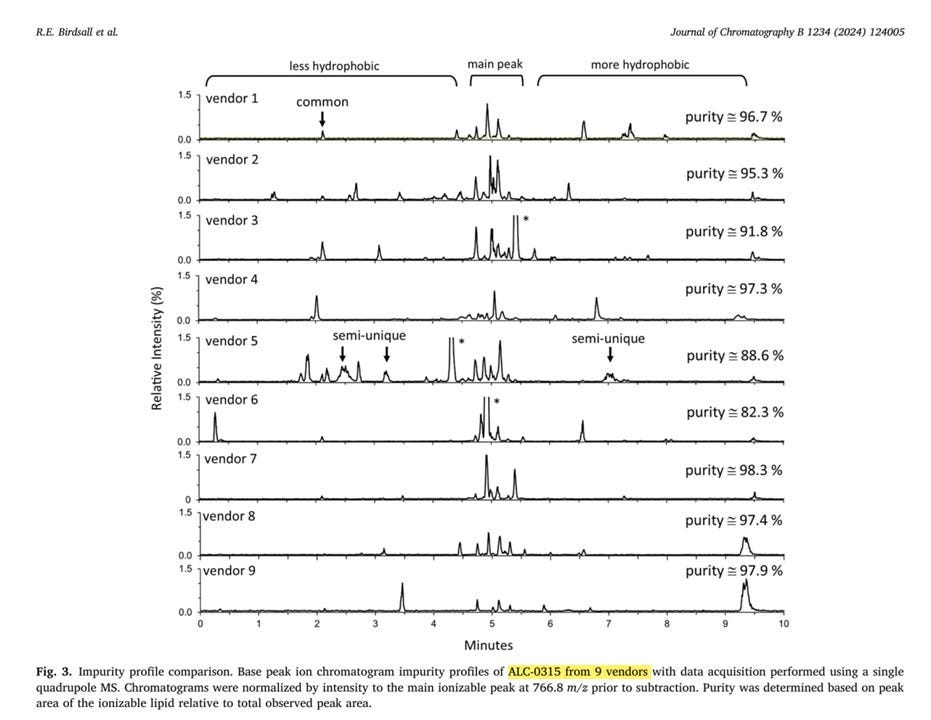
Nur noch 99,9% reine Lipide, ohne Fragmente unbekannter chemischer Struktur uns unbekannter chemischer Eigenschaften? Das könnte teuer werden, wenn sie es überhaupt schaffen.
Und ja, in Zukunft soll man HPLC machen. Warum hat man das bisher nicht gemacht?
Dabei bleibt aber noch das Problem der Chiralität unbehandelt und ob Gemische verwendet werden dürfen.
Es scheint ein gesondertes Dossier zu den Lipiden zu geben: EMA guideline on excipients in the dossier for application for marketing authorisation of a medicinal product. Da müsste man noch genauer schauen, was das für die Lipide bedeutet.
Problem Nr. 10
“Es sollten Spezifikationen für die Freigabe des Endprodukts und die Haltbarkeitsdauer vorgeschlagen werden.”
Von wem sollen diese Spezifikationen vorgeschlagen werden? Hoffentlich nicht vom Hersteller. Das muss man zentral bestimmen. Bei USP zum Beispiel.
“Die Freigabespezifikationen für jede Charge von mRNA-Impfstoff-Fertigprodukten sollen voraussichtlich Prüfungen hinsichtlich der mRNA-Identität, des mRNA-Gehalts, der Reinheit und der Verunreinigungen, der LNP-Eigenschaften, der Wirksamkeit, der Funktionalität sowie allgemeine Prüfungen und Sicherheitsprüfungen umfassen.”
Nur wie soll das getestet werden? Pfizer hat bei den COVID-Plörren zielsicher immer genau den Test genommen, der das Problem NICHT detektiert. Das muss von Extern vorgegeben werden. USP arbeitet daran.
Produktparameter wie pH-Wert, Osmolalität, sichtbare und nicht sichtbare Partikel, Partikel und extrahierbares Volumen.
Sichtbare Partikel sind eine Sache der Selbstkontrolle des Herstellers. Wenn Sichtbare Partikel enthalten sind, passiert erst mal gar nichts. Warum dann überhaupt darauf testen?
Problem Nr. 11
Bei zwei- oder mehrwertigen Impfstoffen sind zusätzlich zu den allgemeinen Leitlinien einige spezifische Aspekte im Abschnitt zum Fertigprodukt zu beachten.
Das Hauptproblem der Hybriden Proteine wird ignoriert.
Problem Nr. 12
Die selben Regeln gelten für saRNA zuzüglich der Charakterisieurng der zusätzlichen Proteine.
Shedding Studien fehlen aber (in beiden Fällen).
Fazit:
Vieles von dem, was in diesem fachlich nicht so herausragenden Draft verlangt wird, fehlt bereits bei den COVID-modRNA-LNP Produkten. Hätte man diese Studien verlangt, wären sie wahrscheinlich heute noch nicht auf dem Markt.
Verlangt man alles, was nötig wäre, muss man erst einmal die Methoden zur Charakterisierung entwickeln, wie die Analyse der 3D Struktur der modRNA im Vergleich zur ursprünglichen, natürlichen mRNA. Damit wäre man im Bereich der Epitranskriptomik, die zumindest schon mal einen Namen hat und sich in der Methodenentwicklung befindet.
Bis diese Methoden entwickelt sind und validiert zur Verfügung stehen, können Jahre bis Jahrzehnte vergehen.
Unterstützungsmöglichkeiten:
Bücherwunschzettel: https://www.amazon.de/registries/gl/owner-view/30LG3DJ4ET90L?ref_=list_d_gl_lfu_nav
Andere Unterstützungsmöglichkeiten für Holgers und meine Forschung:
Konto für Unterstützung für das Projekt Scan 2000
Dr. Merse DE34 4305 0001 0302 7851 75 Sparkasse Bochum
Horst Reissner: IBAN DE51 4401 0046 0406 4514 67
Dr. S. Stebel: https://ko-fi.com/einmalmitprofisarbeiten
Admin. (2023, July 26). Short notes on TRNA structure. BYJUS. https://byjus.com/neet/short-notes-of-biology-for-neet-trna-structure/
Butcher SE, Pyle AM. The molecular interactions that stabilize RNA tertiary structure: RNA motifs, patterns, and networks. Acc Chem Res. 2011 Dec 20;44(12):1302-11. doi: 10.1021/ar200098t. Epub 2011 Sep 7. PMID: 21899297. https://pubmed.ncbi.nlm.nih.gov/21899297/
Hennig J. Structural Biology of RNA and Protein-RNA Complexes after AlphaFold3. Chembiochem. 2025 Apr 1;26(7):e202401047. doi: 10.1002/cbic.202401047. Epub 2025 Feb 20. PMID: 39936575. https://pubmed.ncbi.nlm.nih.gov/39936575/
Bank, R. P. D. (n.d.). RCSB PDB – 1MHK: Crystal Structure Analysis of a 26mer RNA molecule, representing a new RNA motif, the hook-turn. https://www.rcsb.org/structure/1MHK
McKernan, K., Kyriakopoulos, A. M., & McCullough, P. A. (2021). Differences in Vaccine and SARS-CoV-2 Replication Derived mRNA: Implications for Cell Biology and Future Disease. OSF. https://doi.org/10.31219/osf.io/bcsa6
Hagenbüchle O, Larson D, Hall GI, Sprague KU. The primary transcription product of a silkworm alanine tRNA gene: identification of in vitro sites of initiation, termination and processing. Cell. 1979 Dec;18(4):1217-29. doi: 10.1016/0092-8674(79)90234-4. PMID: 519766. https://pubmed.ncbi.nlm.nih.gov/519766/
Mauro VP, Chappell SA. A critical analysis of codon optimization in human therapeutics. Trends Mol Med. 2014 Nov;20(11):604-13. doi: 10.1016/j.molmed.2014.09.003. Epub 2014 Sep 25. PMID: 25263172; PMCID: PMC4253638. https://pubmed.ncbi.nlm.nih.gov/25263172/
DocCheck, M. B. (n.d.). Oncomir – DocCheck Flexikon. DocCheck Flexikon. https://flexikon.doccheck.com/de/Oncomir
Grumelot, S., Mohammed, N., Colonrosado, J., Sadeghi, S. A., Fang, F., Hilsen, K., Shango, B., Saei, A. A., Murray, A. M., Mitchell, M. J., Borhan, B., Sun, L., Vali, H., Whitehead, K. A., & Mahmoudi, M. (2025). Lipid nanoparticle protein coronas form via lipoprotein fusion rather than shell-like adsorption. Biorxiv. https://doi.org/10.64898/2025.12.21.695162, https://www.biorxiv.org/content/10.64898/2025.12.21.695162v1.full.pdf
Rapporteur Rolling Review critical assessment report, Quality aspects, S. 159
Rapporteur Rolling Review critical assessment report, Quality aspects, S. 160
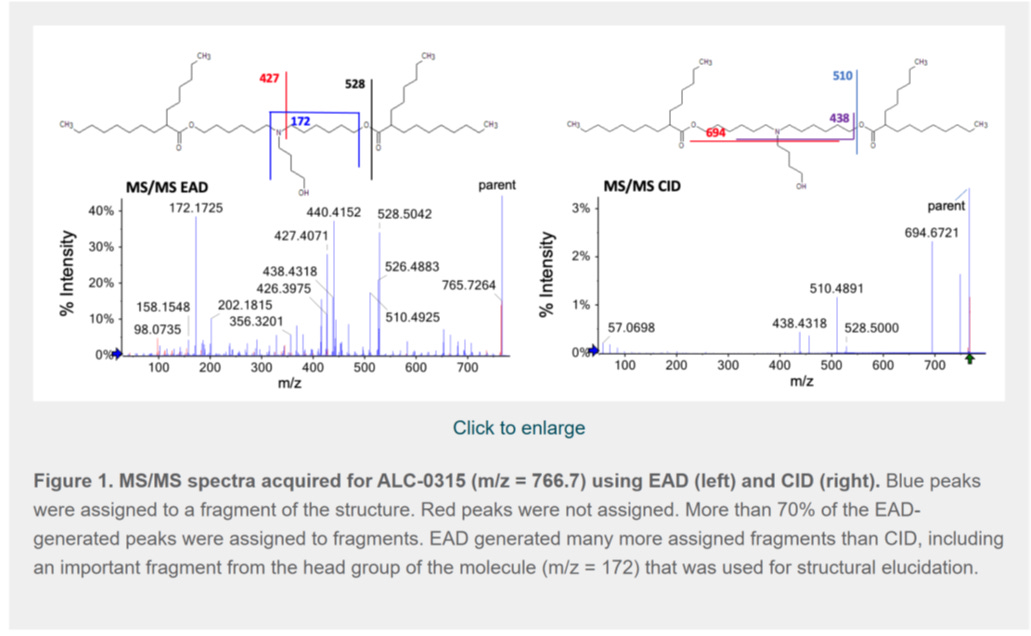
Structural characterization of the cationic lipid nanoparticle component, ALC-0315, and its impurities using electronactivated dissociation (EAD)-based MS/MS fragmentation. (n.d.). https://sciex.com/tech-notes/biopharma/structural-characterization-of-the-cationic-lipid-nanoparticle-c
Birdsall RE, Han D, DeLaney K, Kowalczyk A, Cojocaru R, Lauber M, Huray JL. Monitoring stability indicating impurities and aldehyde content in lipid nanoparticle raw material and formulated drugs. J Chromatogr B Analyt Technol Biomed Life Sci. 2024 Feb 15;1234:124005. doi: 10.1016/j.jchromb.2024.124005. Epub 2024 Jan 18. PMID: 38246008. https://pubmed.ncbi.nlm.nih.gov/38246008/
Excipients in the dossier for application for marketing authorisation of a medicinal product – Scientific guideline | European Medicines Agency (EMA) https://www.ema.europa.eu/en/excipients-dossier-application-marketing-authorisation-medicinal-product-scientific-guideline
News detail. (2026, January 13). European Directorate for the Quality of Medicines & HealthCare. https://www.edqm.eu/en/w/european-pharmacopoeia-updates-testing-for-particulate-contamination-in-pharmaceutical-preparations