Im Dezember 2024 habe ich mich bereits mit den Japanischen Daten zur selbstamplifizierenden RNA (saRNA) Kostaive beschäftigt.
Damals gab es den EU EPAR noch nicht.
Nun gibt es den EPAR.
Vergleichen wir einmal, was man in der EU nicht meldet, aber in Japan in den Unterlagen offiziell drinnen steht.
Hier die Japanischen Daten im Detail:
https://www.pmda.go.jp/files/000269813.pdf
Zu den Highlights aus den japanischen Daten zählt, dass man Verunreinigungen rundweg zugibt. Dazu findet man in den EU Daten seltsamerweise nichts.
2.1.5.2 Produktbezogene Substanzen/produktbezogene Verunreinigungen Die produktbezogene Verunreinigung ist Verunreinigung A, die durch die Spezifikationen für den Wirkstoff angemessen kontrolliert wird. Es wurden keine produktbezogenen Substanzen identifiziert.
2.1.5.3 Prozessbedingte Verunreinigungen Als prozessbedingte Verunreinigungen wurden restliche Plasmid-DNA, Verunreinigung B, Verunreinigung C und elementare Verunreinigungen identifiziert. Restliche Plasmid-DNA, Verunreinigung B und Verunreinigung C werden durch die Spezifikationen für den Wirkstoff angemessen kontrolliert. Es wurde nachgewiesen, dass elementare Verunreinigungen während des Herstellungsprozesses vollständig entfernt werden.
Während der Entwicklung des Wirkstoffs wurde das Herstellungsverfahren von Verfahren A auf Verfahren B umgestellt. Die wesentliche Änderung bestand in der Einbindung des ************************-Verfahrens in den Herstellungsprozess.
Der in nichtklinischen Studien verwendete Wirkstoff wurde nach Verfahren a hergestellt, in klinischen Studien nach Verfahren a oder b, und der Wirkstoff für das geplante Impfstoffprodukt wird nach Verfahren b hergestellt. Für die Verfahrensänderungen wurde die Vergleichbarkeit zwischen dem Wirkstoff vor und nach der Änderung nachgewiesen.
Die folgende Tabelle zeigt die von den Wirkstoffen (mRNA-2002, mRNA-2105 und mRNA-2106) der Arzneimittelkandidaten (ARCT-021, ARCT-154 [Kostaive] und ARCT-165 [Impfstoff für Varianten]) kodierten S-Protein-Typen sowie die eingeführten Mutationen.
Generell sind die japanischen Zulassungsdaten DEUTLICH ausführlicher als der EU EPAR. Im EPAR wird vieles nicht erwähnt, was in den japanischen Daten klar formuliert ist.
Ich empfehle daher, für die Grundlagen, die Artikeln zu den japanischen Zulassungsdaten zu lesen und danach erst die EU-Daten, damit man auch den Unterschied zwischen diesen Behörden begreift.
Die EMA Unterlagen:
Im Gegensatz zu Japan wird das Produkt hier von Seqirus Netherlands B.V. vertrieben und nicht von Meiji Seika.
“Als Teil der CSL Gruppe kann CSL Seqirus auf über hundert Jahre Erfahrung mit Impfstoffen zurückblicken. Von 1916 bis heute wird CSL durch die Aufgabe motiviert, mithilfe neuester Technologien Leben zu retten.”
Die Erklärungen, was ARCT-154 und ARCT-165 sind und worin diese sich unterscheiden fehlt im EU-Dokument, welches nicht einmal maschinenlesbar ist. Ich musste die OCR selbst machen. https://www.ema.europa.eu/en/medicines/human/EPAR/kostaive
ARCT-154 und ARCT-165 sind in diesem Fall tatsächlich vergleichbar, weil sie beide für das Spike-Protein kodieren, welches sich aber in einigen Aminosäuren unterscheidet.
Die Tierversuche sind in den japanischen Daten DEUTLICH ausführlicher und bereits in Teil 2 zu den japanischen Daten behandelt genau wie die Studien in Menschen.
“Bei Mäusen wurden mRNA und ATX-126 im Muskel, in den Lymphknoten (LN, Kniekehlen- und Leistenlymphknoten), in der Milz, in der Leber, im Herzen, in den Eierstöcken, in der Lunge und in den Hoden nachgewiesen. Im Gehirn wurden zum frühesten Zeitpunkt (2 Stunden) sehr geringe Konzentrationen von mRNA nachgewiesen, ATX-126 wurde jedoch zu keinem Zeitpunkt im Gehirn nachgewiesen. Die mRNA war 31 Tage nach der Verabreichung aus den meisten Geweben abgebaut. ATX-126 wurde in geringen Konzentrationen in den Geweben nachgewiesen, und am Tag 31 nach der Verabreichung enthielten die meisten Gewebe < 1 % der verabreichten Dosis von ATX-126, mit Ausnahme der Muskeln und der Leber, die durchschnittlich 3 % bzw. 4 % aufwiesen. Die höchsten Konzentrationen des SARS-CoV-2-S-Glykoproteins wurden im Muskel, dem Zielgewebe, beobachtet, während in der Lunge und den Eierstöcken sehr geringe Konzentrationen nachgewiesen wurden, die bis zum 15. Tag abgebaut waren, außer in den LN. In der 4-wöchigen GLP-Studie zur Toxizität bei wiederholter Verabreichung an Kaninchen wurde mRNA in der Milz nachgewiesen. ATX-126 wurde im Plasma, in den Mesenteriallymphknoten, in der Leber, in der Milz, an den Injektionsstellen und in den Eierstöcken nachgewiesen. In der GLP-Studie zur Fertilität, Embryo-Fetal- und postnatalen Entwicklung bei Kaninchen wurde keine mRNA in den fötalen Geweben oder der Plazenta nachgewiesen, jedoch wurden geringe Konzentrationen in den mütterlichen Plasmaproben von weniger als 10 % der mütterlichen Tiere festgestellt. Niedrige Konzentrationen von mRNA wurden nur in 1 von 20 fetalen Plasmaproben der Bc-Dosisgruppe nachgewiesen. ATX-126 wurde nicht im fetalen Plasma oder in fetalen Geweben nachgewiesen, wohl aber in der Plazenta und im mütterlichen Plasma, was auf einen fehlenden Transfer in das fetale Gewebe bei geimpften Muttertieren hindeutet.”
Die von der EMA geschwärzten Daten findet man ungeschwärzt in den japanischen Daten: 10µg
Was will die EMA mit diesen Schwärzungen öffentlicher Daten erreichen?!
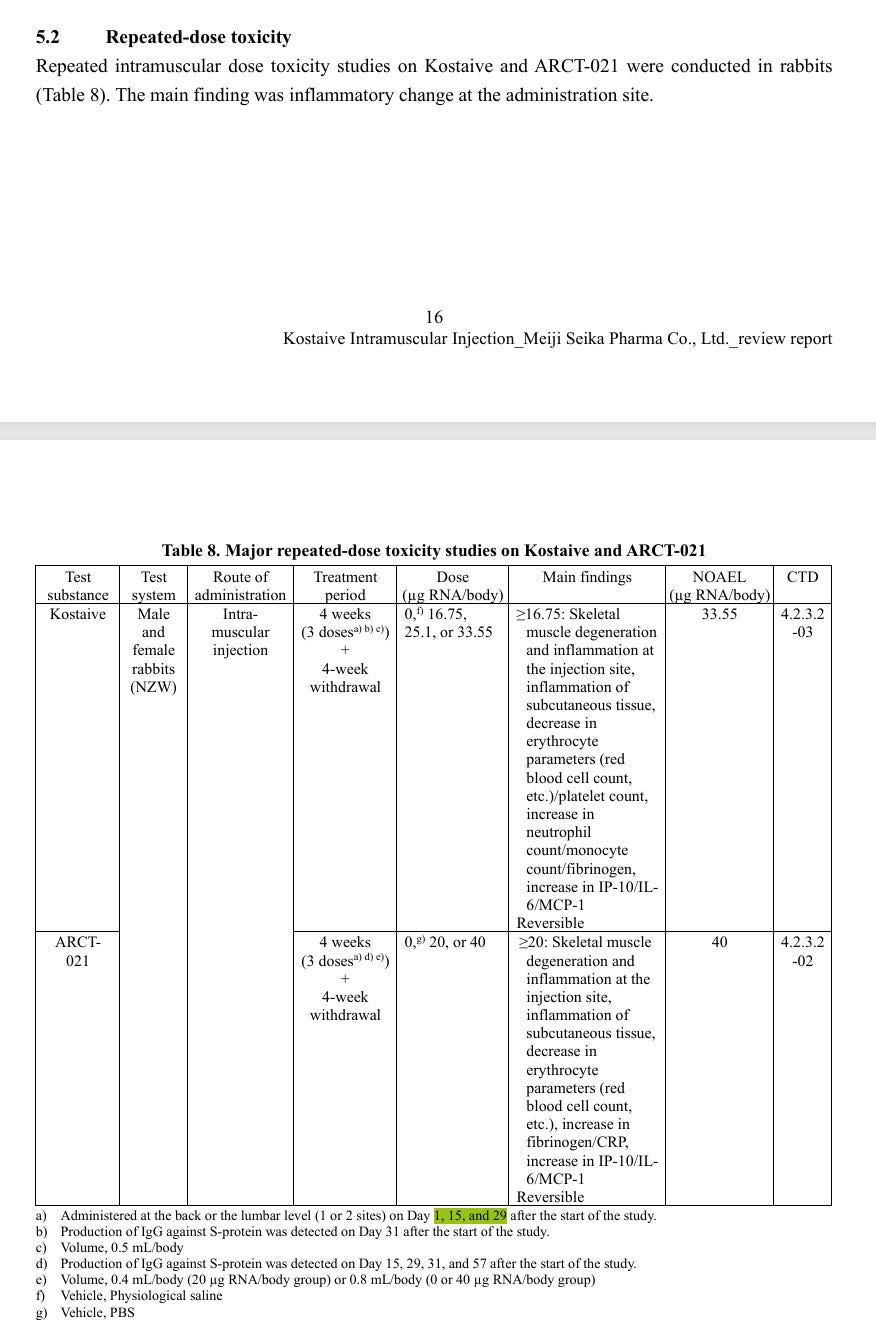
Die gleichen sinnlosen Schwärzungen in der reapeat-dose Toxicity Study, die es in den japanischen Daten schön als übersichtliche Tabelle gibt.
Generell sind die japanischen Daten deutlich übersichtlicher als Tabellen.
“Es wurden keine Genotoxizitätsstudien mit ARCT-021 oder ARCT-154 durchgeführt, da diese für die Zulassung von Impfstoffen nicht als erforderlich angesehen werden (Siebach et al., 2021; WHO, 2005). Genotoxizitätsstudien, die mit ARCT-810 (einem weiteren mRNA-Produkt von Arcturus in klinischer Entwicklung, das ein ähnliches Lipid wie Kostaive enthält) zur Behandlung von Ornithintranscarbamylase-Mangel und dem leeren LNP (ohne mRNA) durchgeführt wurden, fielen in GLP-konformen Genotoxizitätsstudien beide negativ aus; bakterieller Mutagenitätstest (Ames-Test), In-vitro-Test an Säugetierzellen (menschliche periphere Blutlymphozyten) und ein In-vivo-Mikronukleustest an Nagetieren in Studien, die gemäß den ICH-S2-Richtlinien durchgeführt wurden. Eine In-silico-Analyse der potenziellen bakteriellen Mutagenität für ATX-126 war negativ. Auf der Grundlage dieser Beweislage ist nicht zu erwarten, dass Kostaive genotoxisch ist.”
In silico-Analyse ist ein anderer Begriff für Modellierung. Und weil das Modell sagt, das ist OK, geht man davon aus, dass schon nichts passieren wird.
Erneut geschwärzter Fließtext im vergleich zu einer übersichtlichen, japanischen Tabelle ohne Schwärzungen.
Die Phase 3 Studie habe ich schon ausführlich in Teil 2 der japanischen Daten behandelt.
Wie viele Dosen wirklich zum Einsatz kamen, weiß man so genau nicht:
“Bis zum 27. Mai 2025 wurden in Japan insgesamt 1165 Ampullen verkauft. Jede Ampulle enthält 16 Dosen Kostaive. Daher lässt sich schätzen, dass bis zu 18.640 Standarddosen für Impfungen verwendet wurden.”
1165 Ampullen wurden verkauft. Wie viele und wie viel davon vernichtet wurden, weiß keiner so genau.
“Dies steht im Gegensatz zu Adenoviren, die den Zellkern der Wirtszelle während ihres Replikationszyklus umfassend umgestalten (Hidalgo und Gonzalez, 2019), was zu einer geringen Integrationshäufigkeit führt (Wang et al., 2”
Kleiner Hinweis: ADENOVIREN = Johnson&Johnsons und AstraZenecas Coronaimpfungen.
Das Nutzen:Risiko-Profil wird selbst vom Anbieter nur als akzeptabel bezeichnet und nicht als gut oder sehr gut.
Daten zu Schwangerschaft sind nicht wirklich ausreichend vorhanden.
Für die adverse effects auf special interest, gibt es im Anhang Fragebögen:
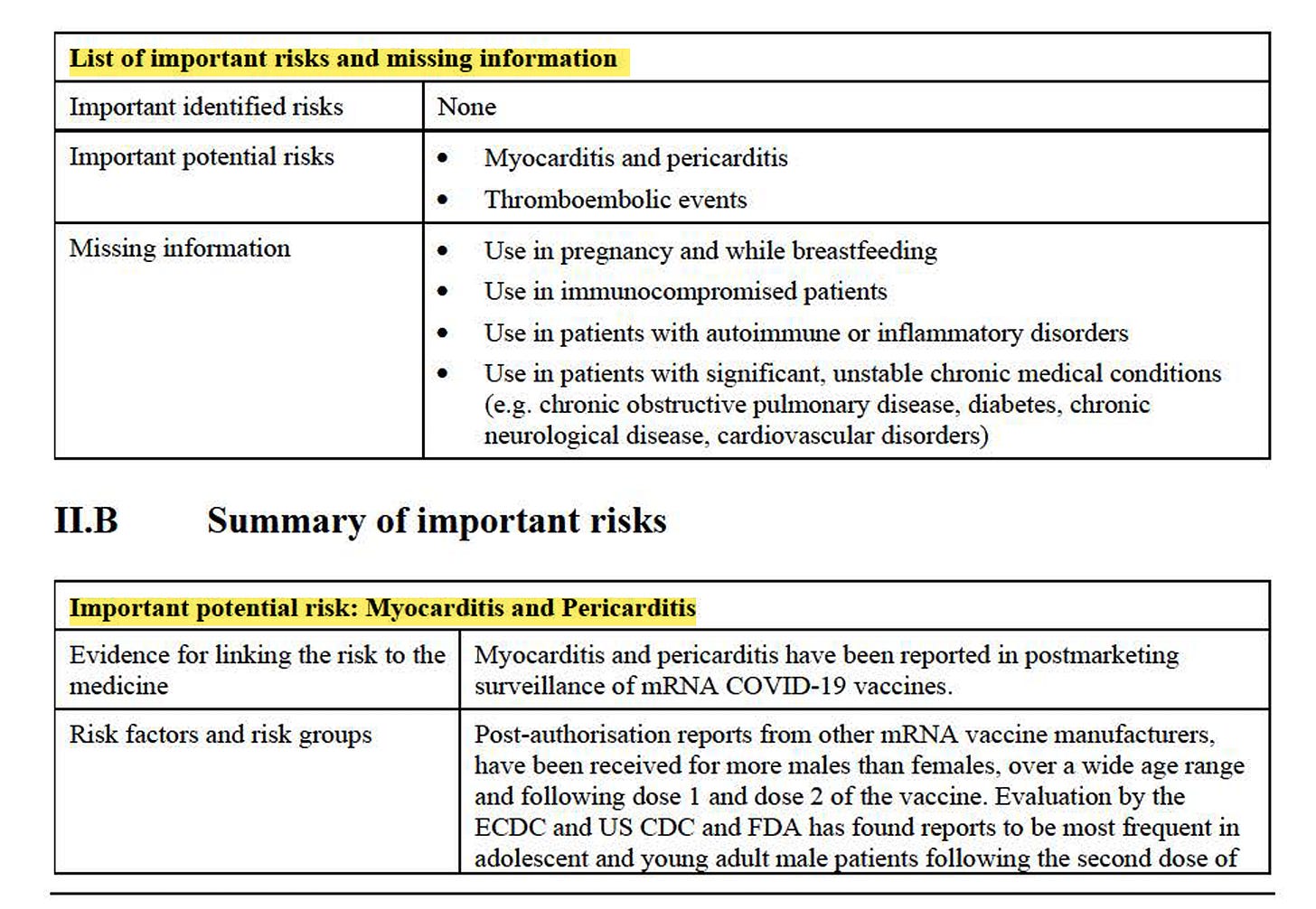
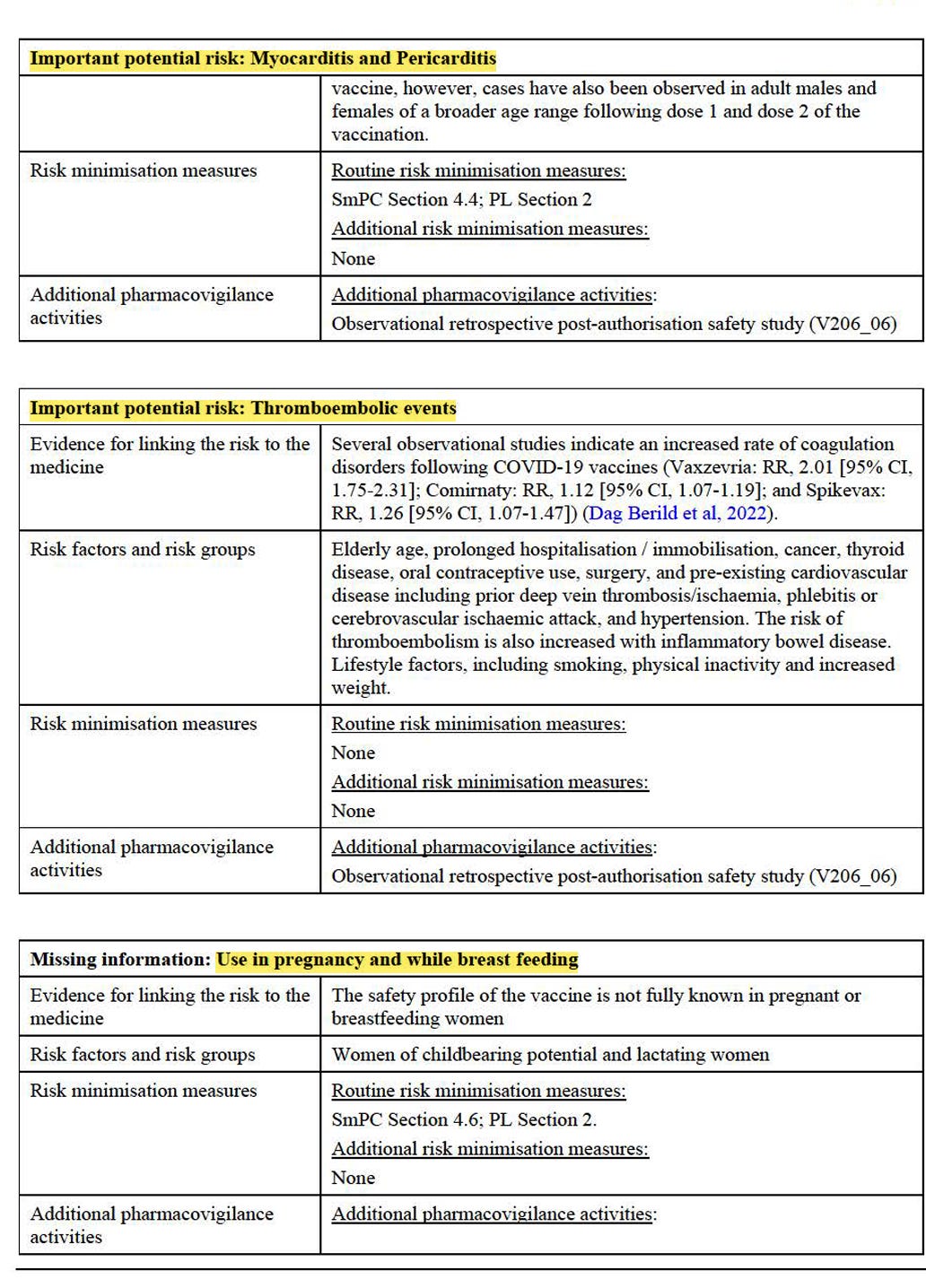
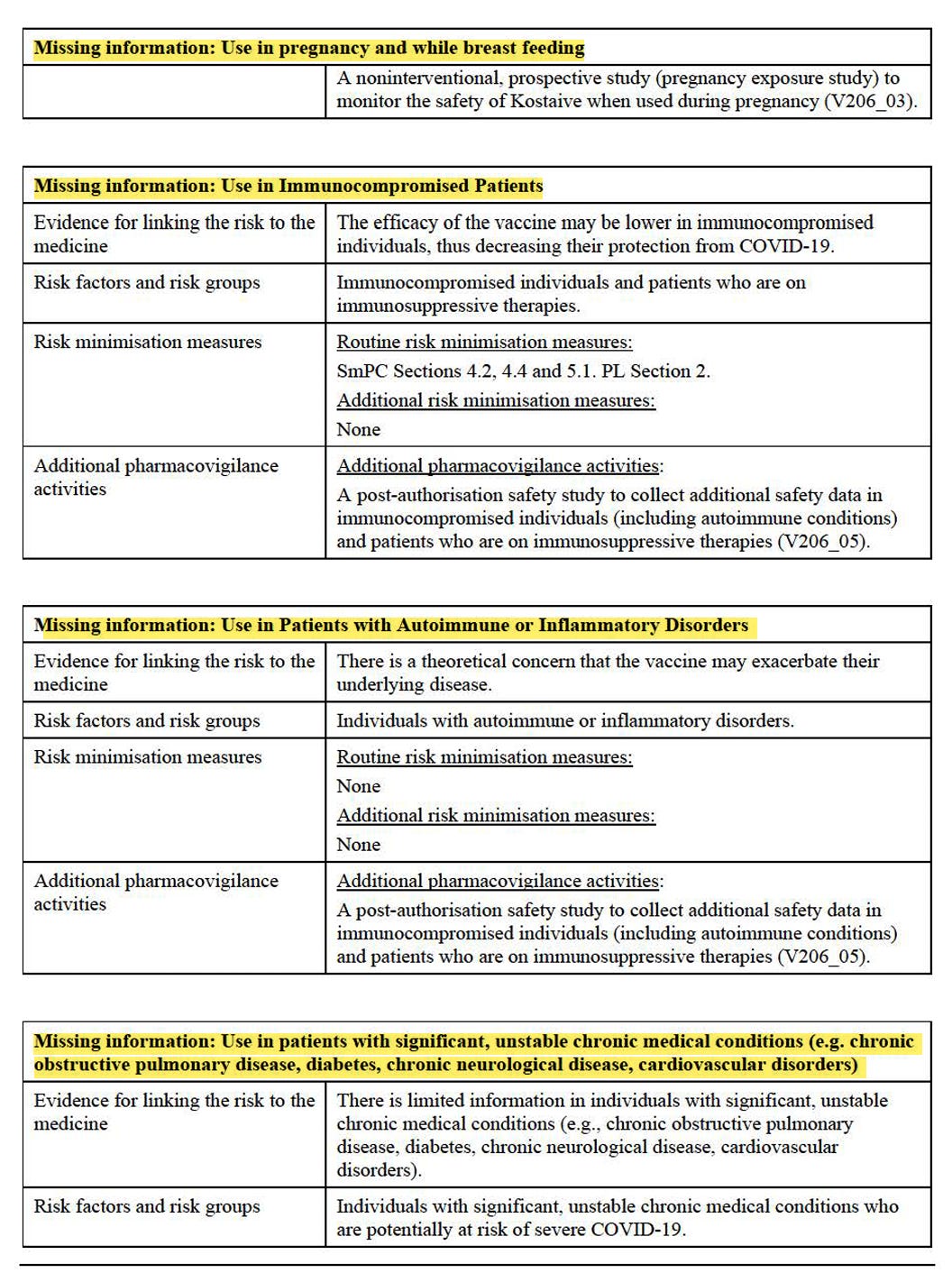
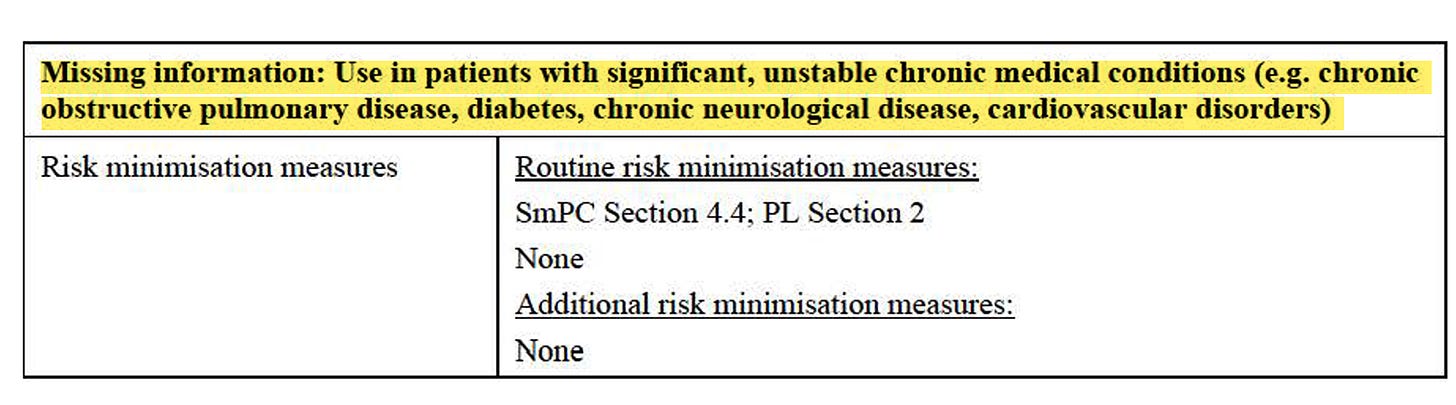
Die Liste wichtiger Risiken und fehlender Informationen ist zumindest recht übersichtlich gestaltet. Eigentlich dürfen nur total gesunde Menschen ohne Risiken das Produkt bekommen, exakt jene, die es nicht brauchen.
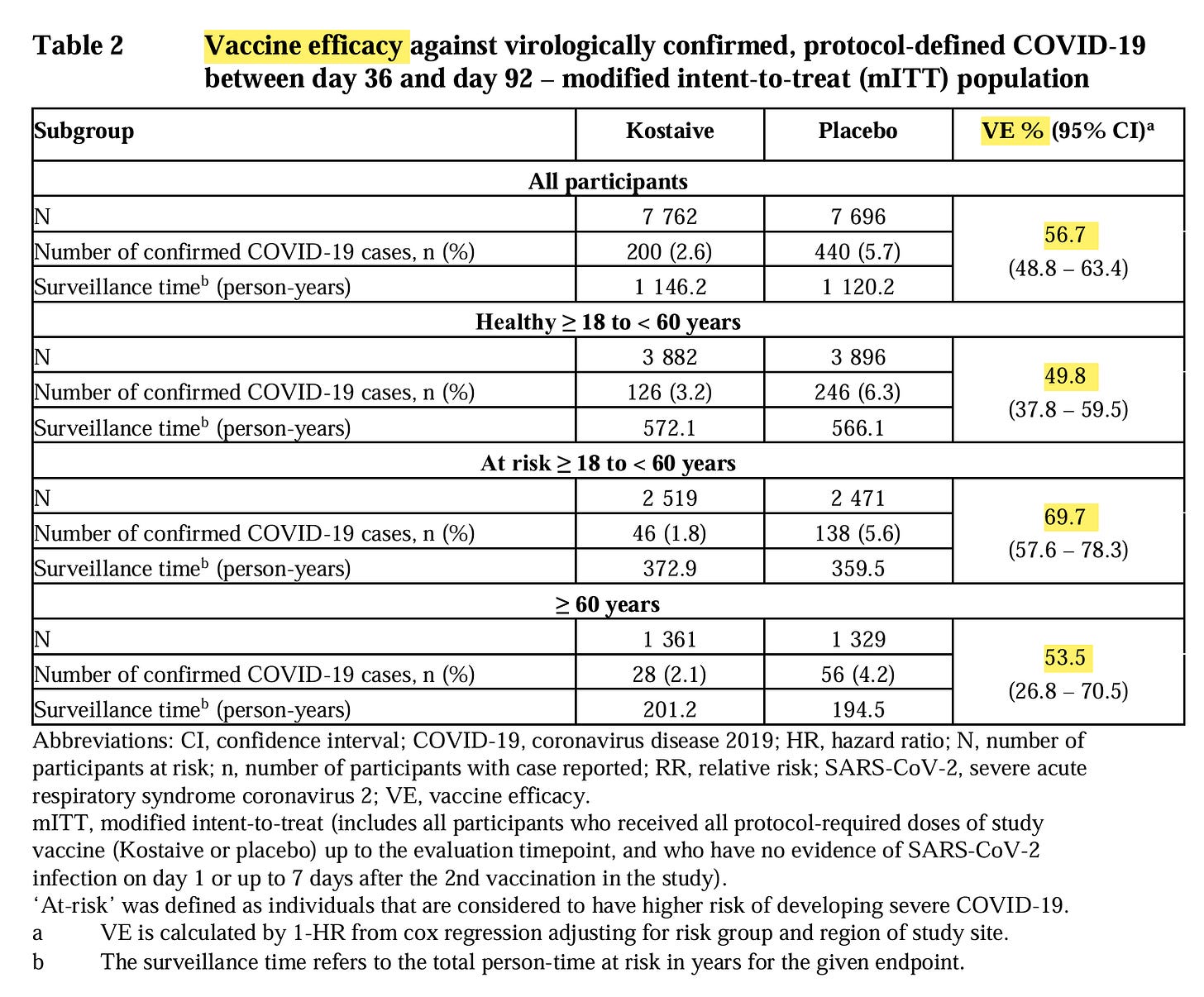
Die Vaccine Efficiency ist so schlecht wie man es aus den japanischen Daten kennt:
Einen Nutzen haben Menschen mit Risiko, welche eigentlich, laut Datenlage, dieses Produkt eher nicht bekommen sollten. Bei gesunden Menschen reißt das Produkt die 50% Hürde und dürfte für diese Menschen gar nicht zugelassen werden.
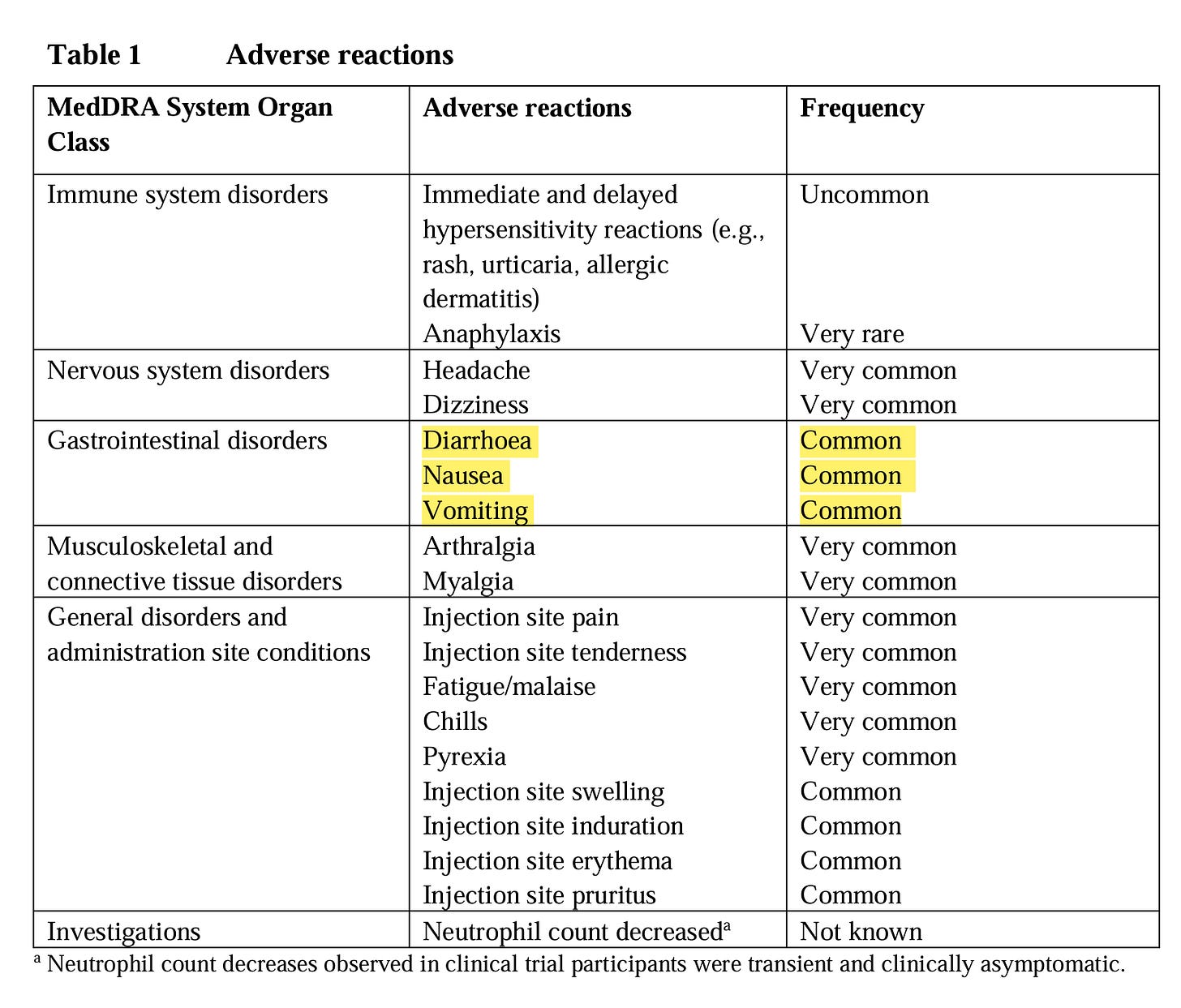
Die Nebenwirkungen sind dafür häufig bis sehr häufig, besonders auch Durchfall, Übelkeit und Erbrechen. https://www.ema.europa.eu/en/documents/product-information/kostaive-epar-product-information_en.pdf
Fazit:
Vieles, was in den japanischen Daten öffentlich steht, fehlt in den EU EPAR Daten komplett, wie der Verfahrenswechsel und die Prozessbedingten Verunreinigungen.
Die EMA schwärzt Daten, die in den japanischen Unterlagen nachzuschauen sind, keine Ahnung, was das soll.
Das Produkt sieht immer noch so schlecht und nutzlos aus, wie in den japanischen Daten, nur hat man die richtig bedenklichen Aspekte teils komplett weggelassen.
Die japanische Behörde ist deutlich transparenter als die EMA und gibt viel mehr Daten frei, als die EMA.
Warum das so ist, sollte man mal bei der EMA nachfragen.
Unterstützungsmöglichkeiten:
Bücherwunschzettel: https://www.amazon.de/registries/gl/owner-view/30LG3DJ4ET90L?ref_=list_d_gl_lfu_nav
Andere Unterstützungsmöglichkeiten für Holgers und meine Forschung:
Konto für Unterstützung für das Projekt Scan 2000
Dr. Merse DE34 4305 0001 0302 7851 75 Sparkasse Bochum
Horst Reissner: IBAN DE51 4401 0046 0406 4514 67
Dr. S. Stebel: https://ko-fi.com/einmalmitprofisarbeiten
Unser Unternehmen. (n.d.). https://www.cslseqirus.de/unser-unternehmen