Da ich immer wieder die gleichen Fragen bekomme, gibt es heute einen Exkurs in die VDJ-Rekombination, also eine Zusammenfassung der Vorlesung “Einführung in die Immunbiologie” aus dem ersten Semester 1997 ergänzt mit aktuellen Daten.
VDJ-Rekombination auf genetischer Ebene war meine Prüfungsfrage im Nebenfach Immunologie am MPI für Immunbiologie in Freiburg.
Das sind prüfungsrelevante Grundlagen, die auch abgefragt werden und somit keine Verschwörungstheorie.
1987 gab es für die Klärung der VDJ-Rekombination den Nobelpreis für den japanischen Molekularbiologen Susumu Tonegawa.
Die Grundlagen kann man sich auch als Nobel Price Lecture geben.
https://www.nobelprize.org/prizes/medicine/1987/tonegawa/lecture/
https://www.nobelprize.org/uploads/2018/06/tonegawa-lecture.pdf
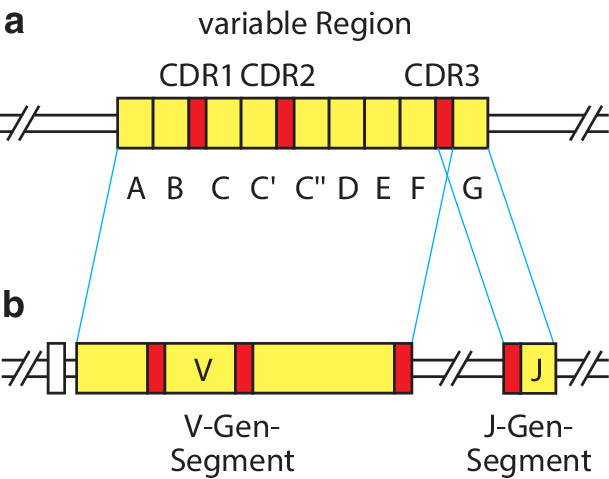
Was ist die VDJ Rekombination?
Die VDJ-Rekombination ist ein genetischer Prozess, der im Knochenmark stattfindet. Hierbei werden Gene in zufälliger Reihenfolge zu größeren Einheiten zusammengestellt, könnte man grob sagen. Mathematisch haben wir es mit Rekombination zu tun. Jede Kugel ist einmal vorhanden, es wird nicht zurückgelegt, aber es gibt viele Kugeln, die auf unterschiedliche Art und Weise kombiniert werden.
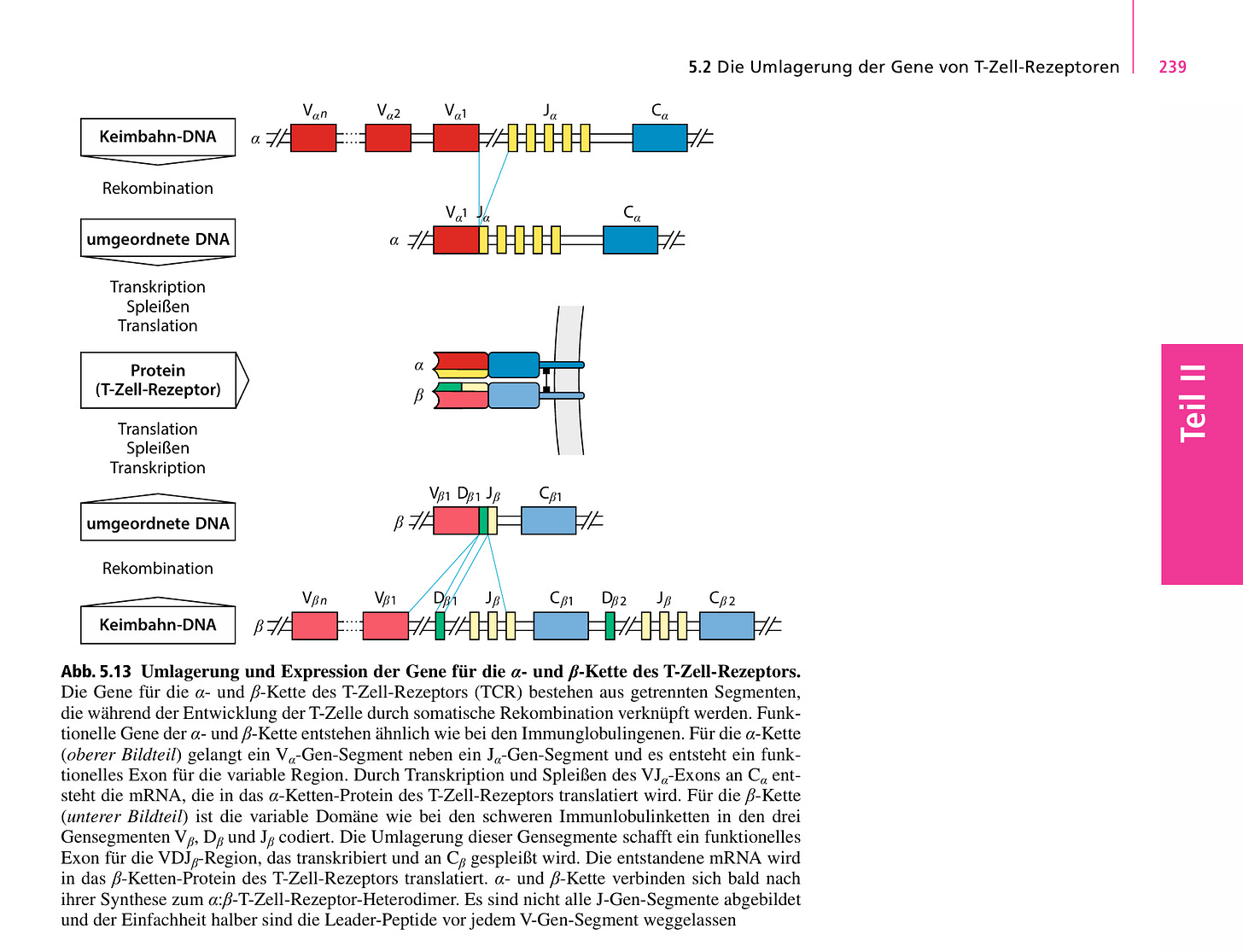
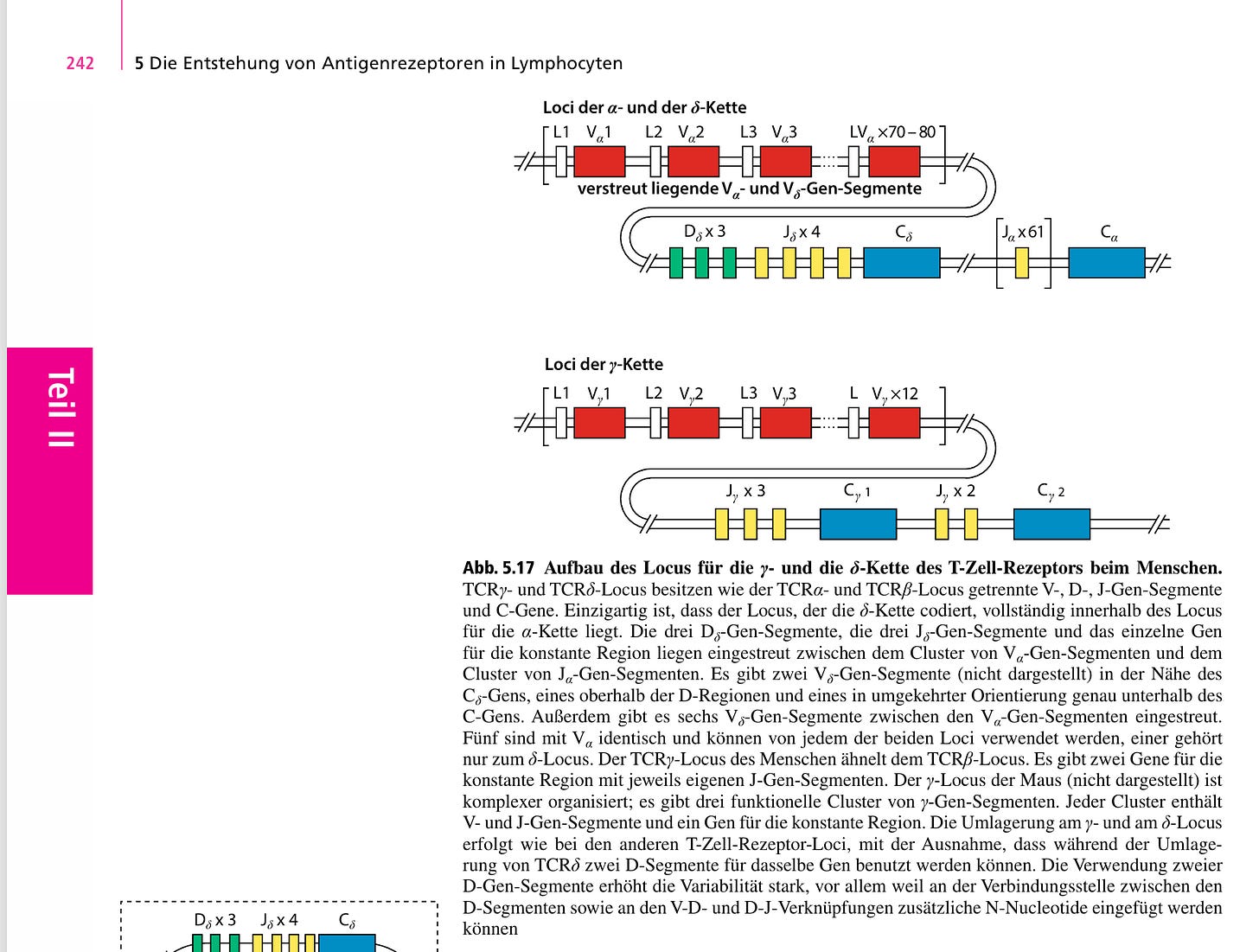
Im Lehrbuch Janeway Immunologie 9. Auflage, wir das in Kapitel 5.2 Seite 239 wie das bei den T-Zell Rezeptoren gemacht wird, wie für die Antigenerkennung auf T-Zellen zuständig sind.
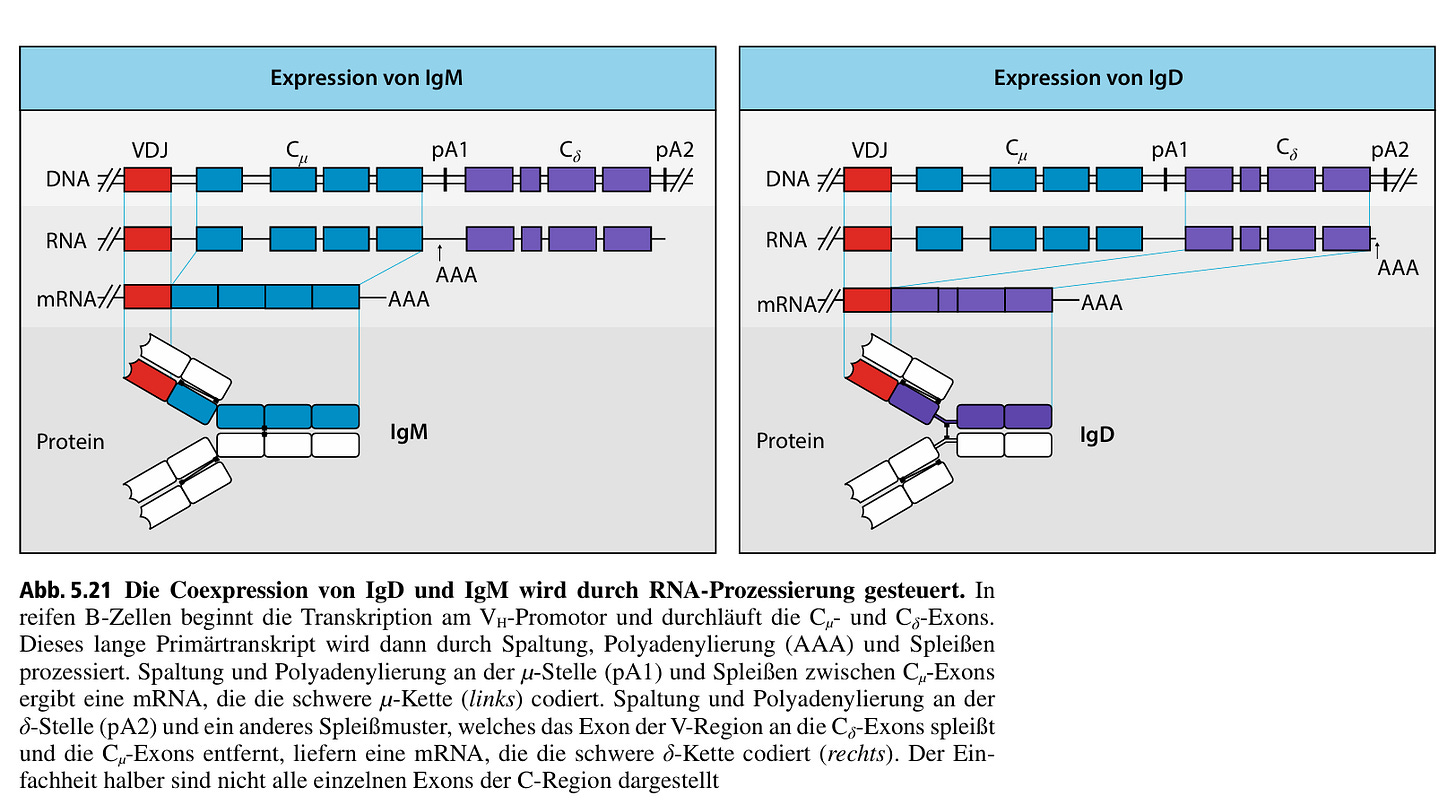
Bei B-Zellen läuft es analog, da verweist das Lehrbuch im Bild auf Seite 247 nur noch auf VDJ, lies bei T-Zellen, wie das geht.
Das Kapitel in der Version von 2018 gibt es sogar kostenlos online.
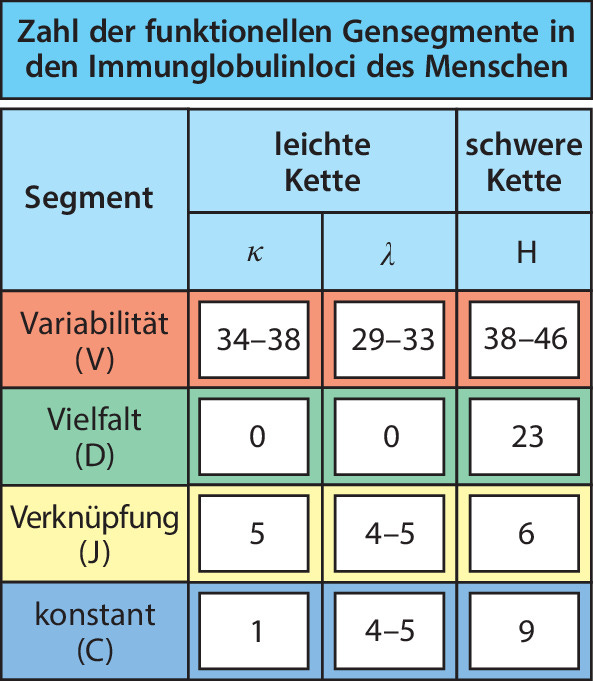
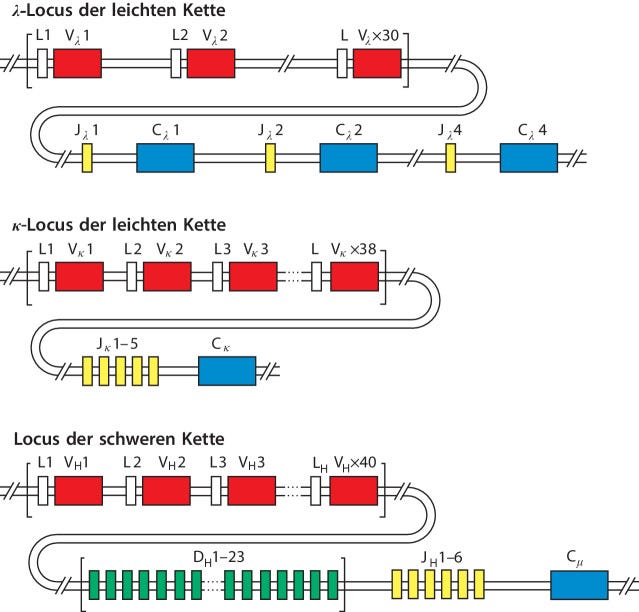
Für die mitlesenden Mathematiker die Daten für die Berechnung der möglichen Varianten:
Und auf welche Art und weise die Gene gezogen werden:
Welche Folgen hat die VDJ-Rekombination für die erworbene Immunität?
Da Antigene auf Molekülen namens MHC nach dem Schlüssel-Schloss Prinzip präsentiert werden und die V(D)J-Rekombination zwar das riesige „Start-Sortiment“ an Erkennungsmustern bildet, muss anschließend im Thymus noch sortiert werden. Wer körpereigene Strukturen erkennt, wird eliminiert, um Autoimmunangriffe zu verhindern. Das ist aber nicht Thema dieses Artikels, das läuft im Hintergrund als Qualitätskontrolle und Qualitätssicherung.
Durch die VDJ-Rekombination sind Milliarden verschiedener T-und B-Zellen entstanden, die theoretisch fast alles binden können. Man nennt das die antigenunabhängige Differenzierung. Das Immunsystem hält für fast jeden Erreger eine „passende“ Zelle bereit – allerdings ist diese Bindung oft noch sehr schwach und ungenau, aber es bindet und erfüllt erst einmal seine Aufgabe. Dieses Grundstock an Ausrüstung stellt sicher, dass wir nicht erst auf eine Mutation warten müssen, um auf einen neuen Erreger zu reagieren, sondern dass die Grundausrüstung bereits vorhanden ist.
Sobald eine B-Zelle ihr passendes Antigen findet, passiert etwas Entscheidendes, das über die bloße VDJ-Rekombination hinausgeht: die Somatische Hypermutation. Man könnte sagen, die Grundausstattung wird für das bestehende Problem optimiert. Statt eines einfachen großen Löffel für alles, der prinzipiell seinen Dienst erfüllt, hat man nun Esslöffel, Suppenlöffel, Teelöffel, Kaffeelöffel, Eislöffel, Löffel mit Röhrchen…
Das naive, angeborene Repertoire des Endprodukts der VDJ-Rekombination ist somit schon mal generell in der Lage ist, eine potenziell unbegrenzte Anzahl fremder Antigene zu erkennen. Der Pool naiver B-Zellen allein kann bereits ein nahezu unbegrenztes Spektrum an Krankheitserregern abdecken. Dabei spielen auch die J Anteile der VDJ-Rekombination eine wichtige Rolle, die gerne übersehen wird.
Es gibt Berechnungen, dass die somatische Hypermutation nett, aber nicht unbedingt lebensnotwendig ist. Das Grundrepertoire würde auch reichen, die somatische Hypermutation ist das Risiko des Gewinns durch die Optimierung aber wert.
Man könnte Sagen, der generelle Schlüssel durch die VDJ-Rekombination passt auf jedes potentielle Schloss, ruckelt aber teilweise ein wenig. Die somatische Hypermutation optimiert die Passung des Schlüssels, damit man nicht ruckeln muss. Wäre nicht nötig, ist aber nett zu haben.
Impfstoffe erfinden keine neuen Antikörper
Eine Impfung ist im Grunde ein “Such- und Trainingsbefehl” für das bereits vorhandene, durch V(D)J-Rekombination entstandene Repertoire. Ohne die VDJ-Rekombination gäbe es keine einzige B-Zelle, die auf den Impfstoff reagieren könnte. Der Impfstoff fungiert als Köder. Er pickt sich aus den Milliarden zufälligen B-Zellen genau die wenigen heraus, deren Rezeptoren (durch Zufall) an den Impfstoff binden. Mit Impfstoff ist aber nicht nur das Antigen im Impfstoff gemeint, damit sind alle Bestandteile des Impfstoffes gemeint und die sind recht vielfältig.
Ein Impfstoff kann nur das potenzieren und optimieren, was die Genetik zuvor durch Zufall bereitgestellt hat. Wäre das menschliche Genom nicht in der Lage, über die VDJ-Rekombination eine B-Zelle gegen ein bestimmtes Protein zu generieren, wäre jede Impfung wirkungslos.
Impfen aktiviert gezielt Zellen, die bereits durch Zufall entstanden sind.
Die gezielte Aktivierung klingt erst mal gut.
Die Sache hat aber einen großen Haken, der dabei nicht bedacht wird.
Die Immunologische Erbsünde
Eine natürliche Infektion führt zu einer breiteren Antikörperantwort als eine Impfung, da das Immunsystem mit dem gesamten Erreger und nicht nur mit einzelnen Bestandteilen konfrontiert wird. Wissenschaftliche Vergleiche zeigen, dass eine natürliche Infektion ein breiteres Spektrum an B-Zell-Klonen aktiviert, da sie gegen alle Proteine eines Erregers gerichtet ist, während viele moderne Impfstoffe nur auf ein spezifisches Protein abzielen.
Das ist nicht nur schlecht für den geimpften Menschen, das hat Folgen für die Weltbevölkerung weil dies zur “Entstehung von Varianten führen, die dem Immunsystem entkommen und die Entwicklung von Impfstoffen gegen dieses neu auftretende Virus weiterhin erschweren werden.”
Die durch natürliche Infektion entstandenen B-Gedächtniszellen reifen über Monate hinweg kontinuierlich mutieren dabei, was zu Antikörpern mit größerer Potenz und Breite führt, anders als nach einer mRNA-Impfung.
Während eine Impfung einen kontrollierten Schutz gegen die gefährlichsten Teile eines Erregers aufbaut, lernt das Immunsystem bei einer natürlichen Infektion am gesamten Erreger und verfeinert seine Antikörper oft über einen längeren Zeitraum und gegen mehr Ziele.
Was bedeutet das für die Masernimpfung
Bereits vor jedem Kontakt mit dem Masernvirus besitzt der Körper durch die VDJ-Rekombination ein angeborenes Repertoire an T- und B-Zellen. Diese Zellen wurden im Knochenmark durch zufällige Neukombination von Gensegmenten erzeugt. Statistisch gesehen existieren bereits „Ur-Antikörper“, die Teile des Masernvirus (z. B. das Hämagglutinin-Protein) binden können.
Die Masernimpfung (Lebendimpfstoff) erzeugt keine neuen Antikörper. Sie fungiert als Selektionswerkzeug, das aus dem riesigen Pool der zufällig entstandenen naiven B-Zellen genau die wenigen herauspickt, die auf Masern passen. Ohne diese biologisch bereits vorhandenen Vorläufer-Zellen könnte die Impfung keine Reaktion auslösen.
Masernimpfungen haben nun ein ganz spezielles historisches Problem. Die heute verwendeten Masernimpfstoffe basieren fast ausnahmslos auf Virusisolaten aus den 1950er Jahren.
In den letzten 76 Jahren haben sich daher Masernvarianten entwickelt.
Die Masernimpfung bildet vor allem H-spezifische Antikörper.
Das muss sogar die google KI zugeben.
Die Mutationen in zirkulierenden Wildtypen können die Fähigkeit von impfinduzierten T-Zellen stören können, auf diese Viren zu reagieren.
“Vor allem aber konnten wir nachweisen, dass Mutationen die Fähigkeit der durch die Impfung induzierten CD4+-T-Zellen beeinträchtigten, auf zirkulierende Viren zu reagieren. Folglich können Mutationen in den Epitopregionen zirkulierender Viren die Wirksamkeit der durch die Impfung induzierten T-Zell-Immunität beeinträchtigen.”
Dennoch wird natürlich auch in dieser Publikation pro Impfung argumentiert und das Ergebnis der Immunflucht ist natürlich: Mehr impfen und öfter.
Aktuell gibt es keine offiziellen Daten, die eine Immunflucht des Masernvirus belegen würden. Wer auch immer das publiziert, kann sich anschließend wahrscheinlich von seiner Karriere verabschieden.
Lustig ist aber schon, dass der Schutz durch die Impfung sinkt, wenn kein Kontakt zu Wildviren erfolgt, daher muss man natürlich nachimpfen, während die Antikörper nach einer Infektion ein Leben lang ausreichen.
Was bedeutet das für die SARS-CoV-2 Injektionen?
Die Immunflucht ist bei Sars-CoV-2 massiv, daher steigt die Infektionswahrscheinlichkeit nach Impfung.
Vermutlich ist das auch der Grund, warum bei vielen Impfungen, die Infektionswahrscheinlichkeit für Geimpfte höher ist als für Ungeimpfte. Pertussis ist auch so ein Beispiel.
Beim Spike-Protein gibt es aber noch ein Problem, daher wurde das erste Paper zum Thema zensiert, obwohl es mittlerweile andere Paper gibt, die das auch indirekt belegen.
Die Geschichte des Papers und seiner Zensur habe ich hier archiviert:
Die Autoren behaupten, dass das Spike-Protein von SARS-CoV-2 kann die VDJ-Rekombination stört, indem es wichtige DNA-Reparaturmechanismen im Zellkern behindert. Ein Teil der Spike-Proteine gelangt während einer Infektion in den Zellkern der Wirtszelle. Dort stört es die Rekrutierung von Schlüsselproteinen der DNA-Reparatur. Da die VDJ-Rekombination auf das gezielte Schneiden und präzise Wiederverknüpfen von DNA-Strängen angewiesen ist (ähnlich einer DNA-Reparatur), führt die Blockade dieser Reparaturproteine zu einer gestörten Bildung funktioneller Immunrezeptoren.
Das Paper müsste repliziert werden, aber wer wird sich trauen, so etwas zu veröffentlichen, wenn man nicht gerade kurz vor der Emeritur ist oder die Karriere ohnehin beenden wollte.
Unterstützungsmöglichkeiten:
Bücherwunschzettel: https://www.amazon.de/registries/gl/owner-view/30LG3DJ4ET90L?ref_=list_d_gl_lfu_nav
Andere Unterstützungsmöglichkeiten für Holgers und meine Forschung:
Konto für Unterstützung für das Projekt Scan 2000
Dr. Merse DE34 4305 0001 0302 7851 75 Sparkasse Bochum
Horst Reissner: IBAN DE51 4401 0046 0406 4514 67
Dr. S. Stebel: https://ko-fi.com/einmalmitprofisarbeiten
Murphy K, Weaver C. Die Entstehung von Antigenrezeptoren in Lymphocyten. Janeway Immunologie. 2018 Apr 23:221–71. German. doi: 10.1007/978-3-662-56004-4_5. PMCID: PMC7844867. https://pmc.ncbi.nlm.nih.gov/articles/PMC7844867/
Murphy K, Weaver C. Die Entstehung von Antigenrezeptoren in Lymphocyten. Janeway Immunologie. 2018 Apr 23:221–71. German. doi: 10.1007/978-3-662-56004-4_5. PMCID: PMC7844867. https://pmc.ncbi.nlm.nih.gov/articles/PMC7844867/
Murphy K, Weaver C. Die Entstehung von Antigenrezeptoren in Lymphocyten. Janeway Immunologie. 2018 Apr 23:221–71. German. doi: 10.1007/978-3-662-56004-4_5. PMCID: PMC7844867. https://pmc.ncbi.nlm.nih.gov/articles/PMC7844867/
Altmeyer, M. P. (2024, August 20). Somatische hypermutation. Altmeyers Enzyklopädie – Fachbereich Innere Medizin. https://www.altmeyers.org/de/innere-medizin/somatische-hypermutation-155379
IJspeert H, Wentink M, van Zessen D, Driessen GJ, Dalm VA, van Hagen MP, Pico-Knijnenburg I, Simons EJ, van Dongen JJ, Stubbs AP, van der Burg M. Strategies for B-cell receptor repertoire analysis in primary immunodeficiencies: from severe combined immunodeficiency to common variable immunodeficiency. Front Immunol. 2015 Apr 8;6:157. doi: 10.3389/fimmu.2015.00157. PMID: 25904919; PMCID: PMC4389565. https://pmc.ncbi.nlm.nih.gov/articles/PMC4389565/
Tangye SG, Nguyen T, Deenick EK, Bryant VL, Ma CS. Inborn errors of human B cell development, differentiation, and function. J Exp Med. 2023 Jul 3;220(7):e20221105. doi: 10.1084/jem.20221105. Epub 2023 Jun 5. PMID: 37273190; PMCID: PMC10242086. https://pmc.ncbi.nlm.nih.gov/articles/PMC10242086/
Chi X, Li Y, Qiu X. V(D)J recombination, somatic hypermutation and class switch recombination of immunoglobulins: mechanism and regulation. Immunology. 2020 Jul;160(3):233-247. doi: 10.1111/imm.13176. Epub 2020 Feb 27. PMID: 32031242; PMCID: PMC7341547. https://pubmed.ncbi.nlm.nih.gov/32031242/
Elhanati Y, Sethna Z, Marcou Q, Callan CG Jr, Mora T, Walczak AM. Inferring processes underlying B-cell repertoire diversity. Philos Trans R Soc Lond B Biol Sci. 2015 Sep 5;370(1676):20140243. doi: 10.1098/rstb.2014.0243. PMID: 26194757; PMCID: PMC4528420. https://pubmed.ncbi.nlm.nih.gov/26194757/
Ramsden DA, Weed BD, Reddy YV. V(D)J recombination: Born to be wild. Semin Cancer Biol. 2010 Aug;20(4):254-60. doi: 10.1016/j.semcancer.2010.06.002. Epub 2010 Jul 1. PMID: 20600921; PMCID: PMC2942997. https://pubmed.ncbi.nlm.nih.gov/20600921/
Havenar-Daughton C, Abbott RK, Schief WR, Crotty S. When designing vaccines, consider the starting material: the human B cell repertoire. Curr Opin Immunol. 2018 Aug;53:209-216. doi: 10.1016/j.coi.2018.08.002. Epub 2018 Sep 3. PMID: 30190230; PMCID: PMC6148213. https://pmc.ncbi.nlm.nih.gov/articles/PMC6148213/
Slabodkin A, Chernigovskaya M, Mikocziova I, Akbar R, Scheffer L, Pavlović M, Bashour H, Snapkov I, Mehta BB, Weber CR, Gutierrez-Marcos J, Sollid LM, Haff IH, Sandve GK, Robert PA, Greiff V. Individualized VDJ recombination predisposes the available Ig sequence space. Genome Res. 2021 Dec;31(12):2209-2224. doi: 10.1101/gr.275373.121. Epub 2021 Nov 23. PMID: 34815307; PMCID: PMC8647828. https://pmc.ncbi.nlm.nih.gov/articles/PMC8647828/
Laserson U, Vigneault F, Gadala-Maria D, Yaari G, Uduman M, Vander Heiden JA, Kelton W, Taek Jung S, Liu Y, Laserson J, Chari R, Lee JH, Bachelet I, Hickey B, Lieberman-Aiden E, Hanczaruk B, Simen BB, Egholm M, Koller D, Georgiou G, Kleinstein SH, Church GM. High-resolution antibody dynamics of vaccine-induced immune responses. Proc Natl Acad Sci U S A. 2014 Apr 1;111(13):4928-33. doi: 10.1073/pnas.1323862111. Epub 2014 Mar 17. PMID: 24639495; PMCID: PMC3977259. https://pmc.ncbi.nlm.nih.gov/articles/PMC3977259/
Khavrutskii IV, Chaudhury S, Stronsky SM, Lee DW, Benko JG, Wallqvist A, Bavari S, Cooper CL. Quantitative Analysis of Repertoire-Scale Immunoglobulin Properties in Vaccine-Induced B-Cell Responses. Front Immunol. 2017 Aug 14;8:910. doi: 10.3389/fimmu.2017.00910. PMID: 28855898; PMCID: PMC5557726. https://pmc.ncbi.nlm.nih.gov/articles/PMC5557726/
Kotagiri P, Mescia F, Rae WM, Bergamaschi L, Tuong ZK, Turner L, Hunter K, Gerber PP, Hosmillo M; Cambridge Institute of Therapeutic Immunology and Infectious Disease-National Institute of Health Research (CITIID-NIHR) COVID BioResource Collaboration; Hess C, Clatworthy MR, Goodfellow IG, Matheson NJ, McKinney EF, Wills MR, Gupta RK, Bradley JR, Bashford-Rogers RJM, Lyons PA, Smith KGC. B cell receptor repertoire kinetics after SARS-CoV-2 infection and vaccination. Cell Rep. 2022 Feb 15;38(7):110393. doi: 10.1016/j.celrep.2022.110393. Epub 2022 Jan 31. PMID: 35143756; PMCID: PMC8801326. https://pubmed.ncbi.nlm.nih.gov/35143756/
Kubo, M., & Miyauchi, K. (2020). Breadth of Antibody Responses during Influenza Virus Infection and Vaccination. Trends in Immunology, 41(5), 394–405. https://doi.org/10.1016/j.it.2020.03.005
Gärtner BC, Sester M. Diversity of antibody responses after influenza infection or vaccination-Needed or nice to have? Am J Transplant. 2021 Aug;21(8):2631-2632. doi: 10.1111/ajt.16554. Epub 2021 Mar 9. PMID: 33638930; PMCID: PMC8014159. https://pmc.ncbi.nlm.nih.gov/articles/PMC8014159/
Gärtner BC, Sester M. Diversity of antibody responses after influenza infection or vaccination-Needed or nice to have? Am J Transplant. 2021 Aug;21(8):2631-2632. doi: 10.1111/ajt.16554. Epub 2021 Mar 9. PMID: 33638930; PMCID: PMC8014159. https://pmc.ncbi.nlm.nih.gov/articles/PMC8014159/
Cho, A., Muecksch, F., Schaefer-Babajew, D., Wang, Z., Finkin, S., Gaebler, C., Ramos, V., Cipolla, M., Mendoza, P., Agudelo, M., Bednarski, E., DaSilva, J., Shimeliovich, I., Dizon, J., Daga, M., Millard, K. G., Turroja, M., Schmidt, F., Zhang, F., . . . Nussenzweig, M. C. (2021). Anti-SARS-CoV-2 receptor-binding domain antibody evolution after mRNA vaccination. Nature, 600(7889), 517–522. https://doi.org/10.1038/s41586-021-04060-7
He B, Liu S, Xu M, Hu Y, Lv K, Wang Y, Ma Y, Zhai Y, Yue X, Liu L, Lu H, Zhou S, Li P, Mai G, Huang X, Li C, Chen S, Ye S, Zhao P, Yang Y, Li X, Jie Y, Shi M, Yang J, Shu Y, Chen YQ. Comparative global B cell receptor repertoire difference induced by SARS-CoV-2 infection or vaccination via single-cell V(D)J sequencing. Emerg Microbes Infect. 2022 Dec;11(1):2007-2020. doi: 10.1080/22221751.2022.2105261. PMID: 35899581; PMCID: PMC9377262. https://pmc.ncbi.nlm.nih.gov/articles/PMC9377262/
History of measles vaccination. (n.d.). https://www.who.int/news-room/spotlight/history-of-vaccination/history-of-measles-vaccination
Muñoz-Alía MÁ, Muller CP, Russell SJ. Antigenic Drift Defines a New D4 Subgenotype of Measles Virus. J Virol. 2017 May 12;91(11):e00209-17. doi: 10.1128/JVI.00209-17. PMID: 28356529; PMCID: PMC5432853. https://pmc.ncbi.nlm.nih.gov/articles/PMC5432853/
de Swart RL, Yüksel S, Osterhaus AD. Relative contributions of measles virus hemagglutinin- and fusion protein-specific serum antibodies to virus neutralization. J Virol. 2005 Sep;79(17):11547-51. doi: 10.1128/JVI.79.17.11547-11551.2005. PMID: 16103210; PMCID: PMC1193617. https://pmc.ncbi.nlm.nih.gov/articles/PMC1193617/
Tahara M, Ito Y, Brindley MA, Ma X, He J, Xu S, Fukuhara H, Sakai K, Komase K, Rota PA, Plemper RK, Maenaka K, Takeda M. Functional and structural characterization of neutralizing epitopes of measles virus hemagglutinin protein. J Virol. 2013 Jan;87(1):666-75. doi: 10.1128/JVI.02033-12. Epub 2012 Oct 31. PMID: 23115278; PMCID: PMC3536376. https://pmc.ncbi.nlm.nih.gov/articles/PMC3536376/
Zemella, A., Beer, K., Ramm, F., Wenzel, D., Düx, A., Merkel, K., Calvignac-Spencer, S., Stern, D., Dorner, M. B., Dorner, B. G., Widulin, N., Schnalke, T., Walter, C., Wolbert, A., Schmid, B. G., Mankertz, A., & Santibanez, S. (2024). Vaccine-induced neutralizing antibodies bind to the H protein of a historical measles virus. International Journal of Medical Microbiology, 314, 151607. https://doi.org/10.1016/j.ijmm.2024.151607
Emmelot ME, Bodewes R, Maissan C, Vos M, de Swart RL, van Els CACM, Kaaijk P. Impact of genotypic variability of measles virus T-cell epitopes on vaccine-induced T-cell immunity. NPJ Vaccines. 2025 Feb 20;10(1):36. doi: 10.1038/s41541-025-01088-y. PMID: 39979288; PMCID: PMC11842548. https://pmc.ncbi.nlm.nih.gov/articles/PMC11842548/
Bianchi FP, Mascipinto S, Stefanizzi P, De Nitto S, Germinario C, Tafuri S. Long-term immunogenicity after measles vaccine vs. wild infection: an Italian retrospective cohort study. Hum Vaccin Immunother. 2021 Jul 3;17(7):2078-2084. doi: 10.1080/21645515.2020.1871296. Epub 2021 Jan 27. PMID: 33502929; PMCID: PMC8189124. https://pmc.ncbi.nlm.nih.gov/articles/PMC8189124/
Shrestha NK, Burke PC, Nowacki AS, Simon JF, Hagen A, Gordon SM. Effectiveness of the Coronavirus Disease 2019 Bivalent Vaccine. Open Forum Infect Dis. 2023 Apr 19;10(6):ofad209. doi: 10.1093/ofid/ofad209. PMID: 37274183; PMCID: PMC10234376. https://pubmed.ncbi.nlm.nih.gov/37274183/
James D Cherry, The 112-Year Odyssey of Pertussis and Pertussis Vaccines—Mistakes Made and Implications for the Future, Journal of the Pediatric Infectious Diseases Society, Volume 8, Issue 4, September 2019, Pages 334–341, https://doi.org/10.1093/jpids/piz005 https://academic.oup.com/jpids/article-abstract/8/4/334/5359449?login=false
Jiang H, Mei YF. SARS-CoV-2 Spike Impairs DNA Damage Repair and Inhibits V(D)J Recombination In Vitro. Viruses. 2021 Oct 13;13(10):2056. doi: 10.3390/v13102056. Retraction in: Viruses. 2022 May 10;14(5):1011. doi: 10.3390/v14051011. PMID: 34696485; PMCID: PMC8538446. https://pmc.ncbi.nlm.nih.gov/articles/PMC8538446/