Ich hatte vor einiger Zeit berichtet, dass Holger und ich Microclots haben, obwohl wir nicht “geimpft” sind.
Eines der Medikamente auf unserem Behandlungsplan war Heparin. Da es zum Binden des Spike-Proteins im Blut dient, haben Holger und ich es nicht genommen. Zwei Blutverdünner haben uns dann doch gereicht. Aspirin 100mg haben wir dauerhaft beibehalten. Clopidogrel haben wir nach 8 Wochen abgesetzt, als es aufgebraucht war. Unter doppelter Plättchenhemmung ist mein Blut dann auch wieder geronnen, anders als ohne Plättchenhemmung. So schlimm war das Verklumpen der Blutplättchen bei mir schon.
Wie funktioniert Heparin gegen das Spike-Protein?
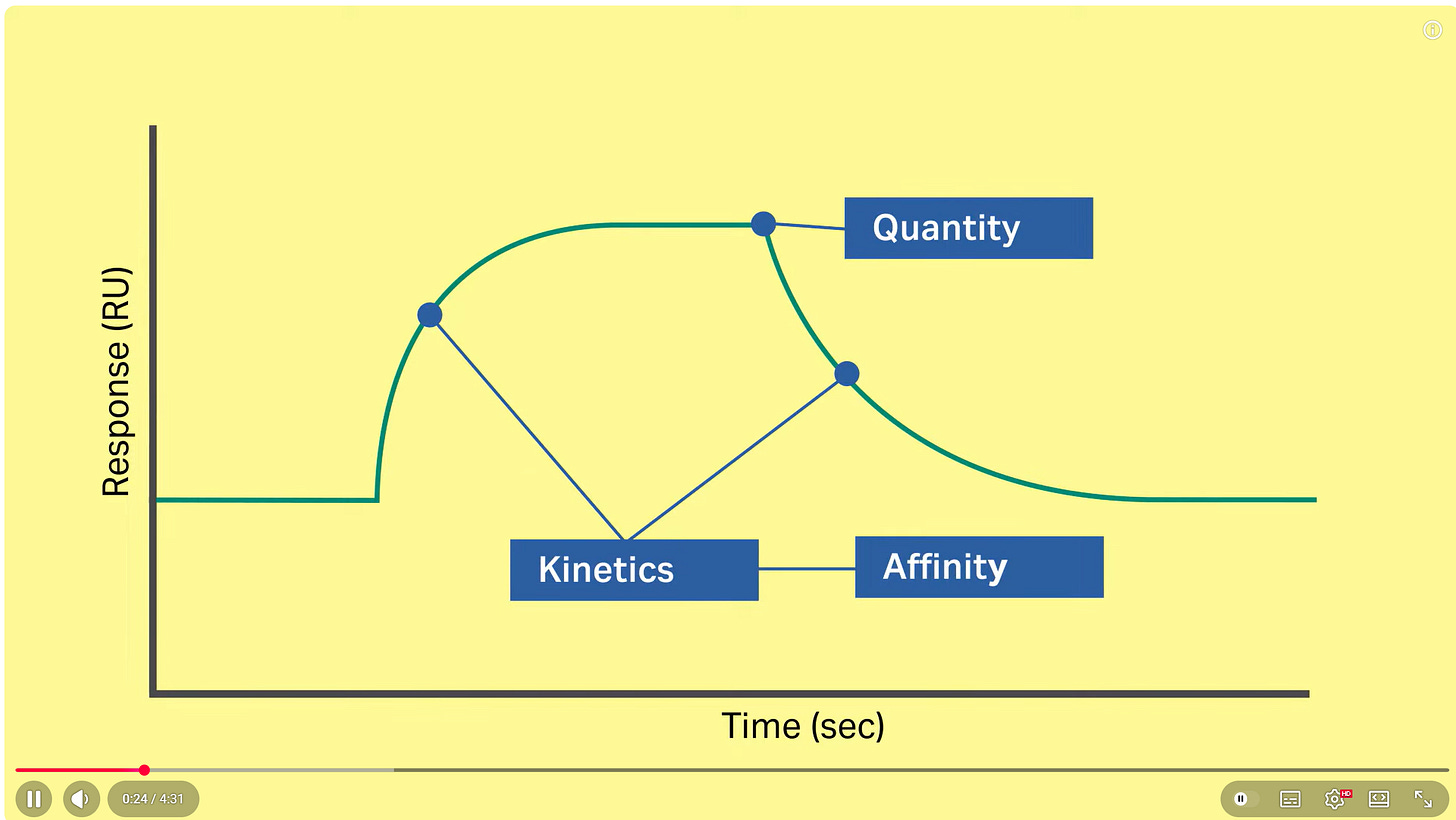
Schon im Juli 2020 konnte gezeigt werden, dass das sowohl das monomere als auch das trimere Spike-Protein an immobilisiertes Heparin bindet. Gemacht wurde das mit Biacore-Messung. Man koppelt das Heparin an den Chip und spült das Spike-Protein über das gebundene Heparin. Bindet das Spike-Protein, gibt es ein messbares Signal.
Was mit Heparin funktioniert, funktioniert übrigens auch mit ACE2 und anderen potentiellen Rezeptoren. Hat nur irgendwie keiner machen wollen, schon gar nicht die Hersteller der modRNA-Produkte.
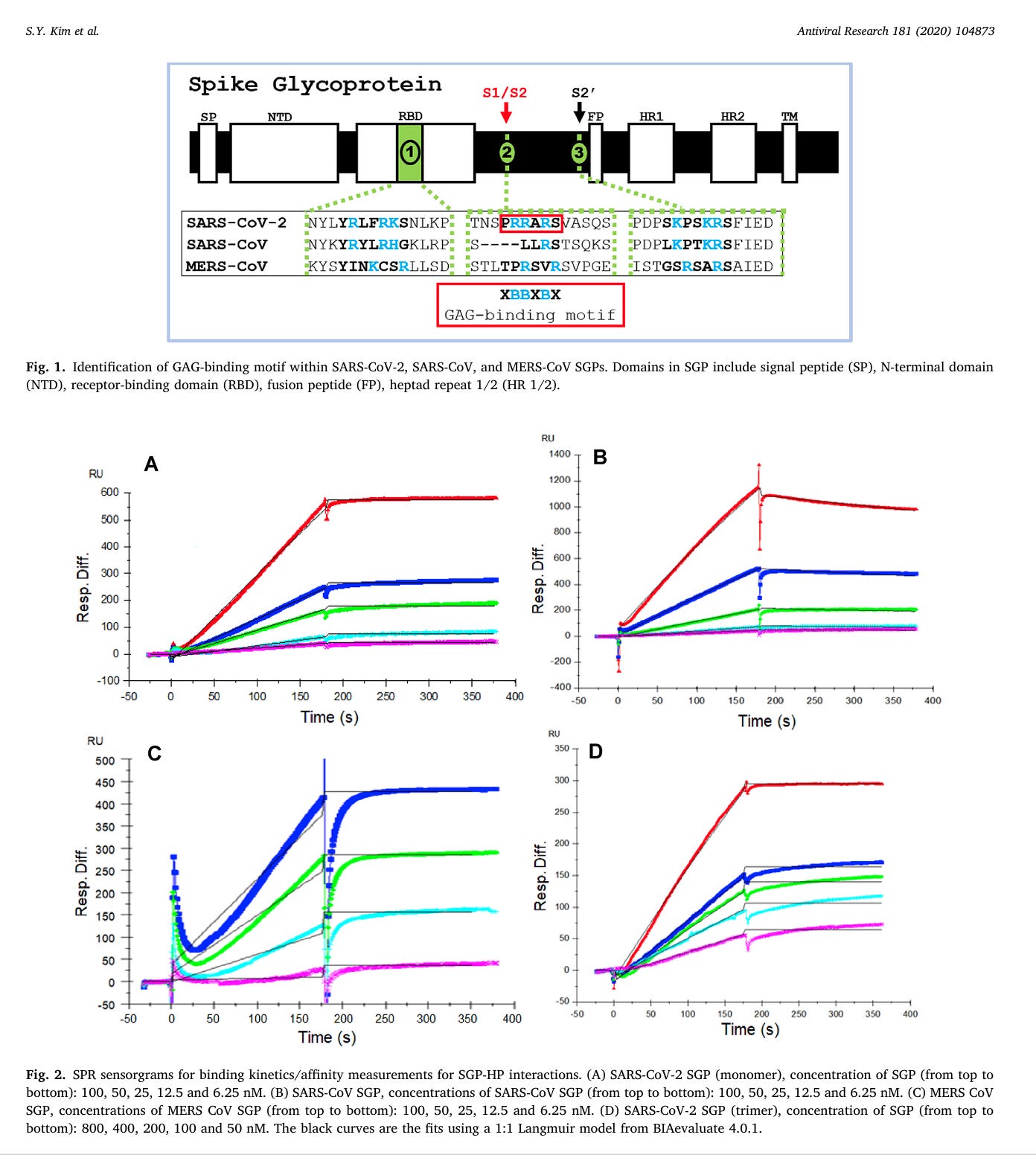
“SPR-Sensorgramme für Bindungskinetik- und Affinitätsmessungen bei SGP-HP-Wechselwirkungen. (A) SARS-CoV-2 SGP (Monomer), SGP-Konzentrationen (von oben nach unten): 100, 50, 25, 12,5 und 6,25 nM. (B) SARS-CoV SGP, Konzentrationen von SARS-CoV SGP (von oben nach unten): 100, 50, 25, 12,5 und 6,25 nM. (C) MERS-CoV-SGP, Konzentrationen von MERS-CoV-SGP (von oben nach unten): 100, 50, 25, 12,5 und 6,25 nM. (D) SARS-CoV-2 SGP (Trimer), Konzentration von SGP (von oben nach unten): 800, 400, 200, 100 und 50 nM. Die schwarzen Kurven sind die Anpassungen unter Verwendung eines 1:1-Langmuir-Modells aus BIAevaluate 4.0.1.”
Was man in diesen Kurven sieht, weil der hintere Teil der Kurve, wo das Signal wieder abnehmen sollte, fehlt: Das Spike-Protein kommt vom Heparin nicht mehr weg, es klebt und das war’s.
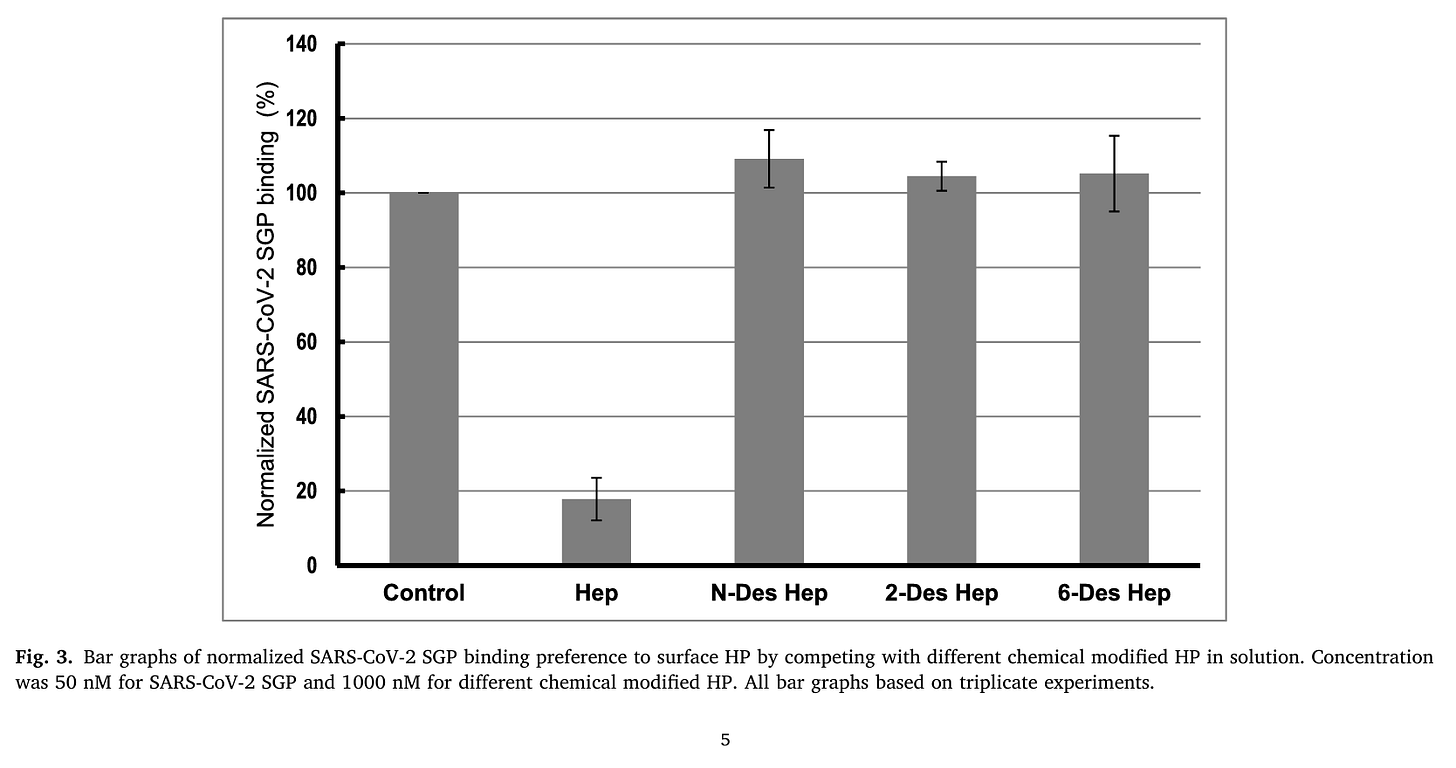
Man hat verschiedene Heparine (HP) ausporbiert: HP, 2-O-desulfatiertes HP und 6-O-desulfatiertes HP. Die waren aber nicht so gut. Das, was bindet sind wohl die Sulfatgruppen (SO4 2-) des Heparin.
Damit war eigentlich im Juli 2020 klar, wer Spike-Protein oder Virus im Blut hat, dem kann mit Heparin geholfen werden. Heparin bindet Virus und Spike, ist erprobt und billig und hat ein bekanntes Nebenwirkungsspektrum.
Damit wäre des mit dem “Impfen” erledigt gewesen.
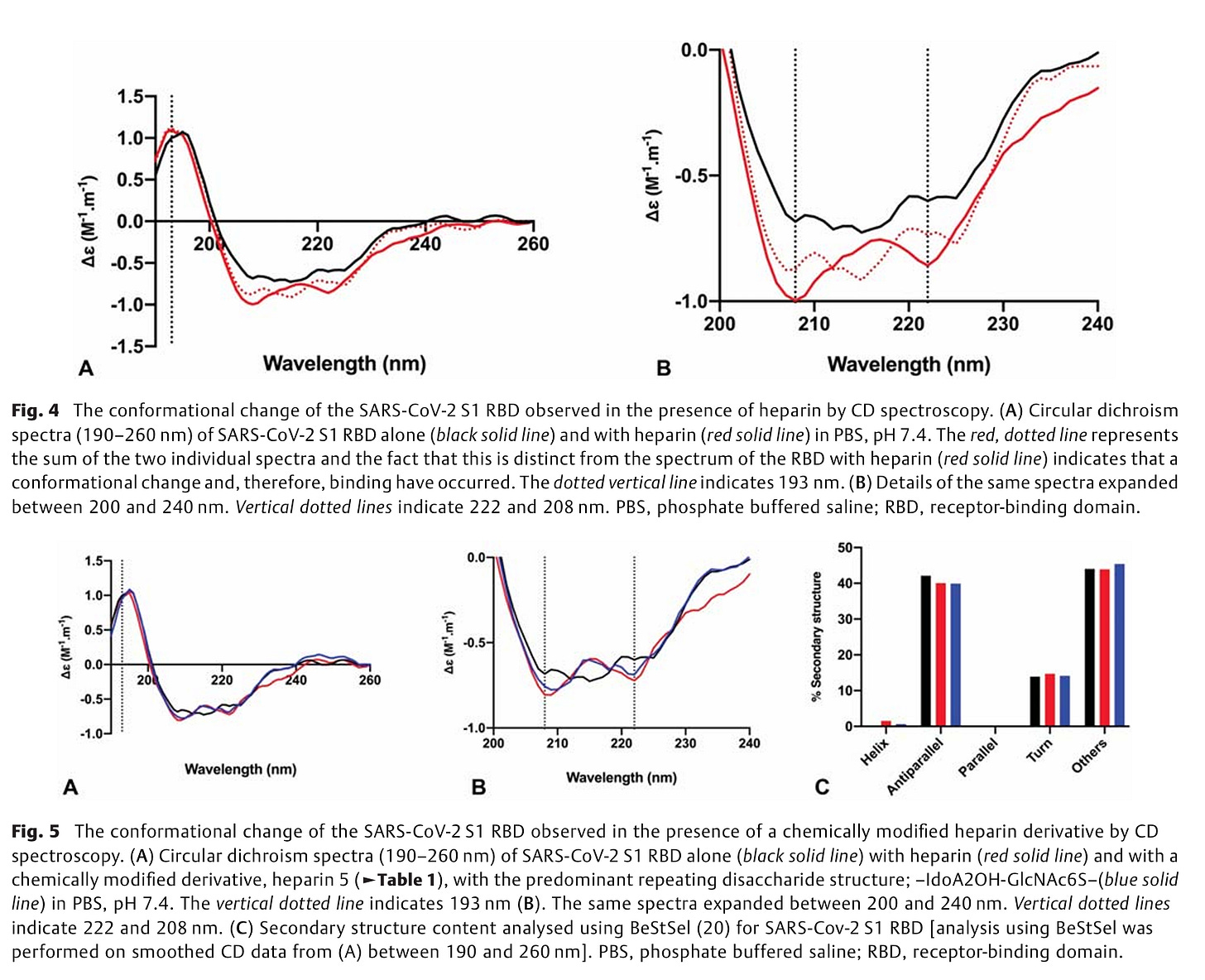
Im Dezember 2020 war klar, dass Herparin soger verhindert, dass das Virus in die Zelle eindringen kann. Im Dezember 2020 zeigte man dass Heparin an die S1-RBD bindet und deren Struktur verändert, was die Invasion der Zellen um bis zu 80 % hemmen kann.
S1-Untereinheit (Rezeptorbindung): Dieser Teil ist für das Erkennen und Binden an den ACE2-Rezeptor auf der menschlichen Zelle verantwortlich. Er enthält die Rezeptor-Bindungsdomäne (RBD) und ist der “äußere” Teil des Proteins. Der obere Teil des Brokkoli
S2-Untereinheit (Membranfusion): Dieser Teil verankert das Spike-Protein in der Virushülle und ist für die Fusion der Virusmembran mit der Zellmembran zuständig, was den Zelleintritt ermöglicht. Das Stamm des Brokkoli.
“Die Verfügbarkeit, die geringen Kosten und die klinische Qualität von Heparin, HS und deren Derivaten sowie die Tatsache, dass sie bei Patienten in der Intensivmedizin sicher verabreicht werden können, machen diese Polysaccharide zu attraktiven Kandidaten für die Erstlinienbehandlung von Viruserkrankungen wie COVID-19 und könnten möglicherweise zu einer prophylaktischen Kontrollstrategie beitragen.”
WARUM HAT MAN DAS NICHT GEMACHT?
Neben den bereits bekannten Biacore Messungen, machten diese Autoren auch Zirkulardichroismus-Spektroskopie (CD-Spektroskopie), konnten also zeigen, dass die Bindung des Spike-Proteins an Heparin, die Struktur des Spike-Proteins veränderten. Das Spike-Protein wurde also nicht nur gebunden, es wurde verbogen.
Mittlerweile weiß man, wie Heparin die Infektion blockiert und zwar durch direkte Konkurrenz um Co-Rezeptoren, allosterische Hemmung der ACE2-Bindung und Blockade der Furin-Spaltung.
Heparin verhindert die Spaltung durch Furin!!!
Eine eierlegende Wollmilchsau.
Heparin verhindert die Infektion der Zellen, bindet das (freie) Spike-Protein und fischt so, das Problem aus dem Blut. Dieses Paper ist leider hinter eine Bezahlschranke, es gibt aber die Grundlagen kostenlos, wie die grafische Zusammenfassung.
Und das funktioniert auch noch bei Omicron, anders als die “Impfung”.
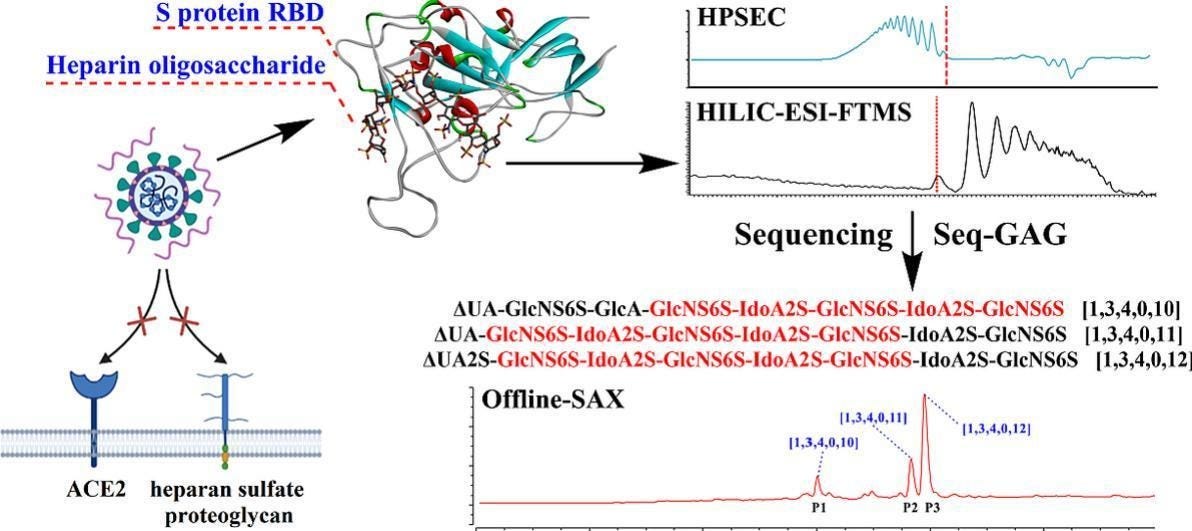
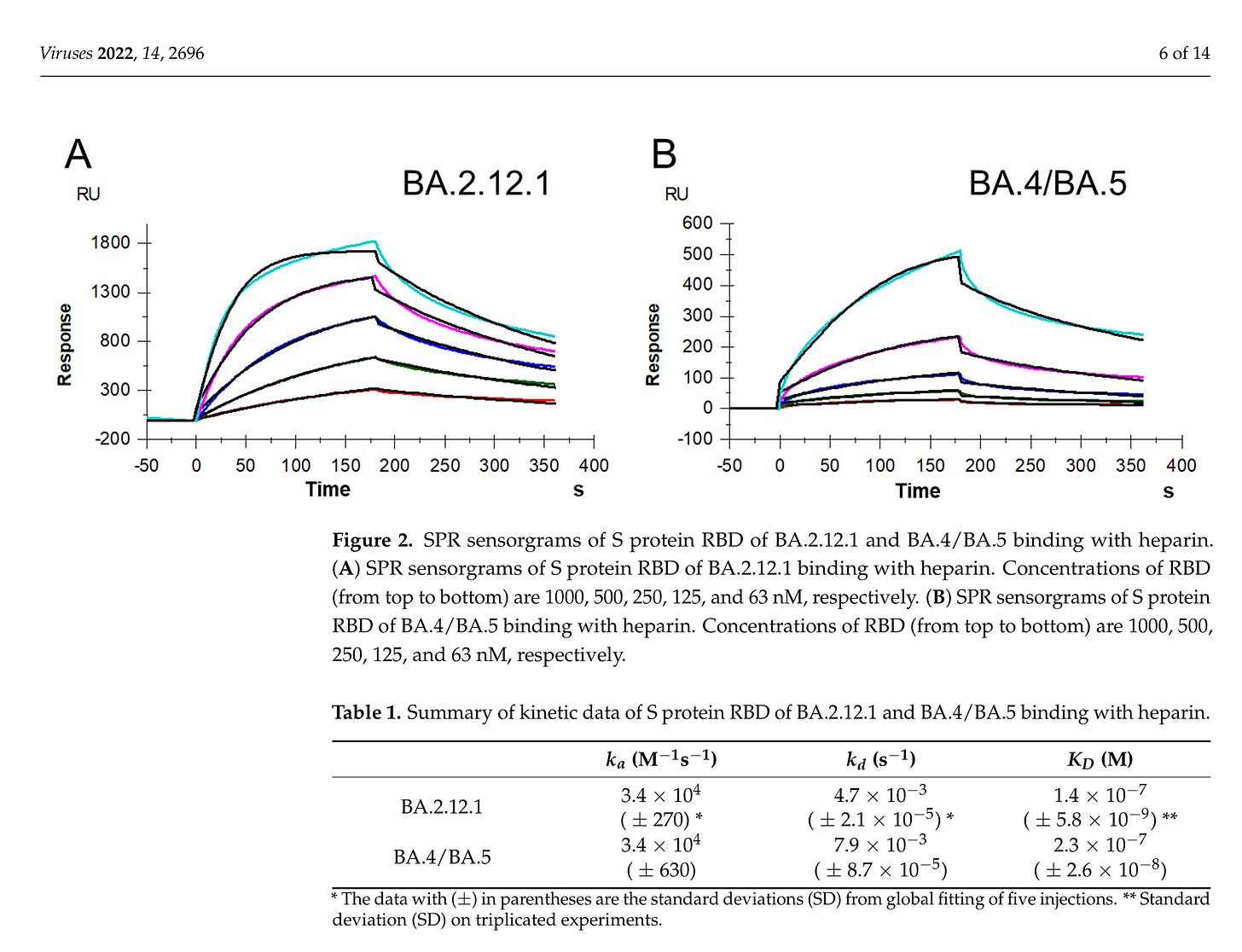
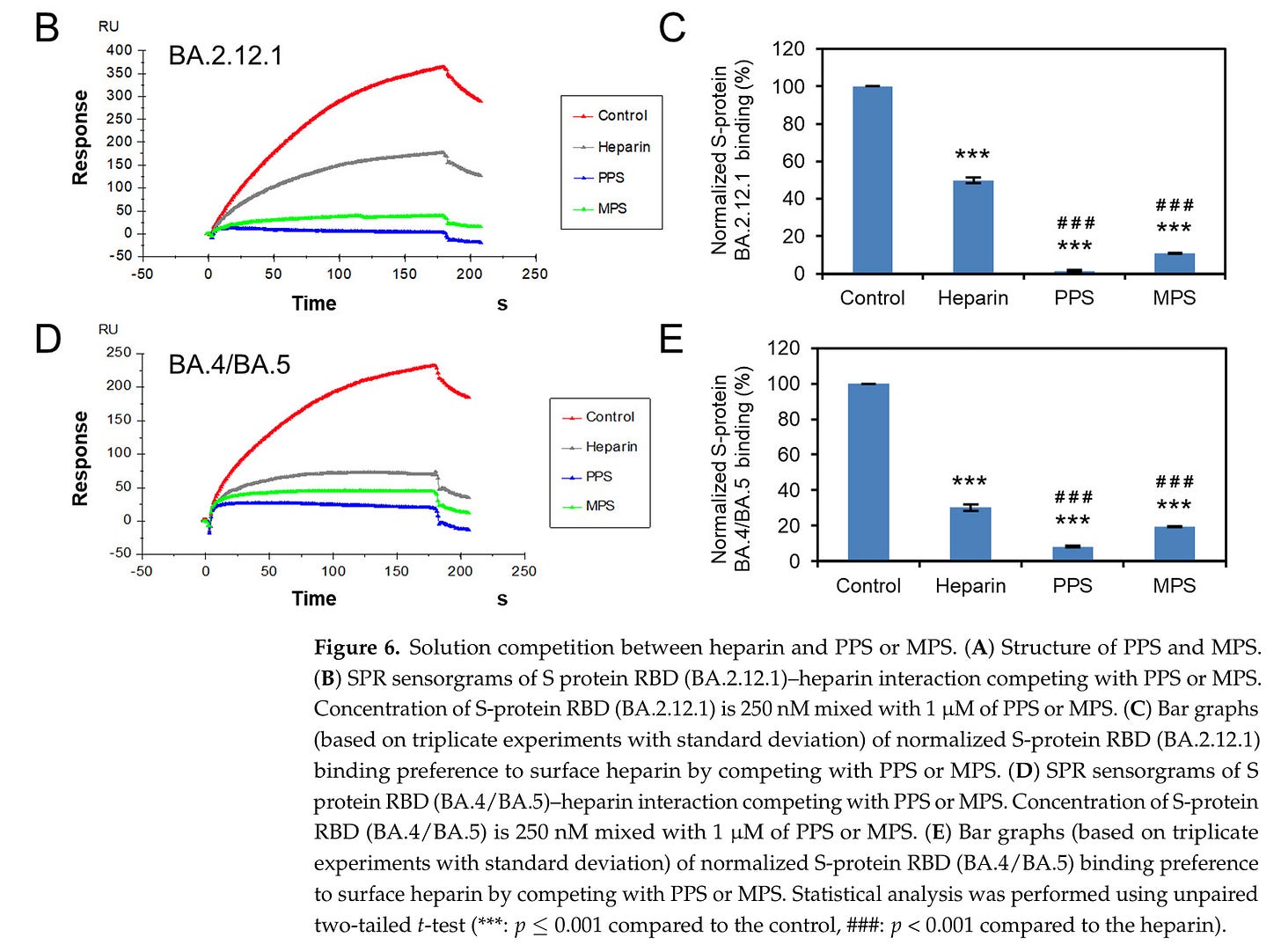
“Mutationen im RBD-Bereich des SARS-CoV-2-S-Proteins könnten die Bindung an HS/Heparin beeinflussen. Die SPR-Analyse ergab, dass die Bindungsaffinität (KD) von Omi-Cron BA.2.12.1 und BA.4/BA.5 im Nanomolarbereich lag, was etwas stärker war als bei der Wildtyp-Variante und mit der von Delta und Omicron B.1.1.529 vergleichbar war. “
“Es zeigte sich, dass ein Heparin-Oligosaccharid mit spezifischer Struktur eine hohe Affinität zum RBD des S-Proteins der Omicron-Sublinie BA.4/BA.5/BA.5.2 aufweist. Die Sequenz mit starker Bindungsfähigkeit im Oktasaccharid lautete [ΔUA2S-GlcNS6S-IdoA2S-GlcNS6S-IdoA2S-GlcNS6S -IdoA2S-GlcNS6S], mit einer Affinitätsenergie von −6,8 kcal/mol, wobei sich die Kernpentasaccharidsequenz GlcNS6S-IdoA2S-GlcNS6S-IdoA2S-GlcNS6S als gemeinsame Bindungseinheit herausstellte.”
Das wusste man aber alles schon im Dezember 2021: “Unsere Ergebnisse deuten darauf hin, dass Heparin die SARS-CoV-2-Infektion über drei Mechanismen hemmen kann: durch allosterische Hemmung der Bindung an den Rezeptor der Wirtszelle, durch direkte Konkurrenz um die Bindung an Heparansulfat-Proteoglykan-Korezeptoren des Wirts sowie durch Verhinderung der Spikeprotein-Spaltung durch Furin.”
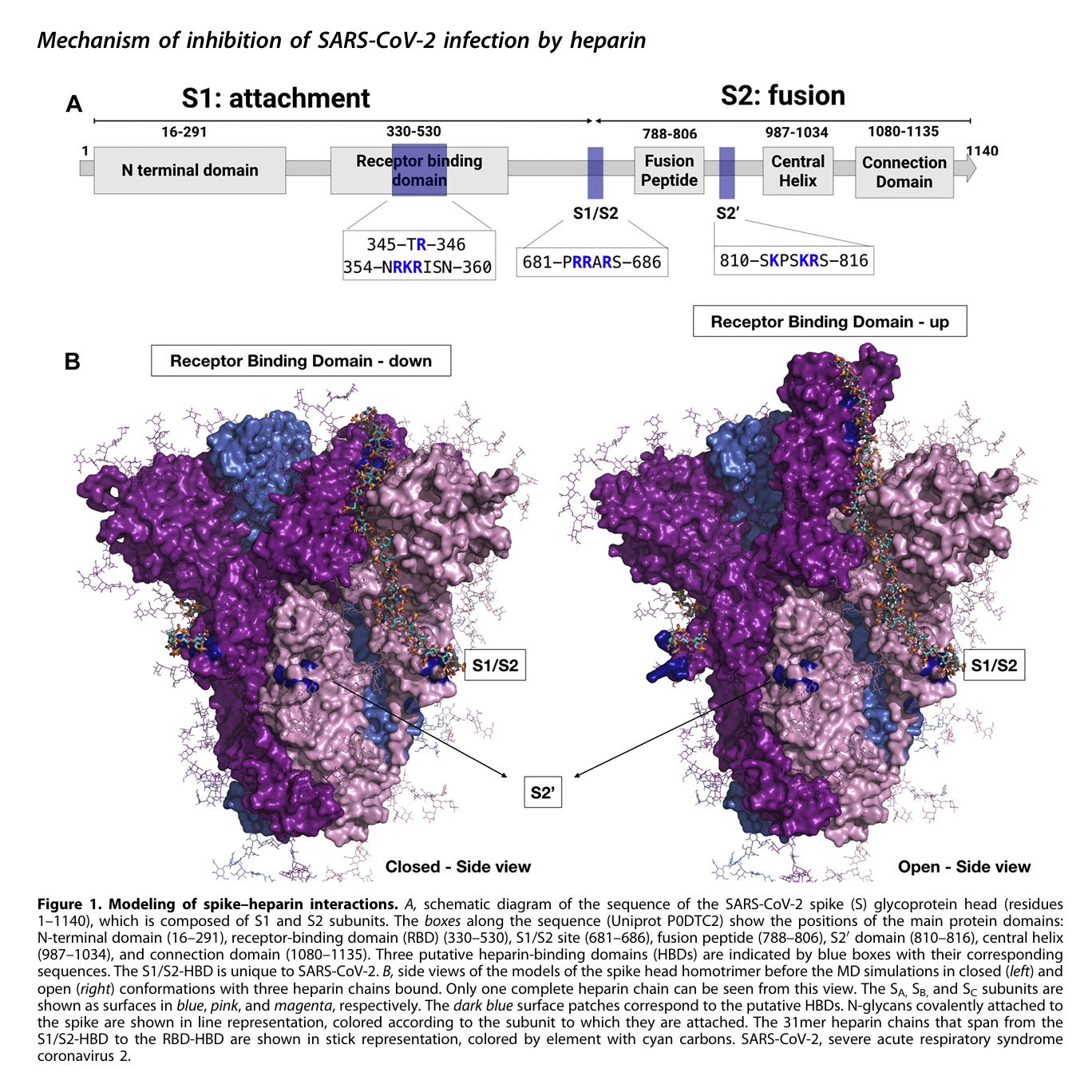
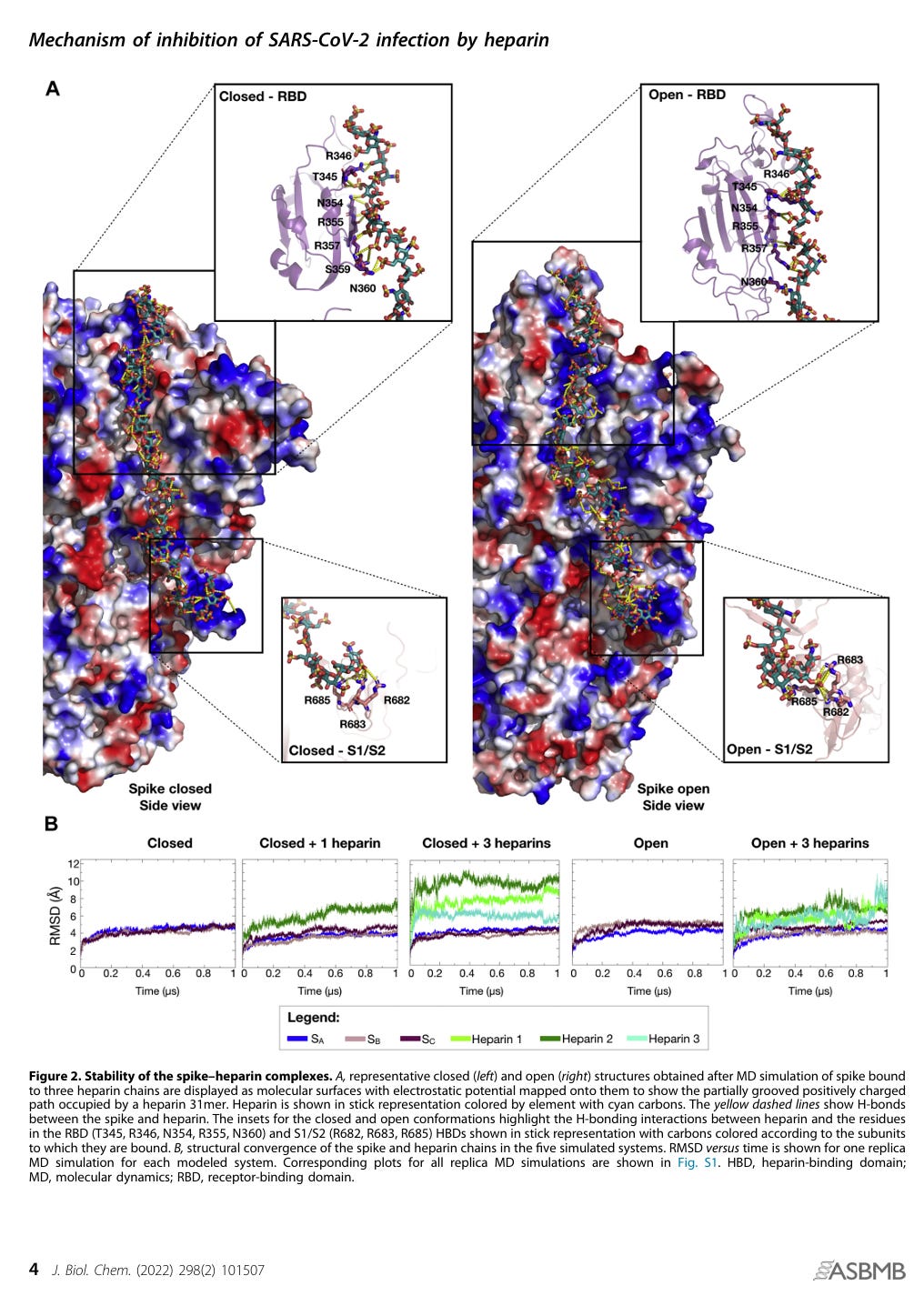
“Abbildung 2. Stabilität der Spike-Heparin-Komplexe. A: Repräsentative geschlossene (links) und offene (rechts) Strukturen, die nach einer MD-Simulation von Spike in Bindung an drei Heparin-Ketten erhalten wurden, sind als Moleküloberflächen dargestellt, auf die das elektrostatische Potential abgebildet wurde, um den teilweise gerillten, positiv geladenen Pfad zu zeigen, den ein Heparin-31-Mer einnimmt. Heparin ist in Stabdarstellung dargestellt, farblich nach Elementen geordnet, wobei Kohlenstoffe cyanfarben sind. Die gelben gestrichelten Linien zeigen Wasserstoffbrückenbindungen zwischen dem Spike und Heparin. Die Einschübe für die geschlossene und offene Konformation heben die Wasserstoffbrückenbindungs-Wechselwirkungen zwischen Heparin und den Resten im RBD (T345, R346, N354, R355, N360) und S1/S2 (R682, R683, R685) HBDs, dargestellt in Stabdarstellung, wobei die Kohlenstoffe entsprechend den Untereinheiten, an die sie gebunden sind, eingefärbt sind. B, strukturelle Konvergenz der Spike- und Heparin-Ketten in den fünf simulierten Systemen. Für jedes modellierte System wird die RMSD über die Zeit für eine Replik-MD-Simulation dargestellt. Entsprechende Diagramme für alle Replik-MD-Simulationen sind in Abb. S1 dargestellt. HBD, Heparin-Bindungsdomäne; MD, Molekulardynamik; RBD, Rezeptor-Bindungsdomäne”
Ich bin kein Freund von Simmulationen, aber die Simmulationen erklären in diesem Fall bekannte, echte Messwerte und sind somit “nur” Erklärung für etwas, das real messbar ist. Ob die Erklärung dabei komplett richtig ist, ist somit irrelevant.
Trotz all dieser Messwerte und Belege für Heparin als einfaches, billiges Mittel, gegen Sars-Cov2 wollte man lieber eine allgemeine Impfpflicht.
Heparin als Möglichkeit Spike-Protein aus dem Blut zu entfernen?
“Es wurde festgestellt, dass Heparansulfat (HS)/Heparin, ein Schlüsselfaktor im Gerinnungsprozess, mit hoher Affinität an das SARS-CoV-2-S-Protein bindet. Wir haben hier festgestellt, dass das S-Protein die Bindung von Antithrombin und Heparin-Cofaktor II an Heparin/HS kompetitiv hemmen kann, was zu einem abnormalen Anstieg der Thrombinaktivität führt. Das SARS-CoV-2-S-Protein kann in einer Konzentration (~10 μg/ml), die der Viruslast bei kritisch kranken Patienten entspricht, im Zebrafischmodell direkt Blutgerinnung und Thrombosen verursachen. Darüber hinaus kann exogenes Heparin/HS die durch das S-Protein verursachte Gerinnung signifikant reduzieren, was auf einen potenziellen neuen Ansatz zur Aufklärung der Ätiologie des Virus hinweist und eine grundlegende Unterstützung für die Antikoagulanzientherapie insbesondere bei kritisch erkrankten COVID-19-Patienten bietet.”
Das Spike-Protein lässt also bei Zebrafisch das Blut gerinnen und daher lässt man den Menschen dieses Protein durch eine Injektion längerfristig selbst produzieren?
Wie auch immer, Heparin scheint ein probates Mittel zum Entfernen des Spike-Proteins aus dem Blut zu sein.
Heparin Nasenspray?
Im November 2020 kam man auf die Idee, Heparin als antivirales Nasenspray zu testen.
“Heparin bindet an das Spike-Protein von SARS-CoV-2 und kann das Eindringen und die Vermehrung des Virus in anfälligen menschlichen Zelllinien und Bronchialepithelzellen hemmen. Die Primärinfektion erfolgt überwiegend über das Nasenepithel, doch die nasale Zellbiologie von SARS-CoV-2 ist bislang nur unzureichend erforscht. Wir stellten die Hypothese auf, dass die prophylaktische intranasale Verabreichung von Heparin einen stammspezifischen Schutz für Haushaltskontakte oder Personen in Hochrisikoumgebungen vor einer SARS-CoV-2-Infektion bieten könnte. Daher untersuchten wir die Fähigkeit von Heparin, die SARS-CoV-2-Infektion und -Replikation in differenzierten menschlichen Nasenepithelzellen zu hemmen, und zeigten, dass eine längere Exposition gegenüber Heparin die Virusinfektion hemmt.”
Es gab dazu tatsächlich eine klinische Studie: Die INHERIT-Studie (Intranasale Heparinbehandlung zur Verringerung der Übertragung unter Haushaltskontakten von COVID-19-positiven Erwachsenen und Kindern), die in in Australien durchgeführt wurde (NCT05204550).
In der INHERIT-Studie wurde Heparin als Nasenspray eingesetzt, um die Bindung des SARS-CoV-2-Virus an die Nasenschleimhaut zu verhindern. Die Lösung enthielt 5.000 Internationale Einheiten (IE) Heparin pro Milliliter in Kochsalzlösung. Pro Sprühstoß wurden 140 µl eingesetzt. Pro Anwendung erfolgten zwei Sprühstöße in jedes Nasenloch. Dies entspricht einer Dosis von 1.400 IE pro Nasenloch (insgesamt 2.800 IE pro Anwendung). Die Anwendung fand dreimal täglich statt.
Bei der nasalen Anwendung wird das Heparin aufgrund seiner Molekülgröße nicht in den Blutkreislauf aufgenommen. Es wirkt rein lokal in der Nase, indem es das Spike-Protein des Virus „maskiert“ und so den Eintritt in die menschlichen Zellen blockiert.
Das schreit nach einem Selbstversuch meinerseits, ob das auch bei Shedding hilft. Wie bereits erwähnt, haben Holger und ich uns entschieden das Heparin nicht zu spritzen und nur die zwei Plättchenhemmer zu nehmen. ABER, das Heparin liegt noch herum und ich habe mich schon gefragt, was ich jetzt damit anfangen soll.
C1V1 = C2V2
Ich habe
0,8 ml = C1
8000 IE = V1
ich will
5000 IE = C2
8000 IE*0,8 ml = 5000 IE * V2
V2 = (8000 * 0,8ml)/5000 (IE kürzt sich raus) = 1,28 ml Endvolumen.
1,28-0,8= 0,38 ml hinzufügen.
Das ist ohne richtige Pipetten nervig.
Ich werde mir einfach Kochsalznasenspray holen und eine Spritze Heparin darin verdünnen. Das ist dünner als das getestete Medikament. So kann ich mich langsam in den Konzentrationen hochtasten und berichten ob es meine Shedding Symptome reduziert.
Unterstützungsmöglichkeiten:
Bücherwunschzettel: https://www.amazon.de/registries/gl/owner-view/30LG3DJ4ET90L?ref_=list_d_gl_lfu_nav
Andere Unterstützungsmöglichkeiten für Holgers und meine Forschung:
Konto für Unterstützung für das Projekt Scan 2000
Dr. Merse DE34 4305 0001 0302 7851 75 Sparkasse Bochum
Horst Reissner: IBAN DE51 4401 0046 0406 4514 67
Dr. S. Stebel: https://ko-fi.com/einmalmitprofisarbeiten
Kim SY, Jin W, Sood A, Montgomery DW, Grant OC, Fuster MM, Fu L, Dordick JS, Woods RJ, Zhang F, Linhardt RJ. Characterization of heparin and severe acute respiratory syndrome-related coronavirus 2 (SARS-CoV-2) spike glycoprotein binding interactions. Antiviral Res. 2020 Sep;181:104873. doi: 10.1016/j.antiviral.2020.104873. Epub 2020 Jul 10. PMID: 32653452; PMCID: PMC7347485. https://pubmed.ncbi.nlm.nih.gov/32653452/
Kim SY, Jin W, Sood A, Montgomery DW, Grant OC, Fuster MM, Fu L, Dordick JS, Woods RJ, Zhang F, Linhardt RJ. Characterization of heparin and severe acute respiratory syndrome-related coronavirus 2 (SARS-CoV-2) spike glycoprotein binding interactions. Antiviral Res. 2020 Sep;181:104873. doi: 10.1016/j.antiviral.2020.104873. Epub 2020 Jul 10. PMID: 32653452; PMCID: PMC7347485. https://pubmed.ncbi.nlm.nih.gov/32653452/
Mycroft-West CJ, Su D, Pagani I, Rudd TR, Elli S, Gandhi NS, Guimond SE, Miller GJ, Meneghetti MCZ, Nader HB, Li Y, Nunes QM, Procter P, Mancini N, Clementi M, Bisio A, Forsyth NR, Ferro V, Turnbull JE, Guerrini M, Fernig DG, Vicenzi E, Yates EA, Lima MA, Skidmore MA. Heparin Inhibits Cellular Invasion by SARS-CoV-2: Structural Dependence of the Interaction of the Spike S1 Receptor-Binding Domain with Heparin. Thromb Haemost. 2020 Dec;120(12):1700-1715. doi: 10.1055/s-0040-1721319. Epub 2020 Dec 23. PMID: 33368089; PMCID: PMC7869224. https://pubmed.ncbi.nlm.nih.gov/33368089/
Mycroft-West CJ, Su D, Pagani I, Rudd TR, Elli S, Gandhi NS, Guimond SE, Miller GJ, Meneghetti MCZ, Nader HB, Li Y, Nunes QM, Procter P, Mancini N, Clementi M, Bisio A, Forsyth NR, Ferro V, Turnbull JE, Guerrini M, Fernig DG, Vicenzi E, Yates EA, Lima MA, Skidmore MA. Heparin Inhibits Cellular Invasion by SARS-CoV-2: Structural Dependence of the Interaction of the Spike S1 Receptor-Binding Domain with Heparin. Thromb Haemost. 2020 Dec;120(12):1700-1715. doi: 10.1055/s-0040-1721319. Epub 2020 Dec 23. PMID: 33368089; PMCID: PMC7869224. https://pubmed.ncbi.nlm.nih.gov/33368089/
An Z, Bu C, Shi D, Chen Q, Zhang B, Wang Q, Jin L, Chi L. Structurally defined heparin octasaccharide domain for binding to SARS-CoV-2 Omicron BA.4/BA.5/BA.5.2 spike protein RBD. Int J Biol Macromol. 2024 Feb;259(Pt 1):129032. doi: 10.1016/j.ijbiomac.2023.129032. Epub 2023 Dec 28. PMID: 38159696. https://pubmed.ncbi.nlm.nih.gov/38159696/
Shi D, Bu C, He P, Song Y, Dordick JS, Linhardt RJ, Chi L, Zhang F. Structural Characteristics of Heparin Binding to SARS-CoV-2 Spike Protein RBD of Omicron Sub-Lineages BA.2.12.1, BA.4 and BA.5. Viruses. 2022 Dec 1;14(12):2696. doi: 10.3390/v14122696. PMID: 36560700; PMCID: PMC9788508. https://pubmed.ncbi.nlm.nih.gov/36560700/
Shi D, Bu C, He P, Song Y, Dordick JS, Linhardt RJ, Chi L, Zhang F. Structural Characteristics of Heparin Binding to SARS-CoV-2 Spike Protein RBD of Omicron Sub-Lineages BA.2.12.1, BA.4 and BA.5. Viruses. 2022 Dec 1;14(12):2696. doi: 10.3390/v14122696. PMID: 36560700; PMCID: PMC9788508. https://pubmed.ncbi.nlm.nih.gov/36560700/
An Z, Bu C, Shi D, Chen Q, Zhang B, Wang Q, Jin L, Chi L. Structurally defined heparin octasaccharide domain for binding to SARS-CoV-2 Omicron BA.4/BA.5/BA.5.2 spike protein RBD. Int J Biol Macromol. 2024 Feb;259(Pt 1):129032. doi: 10.1016/j.ijbiomac.2023.129032. Epub 2023 Dec 28. PMID: 38159696. https://pubmed.ncbi.nlm.nih.gov/38159696/
Paiardi G, Richter S, Oreste P, Urbinati C, Rusnati M, Wade RC. The binding of heparin to spike glycoprotein inhibits SARS-CoV-2 infection by three mechanisms. J Biol Chem. 2022 Feb;298(2):101507. doi: 10.1016/j.jbc.2021.101507. Epub 2021 Dec 18. PMID: 34929169; PMCID: PMC8683219. https://pubmed.ncbi.nlm.nih.gov/34929169/
Paiardi G, Richter S, Oreste P, Urbinati C, Rusnati M, Wade RC. The binding of heparin to spike glycoprotein inhibits SARS-CoV-2 infection by three mechanisms. J Biol Chem. 2022 Feb;298(2):101507. doi: 10.1016/j.jbc.2021.101507. Epub 2021 Dec 18. PMID: 34929169; PMCID: PMC8683219. https://pubmed.ncbi.nlm.nih.gov/34929169/
Zheng Y, Zhao J, Li J, Guo Z, Sheng J, Ye X, Jin G, Wang C, Chai W, Yan J, Liu D, Liang X. SARS-CoV-2 spike protein causes blood coagulation and thrombosis by competitive binding to heparan sulfate. Int J Biol Macromol. 2021 Dec 15;193(Pt B):1124-1129. doi: 10.1016/j.ijbiomac.2021.10.112. Epub 2021 Oct 29. PMID: 34743814; PMCID: PMC8553634. https://pubmed.ncbi.nlm.nih.gov/34743814/
Lee LYY, Suryadinata R, McCafferty C, Ignjatovic V, Purcell DFJ, Robinson P, Morton CJ, Parker MW, Anderson GP, Monagle P, Subbarao K, Neil JA. Heparin Inhibits SARS-CoV-2 Replication in Human Nasal Epithelial Cells. Viruses. 2022 Nov 24;14(12):2620. doi: 10.3390/v14122620. PMID: 36560624; PMCID: PMC9785945. https://pubmed.ncbi.nlm.nih.gov/36560624/
ClinicalTrials.gov. (n.d.-b). https://clinicaltrials.gov/study/NCT05204550