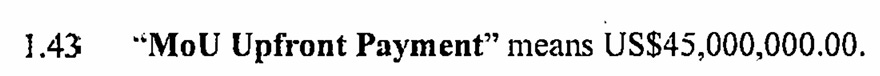Dieser Artikel ist der vierte Artikel zu den Schweizer “Impfstoff”-Verträgen
Bisher behandelt:
Pfizer:
Moderna:
Die Vorgeschichte zu den Verträgen und wie sie vor Gericht erstritten wurden findet sich in Teil 1A
Von Moderna liegen der Öffentlichkeit nun folgende Verträge vor:
Moderna Agreement 5.8.2020
Auch der Vertrag mit Moderna wurde unter anderem mit der Schweizer Armeeapotheke geschlossen.
Im Vorvertrag wurde schon abgesprochen, dass die Schweiz Bulk Ware kauft und selbst für das Abfüllen aufkommen muss. Die Kosten hierfür betragen 2 USD pro vial, so wie ich das verstehe. Könnte aber auch pro Dosis sein, so wirklich spezifiziert ist das im Vorwort, in welchem Worte definiert werden, noch nicht. 2 USD entsprachen am 5.08.2020 laut dem Währungsrechner Oanda, 1,83 CHF bzw. 1,70 EUR. Die umgerechneten im Artikel Preise beziehen sich daher alle auf den zu 5.8.2020 bei Oanda hinterlegten Kurs.
Man muss dazu wissen, Europa wurde aus der Schweiz beliefert. 2021 kamen wahrscheinlich alle Moderna Dosen von Lonza Visp, später kam ein Niederländischer Lonza Standort (Geleen) hinzu. Abgefüllt wurde in Spanien bei Laboratorios Farmacéuticos Rovi, S.A. und ab Mitte/Ende 2021 in Monts, Frankreich bei Recipharm damit sie als europäisches Produkt galten und so auch problemlos in der EU verkauft werden konnten, weil die Schweiz eben nicht EU ist.
So wurde auch Executive Order 13962 von Moderna umgangen, die den Export von COVID-”Impfstoffen” aus den USA verbot, so lange der Bedarf in USA nicht gedeckt war.
Das bedeutet aber auch, dass das EU Produkt, aufgrund seiner komplett eigenen Lieferkette, vor allem bei den Lipiden, wahrscheinlich nicht identisch zum US-Produkt ist und eigentlich wissenschaftlich immer parallel untersucht werden muss.
Die Schweiz machte eine Anzahlung von 41.208.030 CHF / 38.214.585 EUR
Einige Wortdefinitionen scheinen mir wichtig, wie:
„Angemessene Bemühungen“ bedeutet: (i) in Bezug auf den Käufer die angemessenen Anstrengungen und Ressourcen, die eine sorgfältige Person, die ein bestimmtes Ergebnis erzielen möchte, unter ähnlichen Umständen aufwenden würde oder voraussichtlich aufwenden müsste, um sicherzustellen, dass dieses Ergebnis erreicht wird; und (ii) in Bezug auf Moderna ein Maß an Anstrengungen und Ressourcen, das ein in einer vergleichbaren Lage befindliches biopharmazeutisches Unternehmen für ein ähnliches Produkt aufwenden würde, basierend auf den zu diesem Zeitpunkt herrschenden Bedingungen und unter Berücksichtigung von Fragen der Sicherheit und Wirksamkeit, des Produktprofils, der Rechtslage, des zu diesem Zeitpunkt bestehenden Wettbewerbsumfelds und der dringenden Nachfrage nach einem solchen Produkt sowie des voraussichtlichen Zeitpunkts des Markteintritts dieses Produkts, sowie das regulatorische Umfeld und den Status dieses Produkts und andere relevante wissenschaftliche, technische, kommerzielle und Compliance-Faktoren. Übersetzt mit DeepL.com (kostenlose Version)
(viii) die geltenden Rechtsvorschriften einzuhalten, einschließlich, soweit anwendbar, GCP, GDP, GLP und cGMP, in Bezug auf seine Rechte und Pflichten hinsichtlich des Produkts und seiner Tätigkeiten im Rahmen dieser Vereinbarung;
GCP – Good Clinical Practice (Gute klinische Praxis)
GDP – Good Distribution Practice (Gute Vertriebspraxis)
GLP – Good Laboratory Practice (Gute Laborpraxis)
cGMP – current Good Manufacturing Practice (aktuelle Gute Herstellungspraxis)
Das klingt zunächst gut, nur… sind für diese Produktklasse überhaupt bereits entsprechende Regelwerke erstellt worden? USP diskutiert nun schon in der dritten Runde, wie man modRNA-LNP Produkte überhaupt testet und auf was man achten muss. Die EU hat gerade mal einen guideline draft.
Ich habe mir den aktuellen Stand der Beratungen, wie man diese Produkte theoretisch prüfen müsste näher angeschaut.
Biologisch viele blinde Flecken ABER deutlich mehr und sinnvollere Untersuchungen, als gemacht wurden. Sind diese Qualitätskontrollen gesunder Menschenverstand und rückwirkend anwendbar oder ist das nun ein Fall von damals wusste man es nicht besser und kein Verstoß gegen cGMP?
Definition: Das „c“ steht für „current“ (aktuell) und betont, dass pharmazeutische Unternehmen die jeweils neuesten Technologien und Standards bei der Herstellung anwenden müssen.
Inhalt: Umfasst die Maßnahmen zur Qualitätssicherung bei der Produktion von Arzneimitteln und Wirkstoffen.
Ziel: Sicherstellung einer gleichbleibenden Qualität und Reinheit der Produkte, um Risiken für den Endverbraucher auszuschließen
Was war current? Massenspektrometrie für Lipide? Verhinderung von DNA-Rückständen?
Du verstehst das Problem, geneigter Leser?
Das current ist nicht exakt definiert.
Bei all den vielen Seiten an Definitionen ist cGMP nicht im Detail definiert und eher angelehnt an die gängige Praxis, schätze ich. Also keine schmutzigen Socken in die Behälter werfen oder Metallpartikel und Mücken.
Während der Vorvertrag noch fair war, dreht Moderna im eigentlichen Vertrag die Daumenschrauben an und wird direkter, was es von der Schweiz verlangt.
Der Käufer verpflichtet sich, Moderna von jeglichen rechtlichen und finanziellen Forderungen Dritter freizustellen, die aus der Nutzung, Lieferung oder Herstellung des Impfstoffprodukts resultieren. Zudem übernimmt der Käufer die Verantwortung für Kompensationszahlungen an Probanden bei klinischen Studien, die von Behörden angeordnet wurden.
VERPFLICHTUNGEN DES KÄUFERS. 4.1 Freistellung der Moderna-Parteien. Der Käufer stellt jede der Moderna-Parteien von jeglichen Verlusten, Verbindlichkeiten, Ansprüchen, Geldbußen, Schäden, Kosten und Aufwendungen jeglicher Art frei (einschließlich aller Zinsen, Strafen und Rechtskosten (berechnet auf der Grundlage einer vollständigen Entschädigung) sowie aller sonstigen professionellen Kosten und Aufwendungen und einschließlich aller Kosten für die Untersuchung und Verteidigung gegen tatsächliche oder drohende Forderungen. Anspruch, Klage oder Verfahren) („Verluste“ und jeweils ein „Verlust“):
(i) die einer solchen Moderna-Partei im Zusammenhang mit Ansprüchen, Klagen oder Verfahren jeglicher Art durch eine andere Person als den Käufer oder diese Moderna-Partei oder eines ihrer verbundenen Unternehmen (jeweils ein „freistellender Dritter“) im Zusammenhang mit, verursacht durch, sich ergebend aus, in Bezug auf oder resultierend aus der Herstellung, Prüfung, Entwicklung. Lieferung, Export, Import, Vertrieb, Verabreichung, Verkauf, Verkaufsangebot, Spende oder Verwendung des Produkts, das dem Käufer (oder dem Fürstentum Liechtenstein oder einem Spendenland, je nach Anwendbarkeit) im Rahmen dieser Vereinbarung geliefert wurde;
(ii) die einer solchen Moderna-Partei im Zusammenhang mit der Bereitstellung von klinischen Interventionen oder Entschädigungen nach dem Datum des Inkrafttretens an Teilnehmer an klinischen Studien für das Produkt im Gebiet (oder in Liechtenstein oder dem Land oder der Gerichtsbarkeit eines Spenderlandes, je nach Anwendbarkeit) entstehen oder von ihr getragen werden, die im Zusammenhang mit solchen klinischen Studien im Gebiet (oder in Liechtenstein oder dem Land oder der Gerichtsbarkeit eines Spenderlandes, je nach Anwendbarkeit) Ansprüche geltend machen oder Tod oder Personenschäden erleiden ; vorausgesetzt jedoch, dass diese klinischen Studien von der Zulassungsbehörde im Gebiet (oder der zuständigen staatlichen Behörde im Spenderland) angeordnet wurden.
Die Klausel legt fest, dass der Käufer (meist ein Staat wie Deutschland oder die Schweiz) Moderna vor diesen Ansprüchen schützen muss. Wenn also eine geimpfte Person Moderna auf Schadensersatz verklagt, muss der Staat:
Die Verteidigung von Moderna übernehmen oder bezahlen.
Sämtliche Kosten, Strafen und Entschädigungen übernehmen, die Moderna an diese „Dritten“ zahlen müsste.
Neu ist das nicht. Darüber gibt es schon peer reviewed wissenschaftliche Artikel aus dem Jahr 2022, was ein Beleg dafür ist, dass die Mainstreammedien sich jetzt künstlich und vor allem zu spät aufregen. Diese Klauseln sind seit JAHREN bekannt.
Staatsvereinnahmung durch Haftungsfreistellungsforderungen? Auswirkungen auf die Gerechtigkeit bei der weltweiten Verteilung von COVID-19-Impfstoffen: Die Ergebnisse deuten darauf hin, dass die Haftungsfreistellungsforderungen der COVID-19-Impfstoffhersteller sowohl im Rahmen bilateraler Abkommen als auch über die COVAX-Initiative in vielen Ländern mit niedrigem und mittlerem Einkommen (LMICs) zu einer Staatsvereinnahmung führen, in vielen Ländern mit hohem Einkommen (HICs) jedoch nicht. Diese Forderungen schränken die Möglichkeiten der LMICs ein, Impfstoffbeschaffungsverträge mit COVID-19-Impfstoffherstellern abzuschließen, und damit auch ihre Fähigkeit, Impfstoffe durch bilaterale Verhandlungen und durch Spenden aus anderen Ländern zu erhalten. Ebenso kann die Richtlinie der COVAX-Initiative, wonach alle teilnehmenden Länder den Impfstoffherstellern eine Haftungsfreistellung gewähren müssen, Regierungen daran hindern, COVAX-Beschaffungsverträge zu unterzeichnen; dies schränkt die Fähigkeit der COVAX-Initiative ein, ihr angestrebtes Ziel der Förderung einer globalen gerechten Verteilung von COVID-19-Impfstoffen zu erreichen. Diese Ergebnisse unterstreichen die Notwendigkeit, Machtungleichgewichte zwischen Regierungen und Pharmaunternehmen abzubauen und Alternativen zur Haftungsfreistellung zu finden, die weder die gerechte Verteilung von Notfallimpfstoffen noch die Bemühungen zur Beendigung der COVID-19-Pandemie behindern..
Immerhin, Moderna gibt der Schweiz die Wahl: Entweder führt Moderna die Verteidigung auf Kosten des Käufers (Staates), oder der Käufer übernimmt die Verteidigung unter Berücksichtigung von Modernas Interessen. In beiden Fällen trägt der Käufer die vollen Kosten und Verluste, während Moderna die Kontrolle über Vergleiche und die Verteidigungsstrategie behält.
Alles so, wie man das auch schon von BioNTech/Pfizer kennt.
Aber, der nächste Paragraph spezifiziert noch einmal, wie geschützt Moderna gerne sein möchte:
Extremer Schutz: Der Vertrag soll so ausgelegt werden, dass Moderna im Zweifel immer geschützt ist. Man nutzt den maximalen Spielraum, den das Schweizer Recht dafür hergibt.
Keine Geldgrenze: Es gibt keine finanzielle Obergrenze (kein “Cap”). Wenn Schäden in Milliardenhöhe entstehen, muss der Käufer (der Staat) diese komplett bezahlen.
Gilt für alles: Der Schutz gilt für jede einzelne Impfdosis, egal wann oder wie sie geliefert oder verwendet wurde.
Lange Dauer: Dieser Schutz gilt standardmäßig für 12 Jahre nach Vertragsabschluss.
Die “Verlängerung”: Wenn innerhalb dieser 12 Jahre ein rechtliches Problem (ein “Claim”) gemeldet wird, bleibt die Zahlungsverpflichtung des Staates so lange bestehen, bis dieser Fall komplett abgeschlossen ist – auch wenn das länger als 12 Jahre dauert.
Kurz gesagt: Der Staat unterschreibt hier einen “Blankoscheck” für fast alle denkbaren rechtlichen Kosten und Schäden, der mindestens 12 Jahre lang gültig bleibt.
Die einzige echte Einschränkung (Sektion 4.1, letzter Absatz) besagt in einfachen Worten:
Kein Schutz bei Absicht: Wenn Moderna (oder die verbundenen “Moderna Parties”) den Schaden mit Absicht herbeigeführt hat, muss der Staat sie nicht schützen.
Kein Schutz bei grobem Fehlverhalten: Wenn Moderna extrem rücksichtslos oder so nachlässig gehandelt hat, dass es weit über einen normalen Fehler hinausgeht (grobe Fahrlässigkeit), entfällt die Pflicht des Staates zur Kostenübernahme.
Nachweispflicht: Diese Einschränkung greift in der Regel nur dann, wenn ein Gericht oder eine offizielle Stelle dieses schwere Fehlverhalten eindeutig feststellt.
Der Staat zahlt für fast alles (Nebenwirkungen, Lieferfehler, unvorhersehbare Probleme), aber er zahlt nicht, wenn Moderna den Schaden absichtlich oder durch extreme Schluderei selbst provoziert hat.
Ich bin mir nicht sicher, ob es reicht, einen Übersichtsartikel von (ehemaligen) Moderna Mitarbeitern hinzuzuziehen, in welchen die Probleme, die Moderna bekannt waren, gelistet sind.
Letztendlich jedoch nichts Neues, was Moderna verlangt. Das entspricht nur dem US Prep Act. den es so im Rest der Welt nicht gibt. Man braut diesen US Prep. Act. in den Verträgen ein bzw. nach auf Vertragsniveau. Inwieweit das juristisch langfristig hält, wenn man gesellschaftlich zu dem Schluss kommt, dass es sich um ein Verbrechen gegen die Menschlichkeit handelt, sei mal dahin gestellt.
Diese Klausel ist eine sogenannte „Meistbegünstigungsklausel“ (Most Favoured Nations – MFN). Sie soll sicherstellen, dass Moderna niemals schlechter gestellt wird als andere Impfstoffhersteller (wie z. B. BioNTech oder AstraZeneca).
Diese Klausel hier geht einen Schritt weiter: Immunität. Das bedeutet, dass eine Klage gegen Moderna von vornherein gar nicht erst zugelassen wird.
Moderna sichert sich hier ab, dass sie von jeder zukünftigen gesetzlichen „Immunitäts-Welle“ profitieren. Wenn der Staat den Weg von der bloßen Kostenübernahme hin zu einem völligen Klageverbot geht, steht Moderna automatisch an erster Stelle der Geschützten.
Wenn der Staat den rechtlichen Schutzschirm für Moderna nicht lückenlos aufrechterhält oder Rechnungen nicht bezahlt, kann Moderna den Hahn zudrehen – also Lieferungen stoppen und den Vertrag auflösen –, ohne selbst rechtlich belangt werden zu können.
Netter Versuch einer Drohung, aber die Schweiz hatte mehr als genug Vials von anderen Herstellern und heutzutage will keiner den Scheiß mehr. Kann Moderna gerne behalten.
Diese Klausel regelt das Recht zur Verrechnung (Set-off). Es ist ein finanzielles Sicherheitsnetz für Moderna, um sicherzustellen, dass sie ihr Geld bekommen, selbst wenn der Staat eine Zahlung verweigert.
Wenn der Staat Moderna Geld für den versprochenen Haftungsschutz schuldet, darf Moderna dieses Geld einfach von anderen Beträgen abziehen, die sie eigentlich an den Staat überweisen müssten. So muss Moderna nicht dem Geld hinterherlaufen, sondern behält es einfach ein.
Da die Schweiz Moderna aber sicherlich nichts mehr Schuldet, kann Moderna nichts zurückbehalten. Ich würde es darauf ankommen lassen, ungefähr wie die Polen mit Pfizer. Was will Pfizer machen? Keine Waren mehr liefern? Ja und, dann übernehmen andere Firmen den Markt. Womit Will Moderna in diesem Fall drohen? Wir liefern euch keine Produkte mehr (die haben aktuell keine großartigen, neuen Produkte).
Der Staat hat zwar den Impfstoff gekauft, darf damit aber nicht machen, was er will. Er ist verpflichtet, dafür zu sorgen, dass jede einzelne Dose im eigenen Land bleibt, damit Moderna die weltweite Preis- und Verteilungshoheit behält.
Genau wie Regionalcodes bei DVDs verhindern sollen, dass du eine günstige DVD aus den USA oder Asien in Europa abspielst, verhindert diese Klausel den „Graumarkt“ für Impfstoffe. So wie Filmstudios die Player-Hersteller verpflichten, Codes abzufragen, verpflichtet Moderna hier den Staat, als „Polizist“ aufzutreten und jeden Export zu stoppen.
Das ist bei Medikamenten aber üblich. Pharmafirmen versuchen schon immer günstigere Reimporte aus anderen Ländern zu vermeiden dazu dient auch die Serialisierung, man kann auf der Packung auslesen, aus welchem Land zu kommt.
Unternehmen versuchen, Parallelimporte durch verschiedene Marketingstrategien einzudämmen, darunter strategische Preisgestaltung, Dienstleistungsdifferenzierung, Preissenkungen und Angebotsbeeinträchtigung [16]. Mit Hilfe von Angebotsbeeinträchtigung bzw. Mengensteuerung können Unternehmen Niedrigpreis-Vertriebskanäle schließen, um die Versorgung mit Graumarktprodukten zu unterbinden [4]. In der Pharmaindustrie beispielsweise berücksichtigen einige Hersteller den Faktor des Parallelimports bei ihren Entscheidungen über den Markteintritt oder -austritt [1]. Diese Strategie kann den Markteintritt von Parallelimporteuren verhindern, obwohl die Hersteller die Kosten für den Verlust ihrer Gewinne in den gesperrten Regionen tragen müssen. Bei Preisstrategien gleichen Unternehmen, die über mehrere Kanäle verkaufen, die Preise aus, um sich gegen Angriffe von Parallelimporteuren zu verteidigen [59]. Preisstrategien ermöglichen es Unternehmen, die negativen Auswirkungen von Parallelimporten abzumildern, ohne dabei einen Großteil ihrer Marktabdeckung zu verlieren. Zusätzlich zur Preisgestaltung können Unternehmen auch Strategien zur Dienstleistungsdifferenzierung einsetzen, um mit potenziellen Parallelimporteuren zu konkurrieren [30], indem sie ihren Kunden einen hochwertigen Service bieten.
Ein extremes Beispiel hierfür ist Sofosbuvir (Markenname Sovaldi), das Hepatitis C in über 95 % der Fälle heilen kann.
In Europa: Das Originalpräparat ist zugelassen und verfügbar, war aber bei Markteinführung extrem teuer (in Deutschland anfangs ca. 43.000 bis 60.000 Euro für eine 12-wöchige Therapie).
In Afrika/Indien: In Ländern wie Ägypten oder Indien erlaubt der Hersteller Gilead durch freiwillige Lizenzen die Produktion von Generika. Dadurch kostet die exakt gleiche Heilung dort teilweise nur unter 100 Euro.
Pharmafirmen verhindern den Verkauf dieser günstigen Generika in Europa durch strikte Marktabschottung:
Patentschutz: In Europa besitzen die Firmen Patente, die den Verkauf billiger Nachahmerprodukte verbieten. Klagen von Hilfsorganisationen gegen diese Patente wurden vom Europäischen Patentamt oft abgewiesen.
Lizenzbedingungen: Die Verträge für Afrika und Asien verbieten den Export dieser günstigen Pillen in “Hochpreisländer” wie Deutschland.
Wirtschaftliches Argument: Die Firmen argumentieren, dass sie die hohen Preise in Europa benötigen, um die Forschungs- und Entwicklungskosten zu refinanzieren. Würden die “Afrika-Preise” hier gelten, würde laut Herstellern ihr Geschäftsmodell für Innovationen zusammenbrechen.
Gilead geht in Europa aus Gier über Leichen.
In Deutschland lag die durchschnittliche COVID Letalitätsrate bei etwa 0,48 %.
Unbehandelt führt Hepatitis C in etwa 75 % der Fälle zu einer chronischen Infektion, die über Jahrzehnte hinweg schwere Leberschäden wie Zirrhose oder Leberkrebs verursachen kann.
Ohne moderne Medikamente ist das Risiko, an den Spätfolgen zu sterben, deutlich höher als das Risiko einer akuten COVID-Infektion. Allerdings ist Hepatitis C heute in über 95 % der Fälle heilbar (wenn man sich das Medikament leisten kann).
ls das Medikament auf den Markt kam, löste es eine weltweite Debatte über Ethik in der Pharmaindustrie aus. Kritiker sagen:
Ein Medikament, das eine Volkskrankheit heilen kann, darf nicht so teuer sein, dass es staatliche Budgets sprengt.
Die Pharmafirmen halten dagegen, dass die einmalige Heilung (12 Wochen Pillen) billiger sei als eine lebenslange Behandlung der Spätfolgen (Lebertransplantation, Krebs).
Ein weiteres Beispiel ist Ivermectin. Während bei Hepatitis-C-Mitteln der Patentschutz die Barriere ist, ist es bei Ivermectin im Westen eher die bürokratische Hürde (Rezeptpflicht/Zulassung), während es im globalen Süden als preiswertes Standardmedikament fungiert. Andere Strategie, gleiches Ergebnis, der Patient, der es braucht, muss es sich leisten können, wenn er überhaupt ein Rezept bekommt.
Wer sich nun also über diesen Passus im Moderna Vertrag aufregt, sollte das bei allen Medikamenten, wo das so gehandhabt wird tun und nicht nur in diesem einen Fall künstlich Entrüstung simulieren.
Wenn man aber ehrlich ist, alle Länder hatten zu viel von den Plörren, das waren Ladenhüter, die vernichtet wurden. An wen sollte man den Rest den verkaufen? Man kann sich über den Absatz aufregen, aber realistisch betrachtet, waren die Reste unverkäuflicher Sondermüll.
Andererseits ist Moderna in dieser Hinsicht auch fair. Moderna verspricht, den Impfstoff in der Schweiz an niemanden außer den Staat zu verkaufen (z. B. nicht an Privatkliniken oder Apotheken). Der Staat soll der einzige Anbieter sein. Ob das medizinrechtlich so OK ist, sei mal dahin gestellt. Der Staat als Impfdealer, der gleichzeitig Werbung für das Produkt macht und die Leute durch Gängelgesetze zur Abnahme des Produktes zwingt. Klingt irgendwie nicht OK für mich.
Moderna darf trotz dieser Sperre in der Schweiz weiterhin alles tun, was mit der Herstellung zu tun hat. Sie dürfen in der Schweiz produzieren, Rohstoffe importieren und den fertigen Impfstoff von dort aus in jedes andere Land der Welt exportieren. Streng genommen müssen sie das auch, weil in Frankreich, Spanien und den Niederlanden abgefüllt wurde, dafür muss der Stoff die Schweiz verlassen.
Hier kommt nun das, was allen Staaten das Genick brechen wird:
Wenn der Impfstoff „Off-Label“ verwendet wird (also anders als im Beipackzettel zugelassen), verliert der Staat sein Recht, Mängelansprüche gegen Moderna geltend zu machen. Wenn der Impfstoff dann nicht wirkt oder Probleme verursacht, kann der Staat Moderna nicht mehr dafür verantwortlich machen.
Das ist ein ganz normaler Passus, den man sich auch hätte sparen können, weil der für alle Medikamente gilt und schon immer galt.
Basierend auf der Fachinformation eines Medikaments definiert sich Off-Label-Use als die Anwendung eines Arzneimittels außerhalb der von den Zulassungsbehörden genehmigten Bedingungen. Die Fachinformation ist das offizielle Dokument, das den rechtlich bindenden Rahmen für den „bestimmungsgemäßen Gebrauch“ festlegt.
Eine Anwendung gilt als Off-Label-Use, wenn sie von den Angaben in folgenden Abschnitten der Fachinformation abweicht:
Anwendungsgebiete (Indikation): Das Medikament wird gegen eine Krankheit oder Symptome eingesetzt, die dort nicht aufgeführt sind.
Patientengruppen: Einsatz bei Personen, die nicht der zugelassenen Altersgruppe (z. B. Kinder statt Erwachsene), dem Geschlecht oder anderen spezifischen Merkmalen entsprechen.
Dosierung und Anwendung: Die verordnete Menge, die Häufigkeit der Einnahme oder der Zeitraum der Behandlung unterscheidet sich von den Vorgaben im Text.
Art der Anwendung (Applikationsweg): Das Mittel wird anders verabreicht als vorgesehen, beispielsweise als Injektion statt als Tablette.
Gegenanzeigen (Kontraindikationen): Anwendung bei Patienten, bei denen laut Fachinformation eigentlich ein Ausschlussgrund vorliegt.
Im Falle eines Off-Label-Use entfällt in der Regel die Haftung des pharmazeutischen Unternehmers für Schäden, da das Produkt nicht gemäß der genehmigten Fachinformation verwendet wurde. In diesem Fall haftet der Arzt.
Die Schweiz hat Spikevax jedoch explizit damit beworben und empfohlen, dass es schwere COVID-19-Verläufe verhindert. Dies war eine zentrale Säule der nationalen Impfstrategie und der offiziellen Kommunikation.
Man hat einen off-label use beworben!
Damit ist Moderna raus aus aller Haftung durch die Dummheit der Staaten und das zu Recht! Keine Firma kann dafür verantwortlich gemacht werden, wenn der Nutzer ein Produkt falsch verwendet oder missbraucht.
Auch die Empfehlung für Schwangere ist nicht auf Moderna Mist gewachsen, das hat die Schweiz verbockt.
Die Lieferbedingungen finde ich nicht so spannend. Natürlich sichert sich Moderna bei Lieferproblemen ab. Qualitätsmängel sind spannender, denn das ganze Produkt war ein einziger Qualitätsmangel (aus Sicht der Gegner des Produktes).
Ein Mangel liegt vor, wenn der Impfstoff nicht nach den vereinbarten Spezifikationen, den cGMP (aktuelle gute Herstellungspraxis) oder geltenden Gesetzen hergestellt wurde.
Und hier haben wir wieder das Problem, was wäre current GMP gewesen? Wo sind die Methoden, nach denen geprüft werden müsste definiert. War Sichtprüfung cGMP oder HPLC? Wo steht das?
Der Staat muss den Impfstoff sofort bei Lieferung prüfen. Nur… auf welche Art und Weise? Wer hat geprüft, um gegebenenfalls einen Mangel zu attestieren?
Wenn ein Fehler erst später entdeckt wird (der bei der Lieferung nicht erkennbar war), hat der Staat ab Entdeckung 30 Tage Zeit für die Meldung – aber nur bis zum Ablaufdatum des Impfstoffs.
Fallen DNA Produktionsrückstände darunter?
Können Staaten nicht einfach die Ablaufdaten verlängern? Deutschland hat die Haltbarkeit von COVID-19-Impfstoffen mehrfach verlängert. Das ließe sich staatsseitig durchaus aushebeln.
Diese Klausel schließt die Haftung von Moderna für mangelhafte Produkte weitgehend aus und macht die in Abschnitt 10.1(i) genannte Ersatzlieferung zur einzigen Entschädigung für den Käufer. Besonders brisant ist, dass Moderna keine Haftung für Sicherheit, Wirksamkeit oder nicht Marktfähigkeit des Produktes übernimmt, sofern die Herstellung gemäß cGMP erfolgte.
“Moderna will have no obligation for any Product Claims to the extent the Deficient Product was caused by: (a) deficiencies in the safety, efficacy, or marketability of the Product or its distribution;”
„Moderna übernimmt keine Haftung für Produktansprüche, sofern das mangelhafte Produkt auf folgende Ursachen zurückzuführen ist: (a) Mängel hinsichtlich der Sicherheit, Wirksamkeit oder Marktfähigkeit des Produkts oder dessen Vertrieb;“
Wenn das Produkt Spikevax nicht sicher, nicht wirksam und nicht marktfähig war, ist das eben das Pech des Käufers.
Das steht bei BioNTech/Pfizer auch in den Verträgen, nur besser verständlich und einfacher geschrieben.
Moderna sagt: „Solange wir behaupten können, dass wir die Fabrik-Regeln (cGMP) eingehalten haben, sind wir für alles andere – ob es wirkt, ob es sicher ist oder ob es seltsame Fehler hat, die keiner erklären kann – nicht verantwortlich.“
Wie erwähnt, cGMP ist nirgends for modRNA-LNP definiert, man diskutiert noch immer darüber, Jahre später.
Was bedeutet ein nicht marktfähiges Produkt, das nach cGMP hergestellt wurde? Das klingt nach einen Oxymoron. cGMP sollte eigentlich eine Marktfähigkeit garantieren.
Die Fabrik hat alles richtig gemacht, aber das Rezept oder das Ergebnis taugen trotzdem nichts.
Stell dir vor, ein Bäcker hält sich exakt an die Hygienevorgaben und die Backzeit (das wäre das cGMP – die “Gute Herstellungspraxis”). Wenn aber im Rezept steht, dass er Salz statt Zucker nehmen soll, ist der Kuchen am Ende ungenießbar und nicht verkaufbar (nicht marktfähig), obwohl er “sauber” produziert wurde.
Die zentralen Dokumente für cGMP waren möglichweise EudraLex Volume 4 (Good Manufacturing Practice Guidelines) ABER da mRNA-Impfstoffe rechtlich als biologische Arzneimittel eingestuft wurden, galt primär der Annex 2 für biologische Wirkstoffe, was biologisch nicht ganz richtig ist, weil es sich um nanomedizinische Gentherapie handelt und nicht um einfache monoklonale Antikörper oder andere gängige Proteine handelt. Die Probleme zu denen es kommen kann, sind also in cGMP gar nicht erfasst.
Dennoch wurden Moderna und seine wichtigsten Lohnfertiger mehrfach von der US-Gesundheitsbehörde FDA wegen Verstößen gegen die cGMP gerügt. Diese Rügen erfolgen meist in Form eines „Form 483“ (Mängelbericht nach einer Inspektion)
Das Hauptwerk von Moderna in Norwood, Massachusetts, stand mehrfach im Fokus der FDA:
September 2023 (Form 483): Die FDA stellte fünf gravierende Mängel fest.
Reinigungsprobleme: Moderna gab acht Chargen des Wirkstoffs frei, obwohl die Ausrüstung die Reinigungstests (auf Endotoxine und Keime) nicht bestanden hatte.
Abgelaufene Materialien: Im Lager wurden über 2.000 abgelaufene Artikel gefunden, die nicht ordnungsgemäß von nutzbaren Materialien getrennt waren. Teilweise wurden abgelaufene Stoffe sogar in der Produktion verwendet.
Kontaminationsrisiko: Es fehlten ausreichende Maßnahmen gegen Verunreinigungen aus der Luft.
Lonza produzierte den Wirkstoff für Moderna unter anderem in Visp (Schweiz) und Hopkinton (USA):
Visp (Schweiz): Auch hier gab es Inspektionen mit Mängeln. In einem Form 483 wurde bemängelt, dass Labordaten unvollständig waren und Grenzwerte für Keimzahlen in Wasserproben nicht exakt dokumentiert wurden.
Hopkinton (USA): Lonza erhielt in der Vergangenheit (vor der Pandemie) sogar einen Warning Letter (eine schärfere Rüge als ein Form 483) wegen erheblicher cGMP-Verstöße bei der Wirkstoffherstellung.
Catalent übernahm das „Fill & Finish“ (Abfüllen des Impfstoffs in Fläschchen) für Moderna in Bloomington, Indiana:
September 2022: FDA-Inspektoren fanden Qualitätsprobleme, darunter sichtbare Partikel in einigen Fläschchen.
Die Firma wurde gerügt, weil sie Kundenbeschwerden über Partikel nicht gründlich genug untersuchte.
Samsung Biologics füllt ebenfalls Impfstoffe für Moderna ab:
Oktober 2023 & Mai 2025 (Form 483): Die FDA rügte Samsung Biologics mehrfach wegen Datenintegrität und mangelhafter Anlagenpflege.
Mitarbeiter nutzten geteilte Passwörter für IT-Systeme, was eine nachträgliche Kontrolle von Änderungen unmöglich machte.
Testgeräte wurden nicht in den vorgeschriebenen Intervallen neu kalibriert
Bei der Produktion einer Charge von Spikevax wurde in einem einzelnen Fläschchen ein Fremdkörper entdeckt. Nach der Untersuchung stellte sich heraus, dass es sich um eine Mücke handelte, die während des Abfüllprozesses in das Fläschchen gelangt war.
Mit der Mücke sind wir bei Section 6.4 ii, wonach Moderna nicht für „unaufklärbare Gründe“ haftet. Ein Insekt in der Anlage ist jedoch ein klarer Verstoß gegen die cGMP (Hygienevorschriften). In so einem Fall greift die Haftung meist doch, weshalb Moderna die Kosten für diesen Rückruf (Recall) selbst tragen musste und der Staat hier ausnahmsweise Geld zurückfordern oder Ersatz verlangen konnte.
Im August 2021 wurden in Japan ca. 1,63 Millionen Dosen von Moderna suspendiert und später zurückgerufen, weil die Fläschchen Metallpartikel enthielten. Es handelte sich um Partikel aus Edelstahl (Typ 316L). Diese entstanden durch die Reibung zweier falsch montierter Metallteile in der Maschine, die die Stopfen auf die Fläschchen setzt.
Kurz nach der Verabreichung von Dosen aus den betroffenen Chargen starben drei Männer. Eine offizielle Untersuchung ergab jedoch keinen direkten kausalen Zusammenhang zwischen den Partikeln und den Todesfällen.
Da Metallpartikel in der Flüssigkeit ein klarer Verstoß gegen die Herstellungsvorschriften (cGMP) sind, handelt es sich um ein „Deficient Product“. In diesem Fall muss der Hersteller den Schaden (durch Ersatz oder Rückzahlung) oft selbst tragen.
Der Staat haftet zwar für allgemeine Nebenwirkungen des korrekt hergestellten Impfstoffs, aber wenn der Hersteller „schlampig“ arbeitet (z. B. Metallabrieb in der Anlage), greift die staatliche Schutzgarantie meist nicht. Moderna musste hier für die logistischen Kosten des Fehlers selbst geradestehen.
Fallen verunreinigte Lipide, die nicht 99,9% sauber sind, unter schlampige Arbeit?
Die cGMP-Regeln verlangen, dass jeder Rohstoff vor der Verwendung geprüft wird.
Wenn Moderna oder ein Lohnfertiger (wie Lonza) Lipide verwendet, ohne deren Reinheit ausreichend zu testen, oder wissentlich „schmutzige“ Lipide einsetzt, ist das ein direkter Verstoß gegen die Herstellungsvorschriften.
Das betrifft auch BioNTech/Pfizer. Darüber könnte man sie noch ran bekommen.
Wenn nachgewiesen werden kann, dass der Impfstoff wegen verunreinigter Lipide unsicher oder unwirksam ist, kann Moderna (und auch BioNTech/Pfizer) sich nicht mehr auf die allgemeine Haftungsfreistellung berufen. In diesem Fall gilt das Produkt als „Deficient Product“ (mangelhaftes Produkt). Moderna müsste den Schaden dann selbst tragen und könnte die Kosten nicht auf den Staat abwälzen.
Wissenschaftliche Studien haben gezeigt, dass Verunreinigungen in Lipiden tatsächlich die Stabilität der mRNA massiv beeinträchtigen können, z. Bsp. durch die Bildung von Addukten.
Das Witzige daran: Der Artikel ist von Moderna selbst
Ob eine Reinheit von „nur“ 98 % statt 99,9 % bereits als schwere Schlamperei gilt, hängt am Ende davon ab, was exakt in den geheimen Zulassungsakten als Grenzwert vereinbart wurde. Liegt der Wert unter diesem Limit, ist es ein klarer Rechtsbruch.
Dass die Lipide schmutzig waren, habe ich schon ausführlich beschrieben.
Das wäre also ein juristisch theoretisch gangbarer Weg, zumal teils Verunreinigungen enthalten sind, die man bisher nicht einmal chemisch definieren und zuordnen konnte. Man müsste nun aus Rückstellproben die Reinheit der Lipide untersuchen.
Dafür muss der Staat den „Beweis“ (den defekten Impfstoff) wie in einer Asservatenkammer aufbewahren und darf ihn nur nach Anweisung von Moderna bewegen oder vernichten. Wer am Ende die Zeche zahlt, hängt davon ab, wer im Qualitätsstreit recht bekommt.
Moderna sichert dem Käufer als „Demand Confirmation Beneficiary“ eine anteilige, priorisierte Belieferung parallel zu anderen frühen Regierungsabnehmern zu, jedoch unter ausdrücklichem Vorrang der Vereinigten Staaten. Das war aber nicht Modernas Entscheidung, das lag an Trumps Executive Order 13962. Die Verordnung legte fest, dass die US-Regierung sicherstellen muss, dass amerikanische Bürger vorrangigen Zugang zu Impfstoffen erhalten, die mit US-Steuergeldern entwickelt oder gekauft wurden. Erst wenn genügend Impfstoff für alle Amerikaner vorhanden ist, die sich impfen lassen wollen, dürfen die Behörden andere Länder bei der Beschaffung unterstützen oder Impfstoffe exportieren. Moderna, als US-Firma, musste das daher in den Vertrag schreiben, sonst hätte die Firma Probleme im eigenen Land bekommen.
Diese Klausel ist eine der finanziell wichtigsten für Moderna, da sie den Preis an die Menge des Wirkstoffs (Mikrogramm) bindet, nicht an die Anzahl der Behandlungen oder Menschen, die damit geimpft werden können. Falls sich in den Studien herausstellt, dass man statt 100 µg 200 µg pro Spritze braucht, bekommt der Staat zwar weiterhin die bestellte Menge an Wirkstoff, kann damit aber nur noch halb so viele Menschen impfen. DAS stand im Vorvertrag noch anders drinnen. Da hat wohl jemand bei Moderna eins auf den Deckel bekommen, wie man so doof sein kann und hat das im finalen Vertrag angepasst. Die 50µg Dosis war zu diesem Zeitpunkt bereits raus.
Damit sind wir erst auf Seite 19 von 54. Das wird für einen Artikel zu lang, dieser Vertrag brauch alleine wohl zwei Artikel.
Vieles in diesem Vertrag klingt auf den ersten Blick unverschämt, ist bei näherem Hinsehen aber gängige Praxis, über die sich sonst keiner aufregt.
Unterstützungsmöglichkeiten:
Bücherwunschzettel: https://www.amazon.de/registries/gl/owner-view/30LG3DJ4ET90L?ref_=list_d_gl_lfu_nav
Andere Unterstützungsmöglichkeiten für Holgers und meine Forschung:
Konto für Unterstützung für das Projekt Scan 2000
Dr. Merse DE34 4305 0001 0302 7851 75 Sparkasse Bochum
Horst Reissner: IBAN DE51 4401 0046 0406 4514 67
Dr. S. Stebel: https://ko-fi.com/einmalmitprofisarbeiten
Keystone-Sda. (2021, June 2). Lonza baut neue Produktionslinie für Moderna. March 24. https://march24.ch/articles/69672-lonza-baut-neue-produktionslinie-fuer-moderna
[email protected]. (n.d.). ROVI and Moderna Announce Collaboration for Outside the United States Fill-Finish Manufacturing of Moderna’s COVID-19 Vaccine Candidate. https://www.rovi.es/en/content/rovi-and-moderna-announce-collaboration-outside-united-states-fill-finish-manufacturing
Additional manufacturing capacity for Moderna’s COVID-19 vaccine | European Medicines Agency (EMA). (2021, June 11). European Medicines Agency (EMA). https://www.ema.europa.eu/en/news/additional-manufacturing-capacity-modernas-covid-19-vaccine
Moderna, the coronavirus vaccine made in Switzerland. (n.d.). House of Switzerland. https://houseofswitzerland.org/swissstories/science-education/moderna-coronavirus-vaccine-made-switzerland
Executive Order on Ensuring Access to United States Government COVID-19 Vaccines – The White House https://trumpwhitehouse.archives.gov/presidential-actions/executive-order-ensuring-access-united-states-government-covid-19-vaccines/
Gorodensky A, Kohler JC. State capture through indemnification demands? Effects on equity in the global distribution of COVID-19 vaccines. J Pharm Policy Pract. 2022 Aug 19;15(1):50. doi: 10.1186/s40545-022-00442-y. PMID: 35986397; PMCID: PMC9388983. https://pmc.ncbi.nlm.nih.gov/articles/PMC9388983/
Huang, H., He, Y., & Chen, J. (2018). Competitive strategies and quality to counter parallel importation in global market. Omega, 86, 173–197. https://doi.org/10.1016/j.omega.2018.07.009
Hepatitis-C-Medikament Sofosbuvir bleibt oft unerschwinglich. (n.d.). Deutsche Aidshilfe. https://www.aidshilfe.de/de/meldung/hepatitis-c-medikament-sofosbuvir-bleibt-viele-unerschwinglich
Global Report on Access to Hepatitis C Treatment: Focus on Overcoming Barriers https://www.aidsdatahub.org/sites/default/files/resource/global-report-access-hepatitis-c-treatment-overcoming-barriers.pdf
Europäisches Patentamt entscheidet über Patent auf wichtiges Hepatitis-C-Medikament Statement von Ärzte ohne Grenzen. (2021, December 10). Ärzte Ohne Grenzen Österreich. https://www.aerzte-ohne-grenzen.at/article/europaeisches-patentamt-entscheidet-ueber-patent-auf-wichtiges-hepatitis-c-medikament
Zu teuer für die Allgemeinheit – science.ORF.at. (n.d.). science.ORF.at. https://science.orf.at/v2/stories/2935952/
Walsh N, Durier N, Khwairakpam G, Sohn AH, Lo YR. The hepatitis C treatment revolution: how to avoid Asia missing out. J Virus Erad. 2015 Oct 1;1(4):272-5. doi: 10.1016/S2055-6640(20)30924-9. PMID: 27482424; PMCID: PMC4946660. https://pmc.ncbi.nlm.nih.gov/articles/PMC4946660/
Spikevax, INN-COVID-19 mRNA Vaccine (nucleoside modified); https://ec.europa.eu/health/documents/community-register/2021/20211208154383/anx_154383_de.pdf
Ärzteblatt, D. Ä. G. R. D. (n.d.-a). Corona: Verfalldatum für gefrorene Impfstoffe verlängert. Deutsches Ärzteblatt. https://www.aerzteblatt.de/archiv/corona-verfalldatum-fuer-gefrorene-impfstoffe-verlaengert-1029457c-4902-4230-b9cb-8a1f57a21177
EudraLex – Volume 4 – Public Health – European Commission https://health.ec.europa.eu/medicinal-products/eudralex/eudralex-volume-4_en
Exclusive: US FDA finds control lapses at Moderna manufacturing plant | Reuters https://www.reuters.com/business/healthcare-pharmaceuticals/us-fda-finds-control-lapses-moderna-manufacturing-plant-2023-12-15/
FDA Finds QC Failures at Moderna’s Norwood Mfg. Facility | Contract Pharma https://www.contractpharma.com/breaking-news/fda-finds-qc-failures-at-modernas-norwood-mfg-facility/
Lonza Biologics Warning Letter. (n.d.). http://www.expertbriefings.com/lonza-biologics-warning-letter/
FDA Finds Flaws at Vaccine Factory, Accepts Moderna’s Assurances – Bloomberg https://www.bloomberg.com/news/articles/2022-09-20/fda-finds-flaws-at-vaccine-factory-accepts-moderna-s-assurances
FDA lands Samsung Bio 483, 6 observations – BioProcess Insider https://www.bioprocessintl.com/regulations/fda-lands-samsung-biologics-483-with-6-observations
Aus der Mücke einen Elefanten gemacht? Moderna ruft 764.000 Impfdosen wegen „Fremdkörper“ zurück | Euronews https://de.euronews.com/2022/04/13/aus-der-mucke-einen-elefanten-gemacht-moderna-ruft-764-000-impfdosen-wegen-fremdkorper-zur
Japan’s Takeda says ‚human error‘ caused contamination of Moderna vaccines | Reuters https://www.reuters.com/world/asia-pacific/japans-takeda-says-human-error-caused-contamination-moderna-vaccines-2021-10-01/
Moderna to recall COVID-19 doses in Japan after stainless steel contaminants found | Reuters https://www.reuters.com/business/healthcare-pharmaceuticals/japan-finds-stainless-steel-particles-suspended-doses-moderna-vaccine-2021-09-01/
Moderna report says ‚human error‘ to blame for contamination found in 3 vaccine lots from Rovi plant | Fierce Pharma https://www.fiercepharma.com/manufacturing/moderna-report-says-human-error-to-blame-for-rovi-releasing-3-vaccine-lots-after
Packer M, Gyawali D, Yerabolu R, Schariter J, White P. A novel mechanism for the loss of mRNA activity in lipid nanoparticle delivery systems. Nat Commun. 2021 Nov 22;12(1):6777. doi: 10.1038/s41467-021-26926-0. PMID: 34811367; PMCID: PMC8608879. https://pubmed.ncbi.nlm.nih.gov/34811367/
Executive Order on Ensuring Access to United States Government COVID-19 Vaccines – The White House https://trumpwhitehouse.archives.gov/presidential-actions/executive-order-ensuring-access-united-states-government-covid-19-vaccines/