Das ist der zweite Schreckenberg Artikel, welcher zeigt, dass das Spike-Protein Herzzellen schadet. Ich hatte ihm damals Fragen zu seiner Publikation gestellt, die er leider nie beantwortet hat.
Nun hat diese Arbeitsgruppe eine genauere Untersuchung der beiden modRNA-Produkte von BioNTech/Pfizer und Moderna herausgebracht. Der Artikel ist frei zugänglich.
Schreckenberg, R., Woitasky, N., Itani, N., Czech, L., Windhorst, A. C., Juchem, M., Bär, C., Thum, T., Ferdinandy, P., & Schulz, R. (2026). mRNA-based SARS-CoV-2 vaccines: intracellular processing and aggregation of the encoded spike protein as a mechanistic contributor to cardiac cellular stress. Frontiers in Immunology, 17. https://doi.org/10.3389/fimmu.2026.1635478 https://www.frontiersin.org/journals/immunology/articles/10.3389/fimmu.2026.1635478/full?
Ein Problem, welches der Artikel hat ist, die Mischung aus sauber hergestellten LNPs der Marke Eigenbau und Original Produkt mRNA-1273 (Moderna) und BNT162B2 (BioNTech/Pfizer), leider wieder einmal ohne Chargenangabe.
Die leeren LNPs wurden selbst gemischt:
Für die Comirnaty-Formulierung ALC-0315 wurden Cholesterin, DSPC und ALC-0159 in einem Molverhältnis von 46,3/42,7/9,4/1,6 % gemischt. Zur Herstellung der Spikevax-Formulierung wurden SM-102, Cholesterin, DSPC und DMG-PEG2000 in einem Molverhältnis von 50/38,5/10/1,5 % kombiniert.
Auch hier haben wir bereits das Problem, das kleinste Abweichungen in der Mischung andere immunologische Reaktionen hervorrufen können.
Die LNPs mit Spike-Protein waren wohl Originale
Sie wurden bei einer Konfluenz von 60–70 % mit identischen Konzentrationen von authentischem BNT162b2 (2,0 µl oder 0,2 µg RNA/ml) oder mRNA-1273 (3,3 µl oder 0,66 µg RNA/ml) aus Originalfläschchen inkubiert.
Die leeren LNPs musste die Gruppe natürlich selbst herstellen und auch die LNPs mit Glühwürmchen Luciferase. Das Problem bei den selbst hergestellten LNPs ist, dass die Autoren sauberer gearbeitet haben, als die Hersteller. Damit fallen natürlich Probleme weg, welche die echten Produkte haben, wie Kontaminationen durch DNA-Rückstände oder modRNA-Fragmente. Die Marke Eigenbau war möglicherweise sauberer als die echten Produkte und hatte zudem möglicherweise eine leicht andere Zusammensetzung.
Um doppelsträngige RNA-Nebenprodukte zu eliminieren, wurde die RNA mittels Ionenpaar-Umkehrphasen-Hochleistungsflüssigkeitschromatographie gereinigt.
Das haben die Hersteller definitiv nicht gemacht.
Das bedeutet, dass diese Nachbauten unter Umständen den Prozess 1 Produkten ähnlich sind, aber wenig mit dem verschmutzen echten Produkten nach Prozess 2 zu tun haben. Der Artikel vergleicht sauber hergestellte Kontrollen mit Produkten voller Produktionsrückstände und teils anderen Lieferanten der Lipide (Merck, Acuitas).
Wenn nur die Glühwürmchen-Luciferase Eigenbau war, kann es sein, dass diese LNPs weniger Probleme bereiten, weil sie sauberer sind, als die COVID-Original Präparate?
Die Lipide wurde nicht auf ihre Reinheit mittels HPLC oder MS überprüft. Auch ein schwieriger Punkt. Die Lipide von Cayman Chemicals waren definitiv nur Biotech Grade, als ich mir das Sicherheitsdatenblatt das letzte Mal angesehen habe. Acuitas war tatsächlich Lieferant für die Studienmedikation, ist auch nicht USP Qualität und später lieferten auch Merck und Evonick.
Die Autoren haben diesmal nicht selbst hergestelltes Zellkulturen aus frisch entnommenen Rattenherzen genommen sondern normierte, käuflich erwerbbare Zelllinien. Diese Zellen entsprechen somit auch nicht normalen menschlichen Zellen, weil sie alle eigentlich unsterbliche Zelllinien sind. Damit wird in diesem Artikel nur gezeigt, wie sich Produkte nach Prozess 1 in Krebszellen oder embryonalen Zellen verhalten könnten, wenn man ein maximal sauberes Produkt aus Prozess 1 genommen hätte im Vergleich zu einem handelsüblichen Produkt nach Prozess 2.
Die humane Kardiomyozyten-Zelllinie AC16 (#SCC109, Merck KGaA, Deutschland), die aus der Fusion von Primärzellen aus adultem humanem ventrikulärem Herzgewebe mit SV40-transformierten Fibroblasten gewonnen wird, wurde erstmals 2005 beschrieben.
The two cell lines HEK-293 (#85120602, Merck KGaA, Germany) and HeLa (#93021013, Merck KGaA, Germany)
HEK-293-Zellen (Human Embryonic Kidney) sind humane embryonale Nierenzellen.
HeLa Zellen sind Adenokarzinomzellen eines Gebärmutterhalses
Die ersten Spike-Monomere wurden innerhalb von nur zwei Stunden (h) nach der Anwendung von BNT162b2 bzw. mRNA-1273 in menschlichen AC16-Kardiomyozyten nachgewiesen.
1. Versuche in humanen Kardiomyozyten AC16
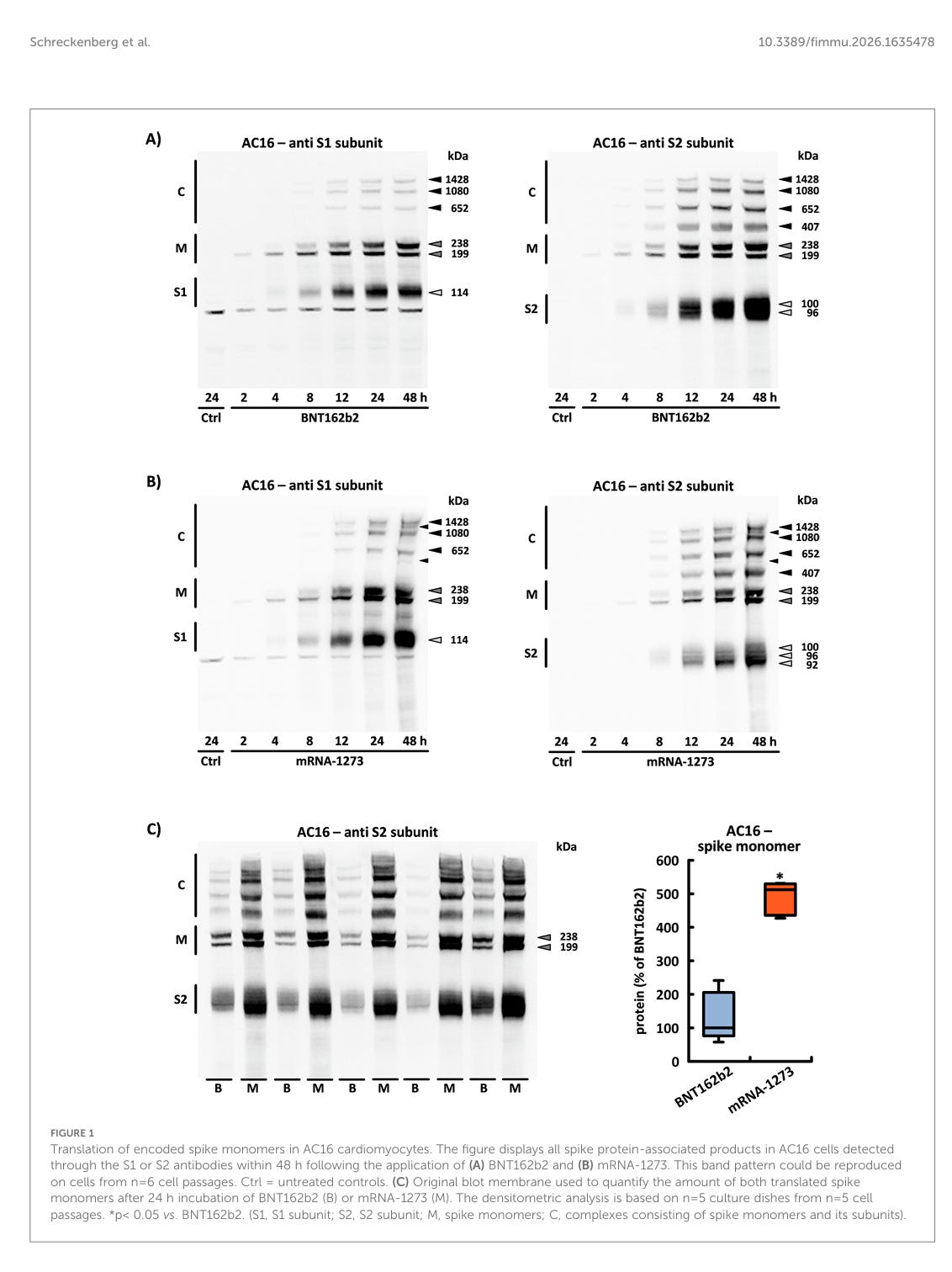
Translation von kodierten Spike-Monomeren in AC16-Kardiomyozyten. Die Abbildung zeigt alle Spike-Protein-assoziierten Produkte in AC16-Zellen, die innerhalb von 48 Stunden nach der Anwendung von (A) BNT162b2 und (B) mRNA-1273 durch die Antikörper S1 oder S2 nachgewiesen wurden. Dieses Bandenmuster konnte auf Zellen aus n=6 Zellpassagen reproduziert werden. Ctrl = unbehandelte Kontrollen. (C) Original-Blot-Membran, die zur Quantifizierung der Menge beider translatierter Spike-Monomere nach 24-stündiger Inkubation von BNT162b2 (B) oder mRNA-1273 (M) verwendet wurde. Die densitometrische Analyse basiert auf n = 5 Kulturplatten aus n = 5 Zellpassagen. *p< 0,05 vs. BNT162b2. (S1, S1-Untereinheit; S2, S2-Untereinheit; M, Spike-Monomere; C, Komplexe aus Spike-Monomeren und ihren Untereinheiten).
Die Abbildung zeigt alle Spike-Protein-assoziierten Produkte in AC16-Zellen, die innerhalb von 48 Stunden nach der Anwendung von (A) BNT162b2 und (B) mRNA-1273 durch die Antikörper S1 oder S2 nachgewiesen wurden.
Diesen Satz muss man genau lesen: “Alle Spike-Protein-assoziierten Produkte, die […] durch die Antikörper S1 oder S2 nachgewiesen wurden.”
Fehlgefaltete Proteine, bei denen die Bindestellen der Antikörper verändert sind, werden somit nicht erfasst. Wieviel fehlgefaltetes Protein oder Proteine in anderen Leserastern entstanden sind, wird mit dieser Methode nicht erfasst.
Was man auch als Laie in den obigen Bildern sehen kann: Da sind zu viele Banden! Wenn eine spezifische S1 Einheit oder S2 Einheit produziert wird, sollte da genau je eine Bande in der richtigen Größe sein. Multimere sollten bei SDS Page nicht vorkommen, weil es sich um ein denaturierendes Gel handelt und die Proben vor dem Auftrag auf das Gel auf 85°C erhitzt wurden. Wenn es da noch Aggregate neben den Monomeren gibt, sind diese sehr, sehr stabil. Möglicherweise thermostabil?
Ich hatte in meiner Promotion auch ein trimeres, thermostabiles Protein (CAT I), nach dem erhitzen und auftragen auf ein SDS Gel sah man nur noch die Monomerenbande.
Die Proteinüberstände wurden dann nach Bedarf verdünnt, gemäß der Methode von Lämmli mit SDS-Probenpuffer (reduzierend, 2x; #S3401, Merck KGaA, Deutschland) gemischt und 5 Minuten lang auf 85 °C erhitzt.
Definitiv kein nicht-denaturierendes Gel. Hier sollten molekulare Interaktionen, die nicht allzu fest sind, gelöst werden. Das könnte ein Hinweis auf Verunreinigung mit LPS sein?
In beiden Fällen führt die Translation von BNT162b2 und mRNA-1273 zu Proteinen mit identischer Aminosäuresequenz und intakter Furin-Spaltstelle. Nach der enzymatischen Spaltung konnten die beiden Spike-Untereinheiten (S1 und S2) nach etwa 4 Stunden nachgewiesen werden. Mit einem Molekulargewicht von 114 kDa wurde die S1-Untereinheit sowohl aus BNT162b2 als auch aus mRNA-1273 gebildet. Es gab jedoch Unterschiede in der Anzahl der auftretenden S2-Untereinheiten. Im Fall von BNT162b2 trennten sich zwei S2-Untereinheiten unterschiedlicher Größe konsistent voneinander, während im Fall von mRNA-1273 die Anzahl der S2-Untereinheiten immer drei betrug (siehe Abbildungen 1A, B).
Zwei bis drei unterschiedliche S2 Untereinheiten? Was das wohl immunologisch verursacht?
Die intrazelluläre Bildung von hochmolekularen Spike-Protein-Aggregaten
Etwa 8 Stunden nach der Verabreichung von BNT162b2 bzw. mRNA-1273 entstanden in den Zellen hochmolekulare Komplexe aufgrund der Bildung kovalenter Bindungen zwischen dem Spike-Monomer und seinen S1- oder S2-Untereinheiten. Die Zusammensetzung dieser Proteinkomplexe wurde in n=6 unabhängigen Zellpassagen untersucht. Sowohl das Molekulargewicht als auch die Bandenintensität dieser Komplexe zeigten ein konsistentes Muster. Dementsprechend kann eine zufällige Aggregation ausgeschlossen werden (siehe Abbildungen 1A, B).
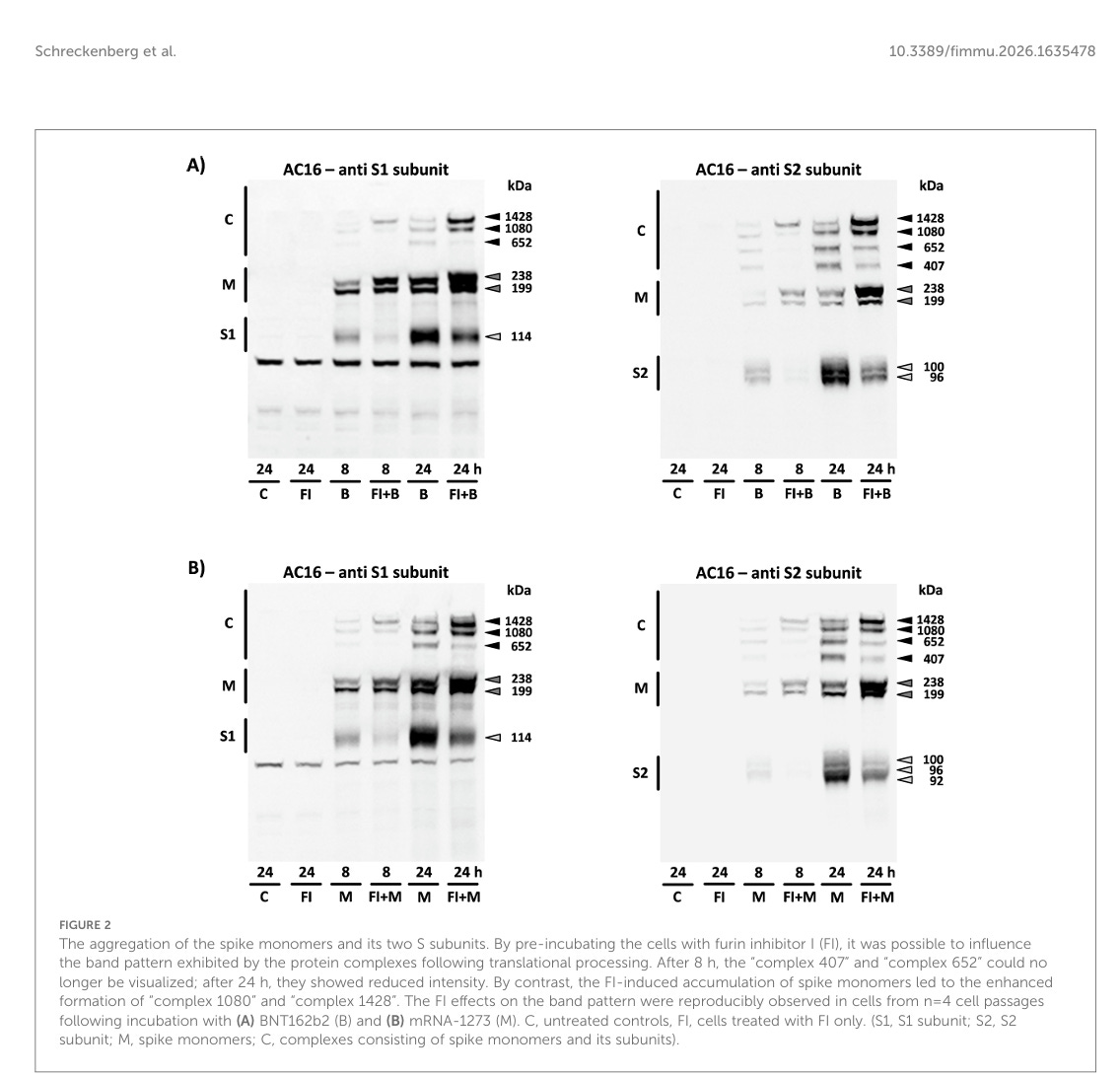
Aufgrund ihrer ausgezeichneten Spezifität gegenüber der S1- oder S2-Untereinheit konnte allein anhand des verwendeten Antikörpers geschlossen werden, dass „Komplex 407“ ausschließlich aus S2-Untereinheiten bestand. Nach Vorinkubation der Zellen mit dem Furin-Inhibitor I wurde die Bildung der S-Untereinheiten über einen Zeitraum von 8 Stunden fast vollständig verhindert, wodurch das Bandenmuster spezifisch beeinflusst wurde. „Komplex 407”, der ausschließlich in Verbindung mit dem S2-Antikörper nachgewiesen wurde, war unter diesen Bedingungen nicht mehr zu beobachten. „Komplex 652”, der zuvor von beiden Antikörpern erkannt wurde, wurde ebenfalls nicht mehr nachgewiesen und bestand somit aus den S1- und S2-Untereinheiten. Die beiden Komplexe mit dem höchsten Molekulargewicht („Komplex 1080“ und „Komplex 1428“), die ebenfalls von beiden Antikörpern nachgewiesen wurden, nahmen in ihrer Intensität deutlich zu. Dementsprechend wurden sie durch die sich anreichernden Spike-Monomere gebildet (siehe Abbildungen 2A, B). Zwei weitere Banden mit einem Molekulargewicht von 538 kDa bzw. 1286 kDa konnten aufgrund ihrer geringen Intensität nur bei optimaler Trennung und effizienter Übertragung nachgewiesen werden (siehe Abbildung 1B).
Ich hätte da eine Idee, woran das liegen könnte.
Die Aggregation der Spike-Monomere und ihrer beiden S-Untereinheiten. Durch Vorinkubation der Zellen mit Furin-Inhibitor I (FI) konnte das Bandenmuster beeinflusst werden, das die Proteinkomplexe nach der translationalen Verarbeitung aufwiesen. Nach 8 Stunden waren „Komplex 407” und „Komplex 652” nicht mehr sichtbar, nach 24 Stunden zeigten sie eine verringerte Intensität. Im Gegensatz dazu führte die FI-induzierte Akkumulation von Spike-Monomeren zu einer verstärkten Bildung von „Komplex 1080” und „Komplex 1428”. Die FI-Effekte auf das Bandenmuster wurden reproduzierbar in Zellen aus n=4 Zellpassagen nach Inkubation mit (A) BNT162b2 (B) und (B) mRNA-1273 (M) beobachtet. C, unbehandelte Kontrollen, FI, nur mit FI behandelte Zellen. (S1, S1-Untereinheit; S2, S2-Untereinheit; M, Spike-Monomere; C, Komplexe aus Spike-Monomeren und ihren Untereinheiten).
2. Die Versuche in HEK und HeLa Zellen
Um zu schauen, ob andere Zelltypen sich anders verhalten als humane Kardiomyozyten, hat die Gruppe die Versuche noch in zwei anderen Zelllinien gemacht.
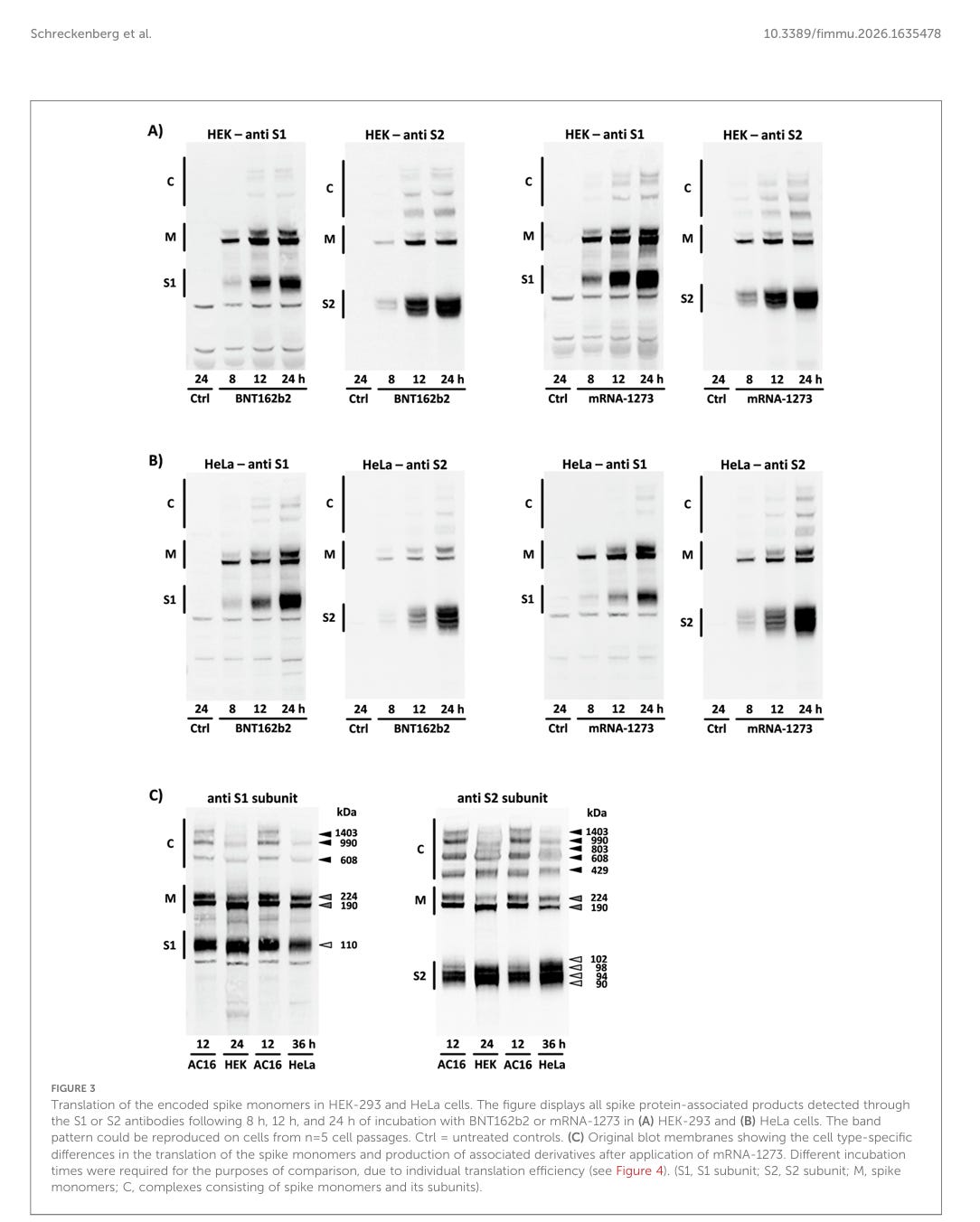
Translation der kodierten Spike-Monomere in HEK-293- und HeLa-Zellen. Die Abbildung zeigt alle Spike-Protein-assoziierten Produkte, die nach 8, 12 und 24 Stunden Inkubation mit BNT162b2 oder mRNA-1273 in (A) HEK-293- und (B) HeLa-Zellen mittels der Antikörper S1 oder S2 nachgewiesen wurden. Das Bandenmuster konnte auf Zellen aus n = 5 Zellpassagen reproduziert werden. Ctrl = unbehandelte Kontrollen. (C) Original-Blot-Membranen, die die zelltypspezifischen Unterschiede bei der Translation der Spike-Monomere und der Produktion assoziierter Derivate nach Anwendung von mRNA-1273 zeigen. Aufgrund der individuellen Translationseffizienz waren für Vergleichszwecke unterschiedliche Inkubationszeiten erforderlich (siehe Abbildung 4). (S1, S1-Untereinheit; S2, S2-Untereinheit; M, Spike-Monomere; C, Komplexe aus Spike-Monomeren und ihren Untereinheiten).
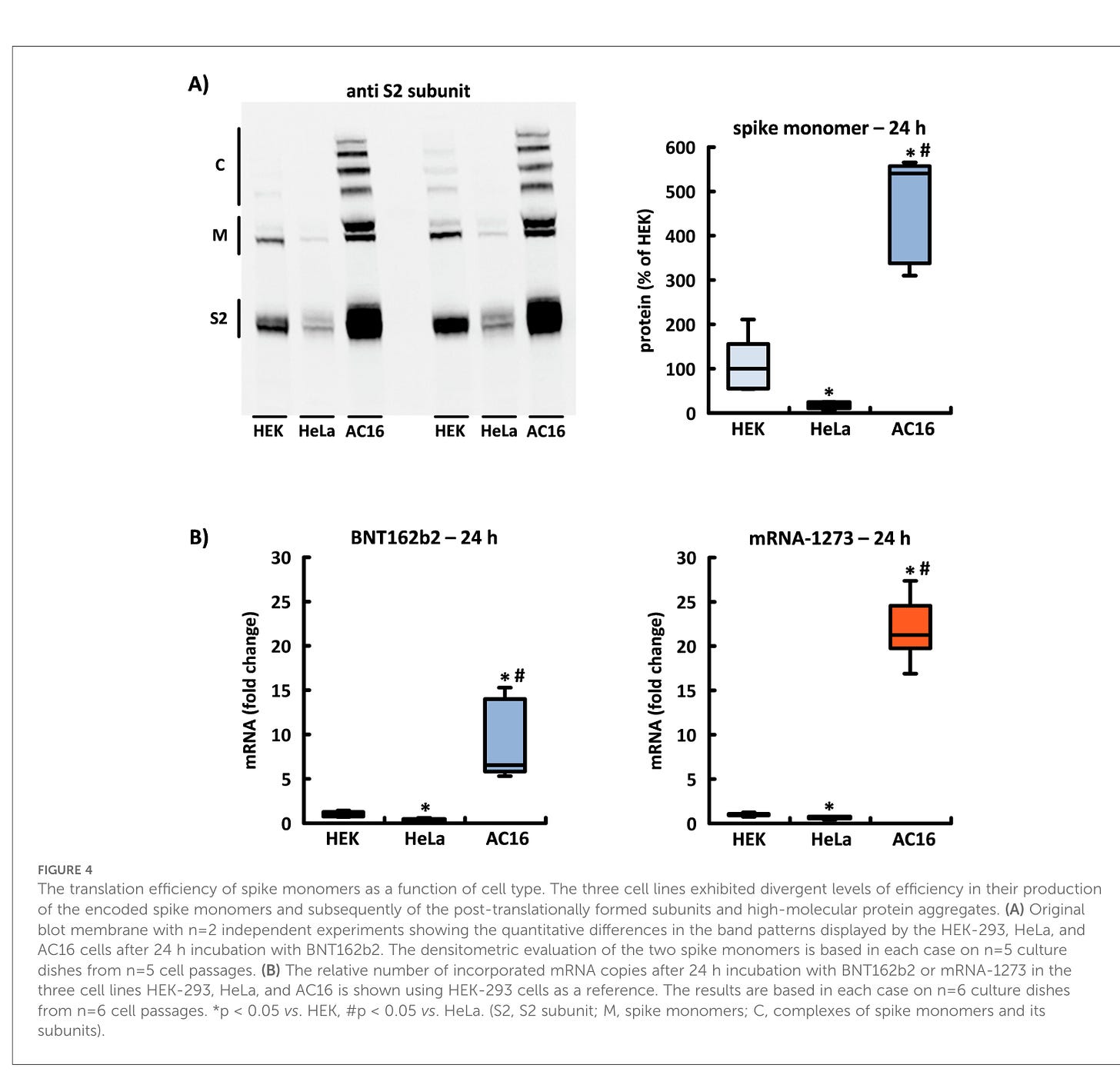
Nach der Anwendung von BNT162b2 und mRNA-1273 zeigte die Menge des produzierten Spike-Proteins dramatische Unterschiede in der Translationseffizienz, die in jeder untersuchten Zelllinie erzielt wurde. In AC16-Kardiomyozyten überstieg die Konzentration von Spike-Monomeren und ihren Untereinheiten sowie von hochmolekularen Komplexen zu allen Zeitpunkten die entsprechenden Konzentrationen in HEK-293- und HeLa-Zellen. Von den beiden zu Vergleichszwecken untersuchten Zelllinien wiesen die HEK-293-Zellen ein Bandenmuster mit höherer Intensität auf (siehe Abbildung 4A).
Die Translationseffizienz von Spike-Monomeren als Funktion des Zelltyps. Die drei Zelllinien zeigten unterschiedliche Effizienzgrade bei der Produktion der kodierten Spike-Monomere und anschließend der posttranslational gebildeten Untereinheiten und hochmolekularen Proteinaggregate. (A) Original-Blot-Membran mit n = 2 unabhängigen Experimenten, die die quantitativen Unterschiede in den Bandenmustern zeigen, die von den HEK-293-, HeLa- und AC16-Zellen nach 24-stündiger Inkubation mit BNT162b2 angezeigt werden. Die densitometrische Auswertung der beiden Spike-Monomere basiert in jedem Fall auf n = 5 Kulturplatten aus n = 5 Zellpassagen. (B) Die relative Anzahl der eingebauten mRNA-Kopien nach 24-stündiger Inkubation mit BNT162b2 oder mRNA-1273 in den drei Zelllinien HEK-293, HeLa und AC16 wird unter Verwendung von HEK-293-Zellen als Referenz dargestellt. Die Ergebnisse basieren jeweils auf n=6 Kulturplatten aus n=6 Zellpassagen. *p < 0,05 vs. HEK, #p < 0,05 vs. HeLa. (S2, S2-Untereinheit; M, Spike-Monomere; C, Komplexe aus Spike-Monomeren und ihren Untereinheiten).
Das heißt, dass auch die verschiedenen Körperzellen im menschlichen Körper diese Unterschiede aufweisen könnten. Das Zellen sich je nach Organ unterschiedlich verhalten ist weder neu noch überraschend. Das sage ich schon seit Jahren. Es könnte sogar sein, dass unterschiedliche Zelltypen, wie bei der Seidenraupe, leicht unterschiedliche Codon-usage haben.
Die proinflammatorischen Eigenschaften des Spike-Proteins
Um zu schauen, ob erhöhte Entzündungswerte auf das Spike-Protein oder generell darauf zurückzuführen sind, dass ein körperfremdes Eiweiß von der Zelle hergestellt wurde, hat man die Zellen die Glühwürmchen-Luciferase (firefly luciferase) zum Vergleich zum Spike-Protein herstellen lassen.
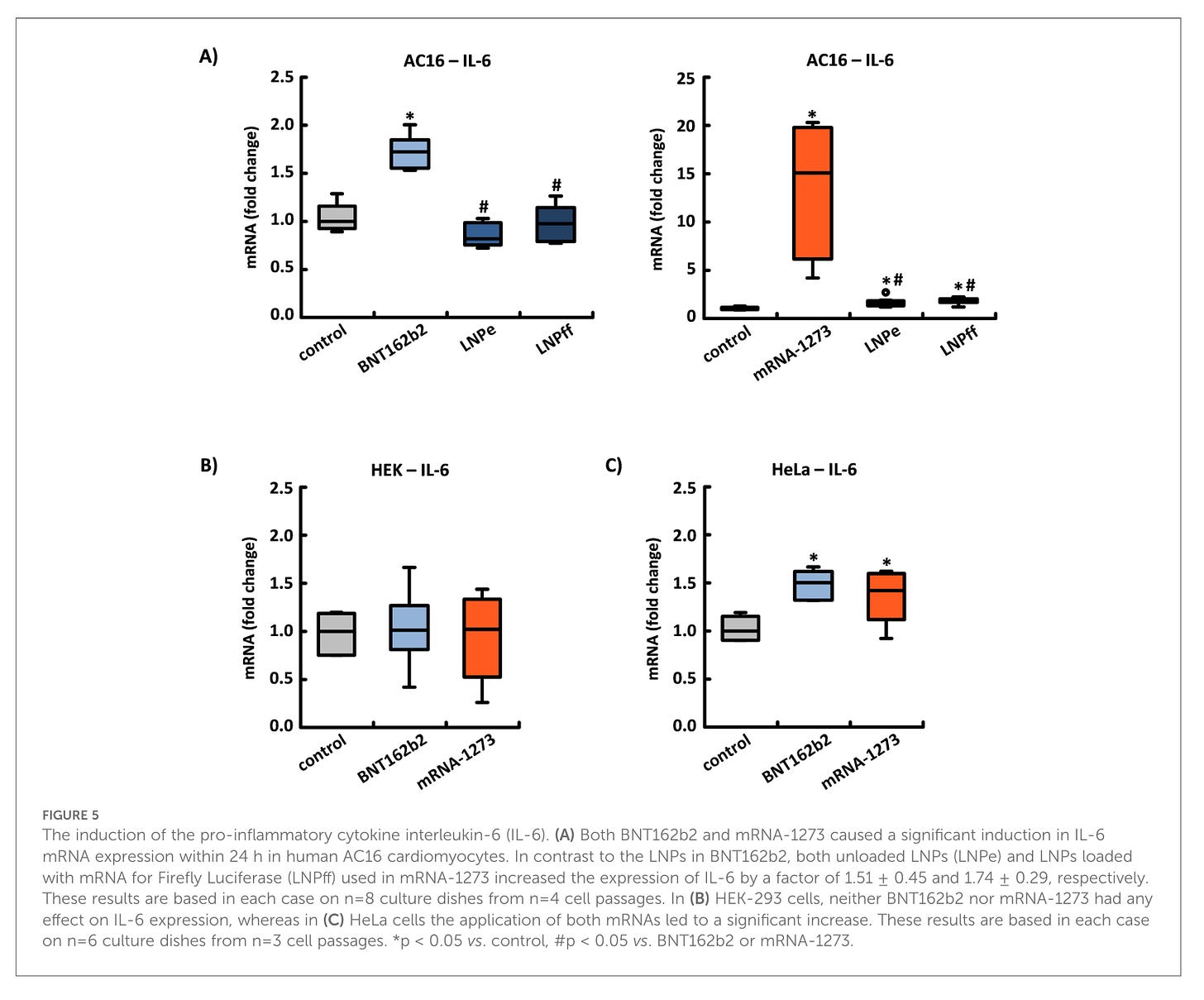
Die Induktion des proinflammatorischen Zytokins Interleukin-6 (IL-6). (A) Sowohl BNT162b2 als auch mRNA-1273 verursachten innerhalb von 24 Stunden eine signifikante Induktion der IL-6-mRNA-Expression in menschlichen AC16-Kardiomyozyten. Im Gegensatz zu den LNPs in BNT162b2 erhöhten sowohl unbeladene LNPs (LNPe) als auch mit mRNA für Firefly-Luciferase (LNPff) beladene LNPs, die in mRNA-1273 verwendet wurden, die Expression von IL-6 um den Faktor 1,51 ± 0,45 bzw. 1,74 ± 0,29. Diese Ergebnisse basieren in jedem Fall auf n = 8 Kulturplatten aus n = 4 Zellpassagen. In (B) HEK-293-Zellen hatten weder BNT162b2 noch mRNA-1273 einen Einfluss auf die IL-6-Expression, während in (C) HeLa-Zellen die Anwendung beider mRNAs zu einem signifikanten Anstieg führte. Diese Ergebnisse basieren in jedem Fall auf n = 6 Kulturplatten aus n = 3 Zellpassagen. *p < 0,05 vs. Kontrolle, #p < 0,05 vs. BNT162b2 oder mRNA-1273.
Auch der Anstieg von IL-6 ist Zelltypabhängig. In AC16 und HeLa Zellen stieg IL-6 an, in HEK-293 Zellen nicht. mRNA-1273 war in AC16 Zellen sowohl leer als auch beladen inflammatorisch, d.h. IL-6 stieg an. Bei Moderna ist das Lipid selbst bereits inflammatorisch, was auch im Moderna eigenen Review so bestätigt wird.
Der Einfluss von BNT162b2 und mRNA-1273 auf die Superoxidproduktion
Es wurde bereits gezeigt, dass das Spike-Protein des SARS-CoV-2-Virus in verschiedenen Zelltypen direkt die Produktion von ROS induziert. Wir untersuchten den Einfluss von BNT162b2 und mRNA-1273 auf den Grad des oxidativen Stresses in AC16-, HEK-293- und HeLa-Zellen unter Verwendung der Superoxid-Indikatoren DHE und MitoSOX.
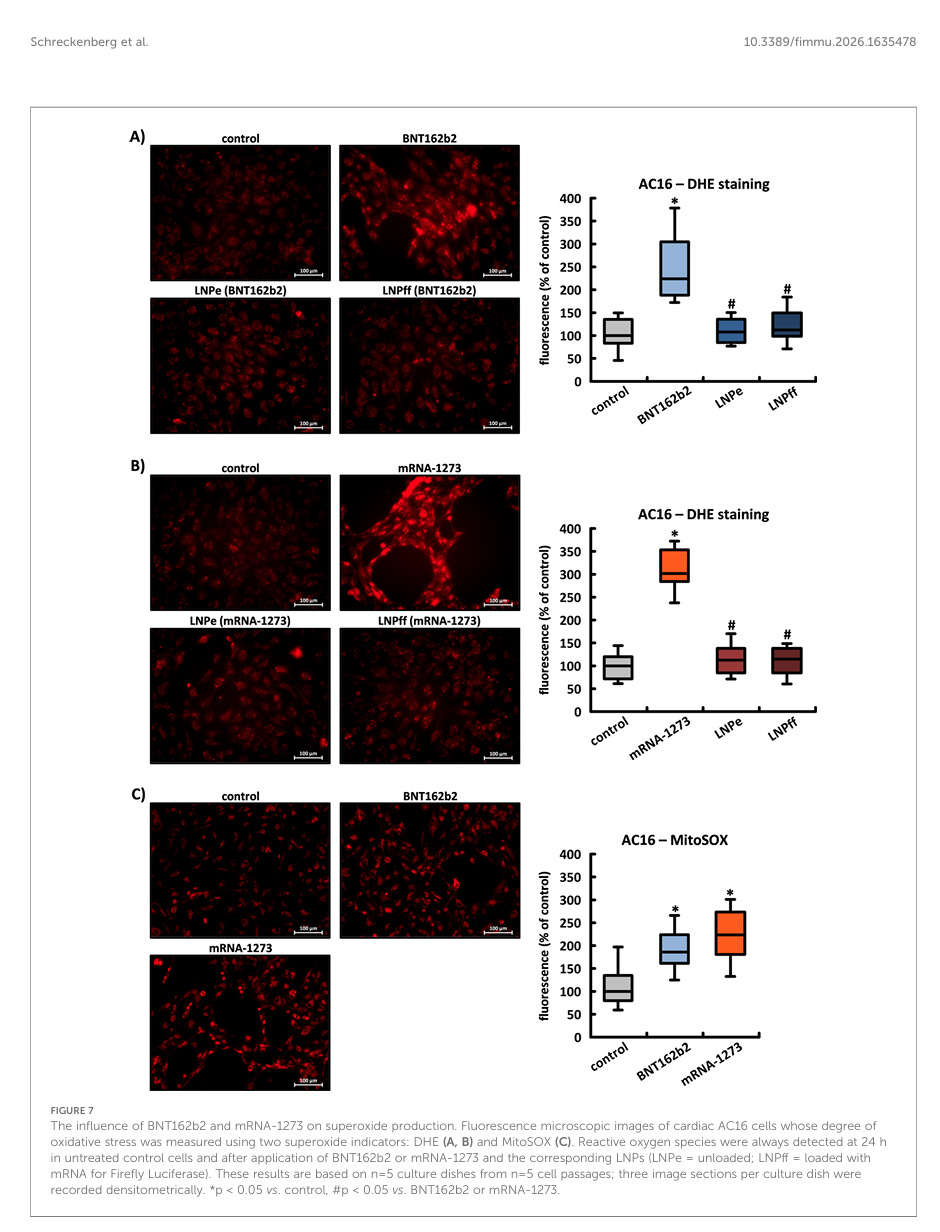
Der Einfluss von BNT162b2 und mRNA-1273 auf die Superoxidproduktion. Fluoreszenzmikroskopische Aufnahmen von kardialen AC16-Zellen, deren oxidativer Stress mit zwei Superoxid-Indikatoren gemessen wurde: DHE (A, B) und MitoSOX (C). Reaktive Sauerstoffspezies wurden immer nach 24 Stunden in unbehandelten Kontrollzellen und nach Anwendung von BNT162b2 oder mRNA-1273 und den entsprechenden LNPs (LNPe = unbeladen; LNPff = beladen mit mRNA für Firefly-Luciferase) nachgewiesen. Diese Ergebnisse basieren auf n = 5 Kulturplatten aus n = 5 Zellpassagen; drei Bildausschnitte pro Kulturplatte wurden densitometrisch aufgezeichnet. *p < 0,05 vs. Kontrolle, #p < 0,05 vs. BNT162b2 oder mRNA-1273.
Weder unbeladene noch mit Firefly-mRNA beladene LNPs beeinflussten die Intensität des DHE-Signals. Nach Inkubation der Zellen mit MitoSOX, dessen Eigenschaften speziell den Nachweis von ROS in Mitochondrien ermöglichen, stieg die Signalstärke um den Faktor 1,86 (± 0,39) bzw. 2,24 (± 0,50) (siehe Abbildungen 7A–C).
Die LNPs ans sich führen nicht zu reaktiven Sauerstoffspezies (ROS) und auch die Glühwürmchen-Luciferase stresst die Zellen nicht.
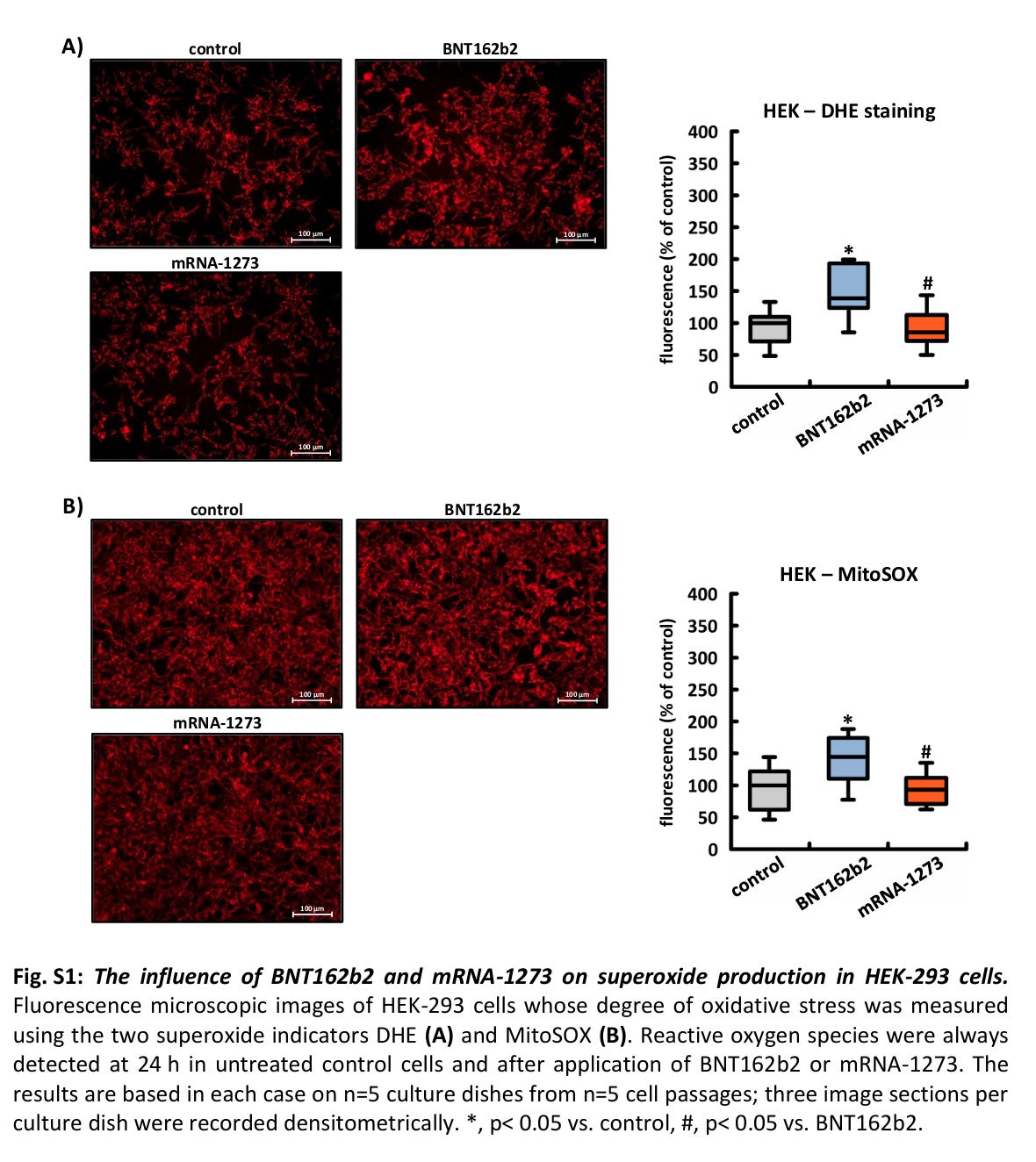
In HEK-Zellen induzierte nur BNT162b2 innerhalb von 24 Stunden die Produktion von Superoxid, das sowohl mit DHE als auch mit MitoSOX nachgewiesen werden konnte (siehe ergänzende Abbildungen S1A, B). In HeLa-Zellen beeinflussten weder BNT162b2 noch mRNA-1273 die Signalstärke eines der beiden Indikatoren während desselben Zeitraums (siehe ergänzende Abbildungen S2A, B).
Abb. S1: Der Einfluss von BNT162b2 und mRNA-1273 auf die Superoxidproduktion in HEK-293-Zellen. Fluoreszenzmikroskopische Aufnahmen von HEK-293-Zellen, deren oxidativer Stress mit den beiden Superoxid-Indikatoren DHE (A) und MitoSOX (B) gemessen wurde. Reaktive Sauerstoffspezies wurden immer nach 24 Stunden in unbehandelten Kontrollzellen und nach Anwendung von BNT162b2 oder mRNA-1273 nachgewiesen. Die Ergebnisse basieren jeweils auf n=5 Kulturplatten aus n=5 Zellpassagen; drei Bildausschnitte pro Kulturplatte wurden densitometrisch erfasst. *, p< 0,05 vs. Kontrolle, #, p< 0,05 vs. BNT162b2.
Auswirkungen der Spike-Protein-Produktion auf die Zellmorphologie von AC16-, HEK-293- und HeLa-Zellen
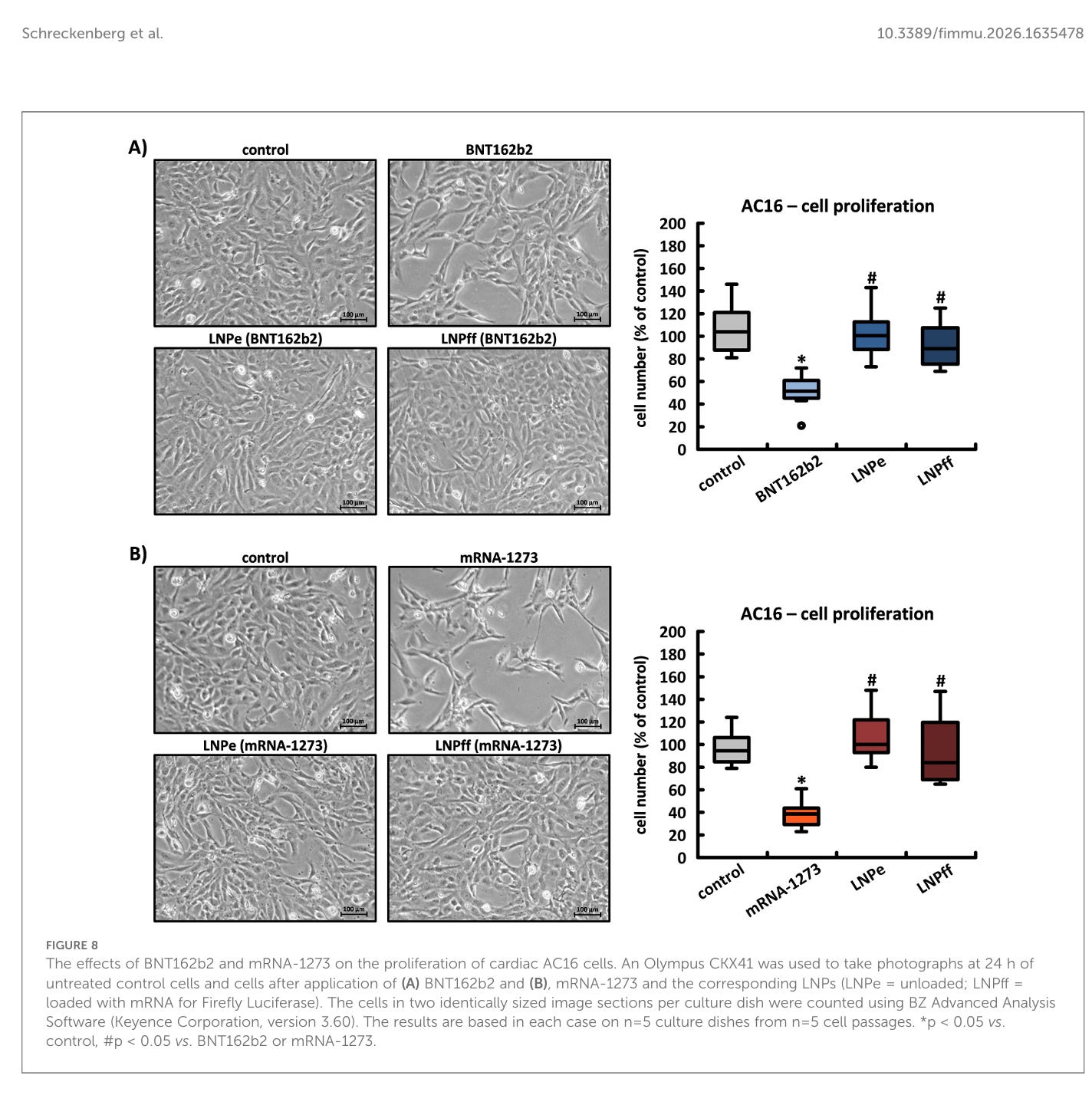
Die intrazelluläre Produktion des Spike-Proteins, nicht jedoch die LNPs oder die RNA an sich, hatte dramatische Auswirkungen auf die Zellmorphologie in AC16-Kulturen, was besonders innerhalb der ersten 24 Stunden bei relativ geringer Zelldichte auffällig war; mit einer Verzögerung von etwa 36 Stunden im Vergleich zu unbehandelten Kontrollen erreichten nur die mit BNT162b2 inkubierten Zellen eine 100-prozentige Konfluenz. Entsprechend der höheren Syntheserate des Spike-Proteins und seiner Aggregate zeigte mRNA-1273 eine deutlich stärkere Ausprägung der beschriebenen Eigenschaften. Unbeladene und mit Firefly-mRNA beladene LNPs verursachten keine morphologischen Anomalien und hatten keinen Einfluss auf die Zellteilung in AC16-Kardiomyozyten (siehe Abbildungen 8A, B).
Das Problem ist also eindeutig das Spike-Protein, welches die Zellen schädigt und das scheint mengenabhängig. Je mehr Spike-Protein, desto mehr Schaden.
Die Auswirkungen von BNT162b2 und mRNA-1273 auf die Proliferation von kardialen AC16-Zellen. Mit einem Olympus CKX41 wurden nach 24 Stunden Fotos von unbehandelten Kontrollzellen und Zellen nach Anwendung von (A) BNT162b2 und (B) mRNA-1273 und den entsprechenden LNPs (LNPe = unbeladen; LNPff = beladen mit mRNA für Firefly-Luciferase) aufgenommen. Die Zellen in zwei identisch großen Bildausschnitten pro Kulturplatte wurden mit der BZ Advanced Analysis Software (Keyence Corporation, Version 3.60) gezählt. Die Ergebnisse basieren jeweils auf n = 5 Kulturplatten aus n = 5 Zellpassagen. *p < 0,05 vs. Kontrolle, #p < 0,05 vs. BNT162b2 oder mRNA-1273.
Sekretion des Spike-Proteins als Voraussetzung für die Immunantwort
Sekretion, also das Ausscheiden der Spike-Proteine war eigentlich nicht als teils der Immunantwort von den Medien angepriesen. Das Spike-Protein sollte eigentlich in der Membran verankert bleiben und gut. Es sollte nicht frei im Überstand/Blut herumschwimmen und Schaden anrichten.
Die „Überstände“ aller drei Zelllinien wurden nach 24 Stunden Inkubation auf Sekretionsprodukte analysiert, die durch BNT162b2 und mRNA-1273 nach der Translation der Spike-Monomere induziert wurden. Das intrazelluläre Bandenmuster jedes Zelltyps wurde mit dem des entsprechenden Überstands verglichen. Von den zahlreichen Spike-Monomer-Derivaten, die im Zelllysat nachgewiesen werden konnten, war nur die S1-Untereinheit im Überstand aller drei Zelllinien nachweisbar (in einigen Fällen als Doppelbanden).
Ähm, halt mal, wenn nur S1, also der Kopf des Brokkoli im Überstand/Blut zu finden ist, was genau bringt dann das Prolinschloss, welches das Spike-Protein entschärfen sollte? Das Prolinschloss ist am unteren Ende von S2 angebracht.
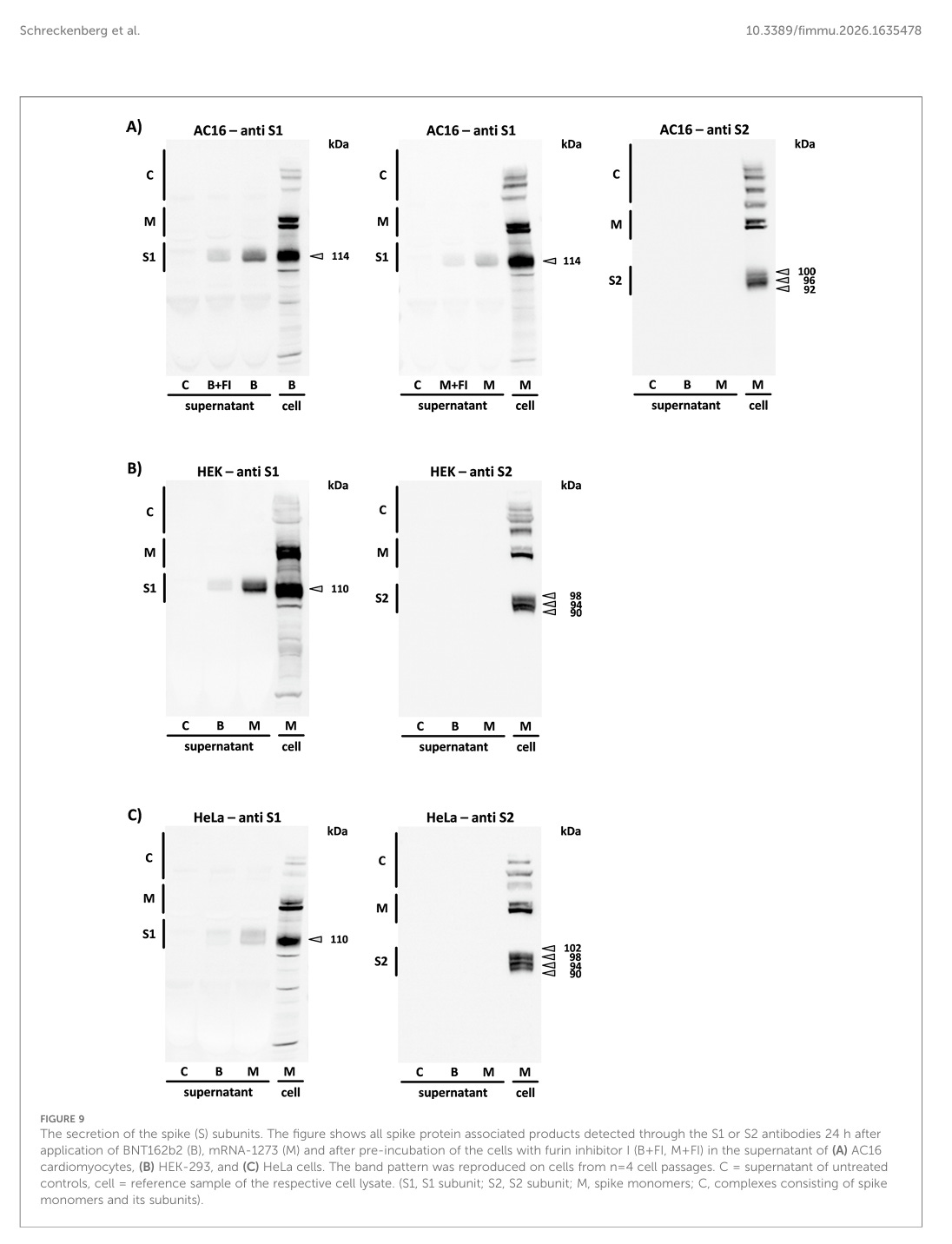
Die Sekretion der Spike (S)-Untereinheiten. Die Abbildung zeigt alle Spike-Protein-assoziierten Produkte, die 24 Stunden nach der Anwendung von BNT162b2 (B), mRNA-1273 (M) und nach Vorinkubation der Zellen mit Furin-Inhibitor I (B+FI, M+FI) im Überstand von (A) AC16-Kardiomyozyten, (B) HEK-293- und (C) HeLa-Zellen. Das Bandenmuster wurde auf Zellen aus n=4 Zellpassagen reproduziert. C = Überstand unbehandelter Kontrollen, Zelle = Referenzprobe des jeweiligen Zelllysats. (S1, S1-Untereinheit; S2, S2-Untereinheit; M, Spike-Monomere; C, Komplexe aus Spike-Monomeren und ihren Untereinheiten).
Nun haben wir bei diesem Versuch noch ein Problem: Das Spike-Protein wird gerne in und auf Exosomen/extrazellulären Vesikeln gefunden. Diese wurden aber nicht getestet oder sind die im Überstand mit dabei?
Was passiert, wenn man zwei verschiedene Spike-Proteine gleichzeitig in einer Zelle exprimiert?
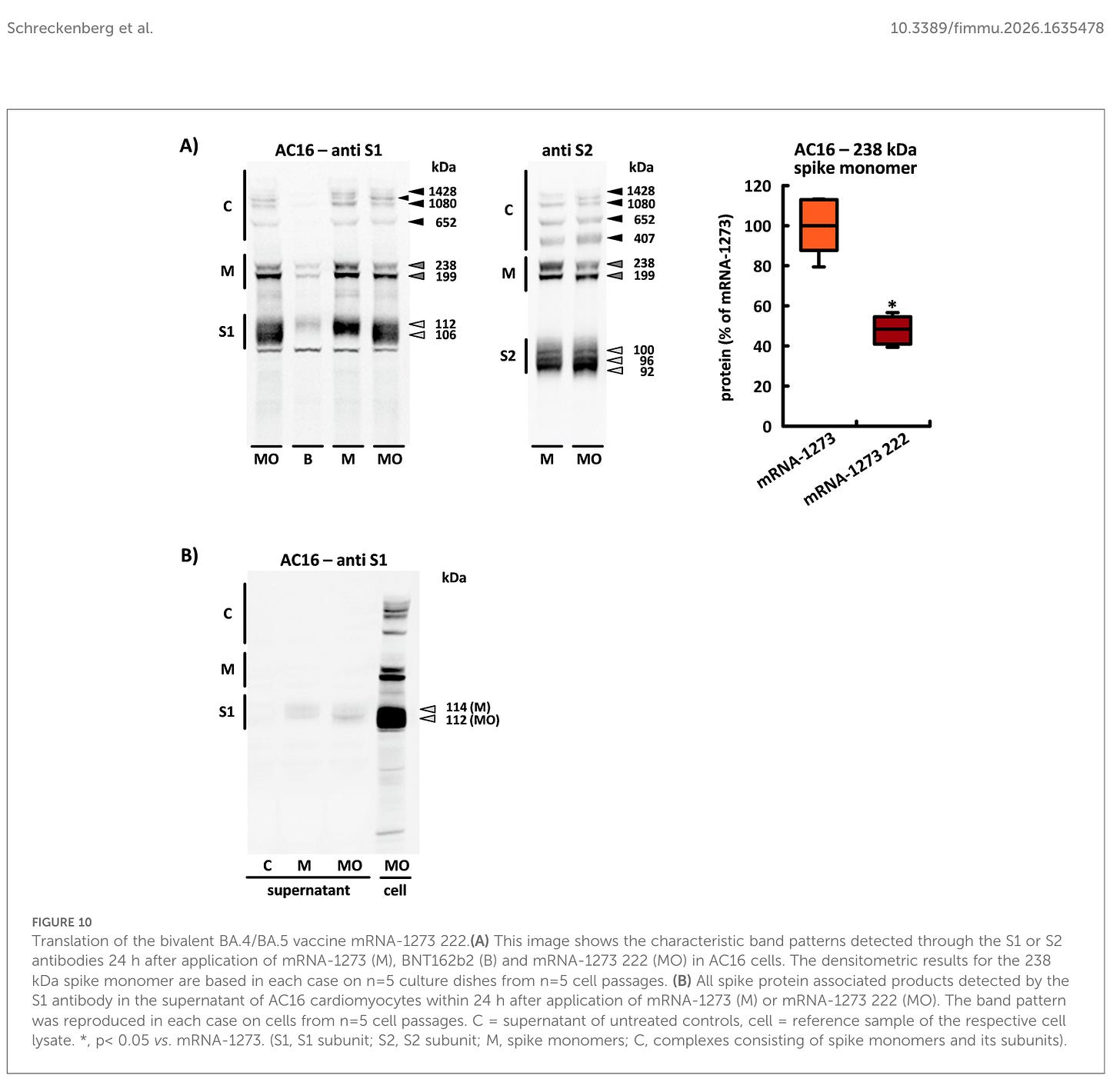
Der bivalente Impfstoff produzierte ebenfalls zwei Spike-Monomere mit identischem Molekulargewicht, jedoch wies das Produkt mit höherem Molekulargewicht eine deutlich geringere Intensität auf (0,48 ± 0,06). Darüber hinaus induzierte mRNA-1273–222 die Bildung von zwei unterschiedlich großen S1-Untereinheiten: Die Bande mit dem höheren Molekulargewicht (das etwa 112 kDa betrug) hatte ein etwas geringeres Molekulargewicht als die S1-Untereinheit des monovalenten Impfstoffs; eine zweite S1-Untereinheit wurde mit einem deutlich reduzierten Molekulargewicht von etwa 106 kDa nachgewiesen. Zwischen den drei S2-Untereinheiten gab es keine Unterschiede. Im Überstand fanden wir jedoch nur die S1-Untereinheit mit höherem Molekulargewicht, die im Vergleich zur sekretierten Untereinheit des monovalenten Impfstoffs auch extrazellulär ein niedrigeres Molekulargewicht aufwies (siehe Abbildungen 10A, B).
Übersetzung des bivalenten BA.4/BA.5-Impfstoffs mRNA-1273 222.(A) Dieses Bild zeigt die charakteristischen Bandenmuster, die 24 Stunden nach der Anwendung von mRNA-1273 (M), BNT162b2 (B) und mRNA-1273 222 (MO) in AC16-Zellen durch die S1- oder S2-Antikörper nachgewiesen wurden. Die densitometrischen Ergebnisse für das 238 kDa Spike-Monomer basieren jeweils auf n=5 Kulturplatten aus n=5 Zellpassagen. (B) Alle Spike-Protein-assoziierten Produkte, die durch den S1-Antikörper im Überstand von AC16-Kardiomyozyten innerhalb von 24 Stunden nach Anwendung von mRNA-1273 (M) oder mRNA-1273 222 (MO) nachgewiesen wurden. Das Bandenmuster wurde in jedem Fall an Zellen aus n=5 Zellpassagen reproduziert. C = Überstand unbehandelter Kontrollen, Zelle = Referenzprobe des jeweiligen Zelllysats. *, p< 0,05 vs. mRNA-1273. (S1, S1-Untereinheit; S2, S2-Untereinheit; M, Spike-Monomere; C, Komplexe aus Spike-Monomeren und ihren Untereinheiten).
Erneut nur S1 Untereinheiten im Überstand und in der Zelle diverse Komplexe, die was auch immer verursachen.
Fazit
Unsere Analysen zeigen, dass die posttranslationale Verarbeitung der kodierten Spike-Monomere wesentlich komplexer ist als bisher angenommen. In unseren Experimenten haben wir unabhängig vom Zelltyp durchweg zwei Translationsprodukte unterschiedlicher Größe nachgewiesen. Diese Beobachtung lässt sich durch das Vorhandensein von zwei potenziellen Initiationsstellen für die Translation erklären. Diese Komplexität ist besonders relevant im Zusammenhang mit mRNA-basierten Impfstoffen, bei denen die Regulation der Translation, Verarbeitung und Sekretion vollständig von den Eigenschaften der transfizierten Wirtszellen bestimmt wird. Unsere Daten bestätigen diese ausgeprägte Zelltypabhängigkeit und deuten darauf hin, dass die resultierenden Derivate, einschließlich nicht sekretierter Spaltprodukte und kovalent gebundener Komplexe, funktionell relevante Auswirkungen auf die Morphologie, Proliferation und zellulären Stressreaktionen haben.
Man hat also herausgefunden, dass die Proteinproduktion doch komplexer ist als gedacht, dass konstant mehr Produkte herauskommen sollten als geplant und man nicht weiß, was das verursachen könnte und bestätigt, dass das Produkt vom jeweiligen Zelltyp abhängt. Wie gut, dass er Mensch so viele verschiedene Zelltypen hat, da kommt irgendwo sicherlich das geplante Spike-Protein dabei heraus und der andere Schrott, wenn schert’s.
Derzeit können wir nur Spekulationen über die Stabilität und Halbwertszeit der Spike-Proteine und ihrer hochmolekularen Komplexe sowie über die damit verbundenen Auswirkungen auf die Lebensfähigkeit und Funktion verschiedener Körperzellen anstellen, wobei besonderes Augenmerk auf irreversible postmitotische Zelltypen wie Neuronen und Kardiomyozyten zu richten ist, die aufgrund ihrer begrenzten Regenerationsfähigkeit möglicherweise einer genaueren Untersuchung bedürfen. Neuropathologische Studien an SARS-CoV-2-Patienten haben eine Gliazellenaktivierung, Neuroinflammation und mikrovaskuläre Veränderungen dokumentiert, die zu anhaltenden neurologischen Symptomen lange nach Abklingen der akuten Infektionsphase beitragen können (32–34). Ob intrazellulär exprimierte Spike-Proteine zu diesen Mechanismen beitragen können, ist noch unbekannt, verdient jedoch weitere Untersuchungen, insbesondere im Zusammenhang mit irreversiblen postmitotischen Zelltypen. Diese Annahme wird durch die Tatsache gestützt, dass Spike-abgeleitete hochmolekulare Aggregate auch in U343-Zellen nachgewiesen wurden, die astrozytäre Eigenschaften aufweisen (siehe Ergänzende Abbildung S4).
Diese schweren Aggregate verschiedener Spikes oder Spike-Teile könnten echt schlecht für das Nervensystem sein und auch besonders für jene Zellen, die eigentlich ein Leben lang halten sollten und im Laufe des Lebens nicht ersetzt werden.
Die Effizienz der Spike-Monomer-Produktion variierte in Abhängigkeit vom Zelltyp und der verwendeten mRNA.
Daher wurde auch kreuzgeimpft, das mittelt sich so sicherlich irgendwie wieder raus.
Obwohl quantitative Daten zur Myokardaufnahme, Biodistribution und Spike-Protein-Expression nach mRNA-Impfung beim Menschen nach wie vor begrenzt sind, deuten unsere Ergebnisse darauf hin, dass bereits geringe Konzentrationen von LNPs, die das Myokard erreichen, ausreichen können, um eine Myokarditis auszulösen, die histopathologisch als atypisch nach COVID-19-mRNA-Impfung klassifiziert wurde (41).
[…] Angesichts der einzigartigen elektrophysiologischen und strukturellen Eigenschaften des Herzgewebes können selbst kleine fokale Läsionen innerhalb des Myokards unverhältnismäßig große funktionelle Auswirkungen haben. Solche Läsionen können die elektrische Leitfähigkeit stören oder die neuronale Innervation des Herzens verändern, was möglicherweise zu subklinischen oder klinischen Manifestationen führen kann (43–45).
Nun muss der übliche entschuldigende Satz rein, damit man durch die Zensur kommt.
Während das Risiko für kardiovaskuläre Komplikationen nach einer SARS-CoV-2-Infektion in der Allgemeinbevölkerung weiterhin deutlich höher ist, verdient das seltene Auftreten von Myokarditis nach einer mRNA-basierten COVID-19-Impfung weiterhin große Aufmerksamkeit.
Das Spannende an diesem Satz ist jedoch: ER HAT KEINE ZITATION, KEINEN BELEG FÜR DIE BEHAUPTUNG!!!
Wenn das so stimmen würde, wäre es doch nicht schwer gewesen, diesen Satz mit einer Studie zu belegen? So steht er als unbelegte Behauptung im Text. Als Reviewer hätte ich an dieser Stelle Quellenverweise verlangt.
Unsere Ergebnisse deuten darauf hin, dass die beobachteten Nebenwirkungen eine Entzündungsreaktion auf die Spike-Protein-bezogenen Produkte sind, die innerhalb der Zelle gebildet werden.
In allen drei Zelllinien konnte nur die S1-Untereinheit im Überstand nachgewiesen werden. Die Immunantwort richtet sich daher höchstwahrscheinlich in erster Linie gegen die Untereinheit, deren N-Terminus die Rezeptorbindungsdomäne (RBD) enthält, während die membranverankerte S2-Untereinheit möglicherweise weiterhin zur Antigenpräsentation und zellulären Immunaktivierung beiträgt. Unsere Ergebnisse stimmen jedoch mit den Befunden von Wheeler et al. überein, die nach mRNA-basierten Corona-Impfungen fast ausschließlich Antikörper gegen Epitope der RBD oder der S1-Untereinheit nachweisen konnten, nicht jedoch gegen die S2-Untereinheit.
Wenn nur die RBD im Blut ist, warum hat man das ganze Spike-Protein kodiert?
Furin, eine Endoprotease aus der Familie der Proproteinkonvertasen, katalysiert in erster Linie die proteolytische Reifung von Vorläuferproteinen im eukaryotischen Proteinsekretionsweg im trans-Golgi-Netzwerk (TGN) (67). Nach der Translation der kodierten Spike-Monomere und ihrer Aufnahme in das endoplasmatische Retikulum (ER) werden die beiden S-Untereinheiten im Golgi-Komplex (GC) oder im TGN proteolytisch gebildet, von wo aus nur die S1-Untereinheit sekretiert wird. Die genauen Mechanismen, durch die das Schicksal der Proteine im TGN bestimmt wird, sind noch weitgehend unbekannt (68).
Man lässt die Zelle ein Protein produzieren, ohne verstanden zu haben wie die Proteinverarbeitung im Trans-Golgi-Netzwerk funktioniert. Man weiß also nicht, was letztendlich im Körper kursiert.
Auf ihrem Weg vom ER zum TGN durchlaufen Proteine einen sorgfältigen Verarbeitungsprozess, um eine ordnungsgemäße Synthese, korrekte Faltung und fehlerfreie Assemblierung sicherzustellen. Es wurden verschiedene Ursachen für die Bildung von Proteinaggregaten im ER und GC identifiziert. Wenn kovalent gebundene Spike-Proteinkomplexe nicht effizient entfernt werden, können sie sich im ER ansammeln und zu toxischen Proteinaggregaten führen, die Zell- und Gewebeschäden verursachen können (69, 70).
Dieser Artikel geht ganz natürlich davon aus, dass das Spike-Protein nicht in freien Ribosomen im Zelllumen hergestellt wird sondern im Endoplasmatischen Retikulum, was auch korrekt ist. Ob das den Lesern auffällt?
Unsere Ergebnisse deuten insgesamt darauf hin, dass die intrazelluläre Akkumulation verschiedener Spike-Protein-Derivate zu potenziell proteotoxischen Folgen führen kann. Bemerkenswert ist, dass die Vorbehandlung mit einem Furin-Inhibitor die Bildung größerer S1/S2-Komplexe unterdrückt, gleichzeitig aber die Aggregation von unverarbeiteten Monomeren fördert (siehe Abbildung 2).
Ich sage nur: Inclusion bodies, das habe ich schon vor Jahren geschrieben. Fehlgefaltete Proteine werden als Einschlußkörperchen in dunklen Ecken der Zelle entsorgt.
Dies deutet darauf hin, dass die intrazelluläre Anreicherung von Spike-Proteinen Entzündungswege aktivieren kann, möglicherweise über ER-Stress und die Unfolded Protein Response (UPR).
Im Gegensatz zur intrazellulären Translation und Verarbeitung von mRNA-abgeleiteten Spike-Proteinen, die zu Off-Target-Effekten, intrazellulärer Akkumulation und Aggregation führen können, vermeidet der proteinbasierte Ansatz von Nuvaxovid diese Risiken vollständig. Unsere Ergebnisse unterstreichen, dass nicht nur das Spike-Protein selbst, sondern auch seine intrazelluläre Produktion und posttranslationale Verarbeitung zu den ausgeprägten zellulären Stressreaktionen beitragen, die nach einer mRNA-Impfung beobachtet werden.
Das Problem bei dieser Argumentation ist jedoch, dass auch Nuvaxovid eine Myokarditiswarnung (Black Box Warnung) bekommen hat. Selbst das korrekt gefaltete, komplette Spike-Protein, welches von den Zellen nicht selbst produziert wird, macht Myokarditis. Da hätte ich als Reviewer auch reingegrätscht.
Die Schlussfolgerung der Autoren ist für einen wissenschaftlichen Artikel in einer Mainstream Wissenschaftszeitschrift schon SEHR direkt, direkter als man es früher gewagt hat:
Das Risikoprofil einer mRNA-induzierten Immunisierung lässt sich derzeit nicht allgemein definieren, da die derzeit verwendeten nicht-zelltypspezifischen LNPs nach der Injektion auch entfernte Zellen erreichen können und die Art und das Ausmaß möglicher Nebenwirkungen von den transfizierten Zelltypen und den Eigenschaften des Immunogens abhängen.
Treffer. Versenkt.
Wie kann man Risiko:Nutzen berechnen, wenn das Risikoprofil nicht bestimmbar ist?
Angesichts der außergewöhnlich hohen Sicherheitsstandards, die für Impfstoffe gelten, ist ein genaues Verständnis der intrazellulären Verarbeitung kodierter Proteine und ihrer potenziellen Auswirkungen auf zelluläre physiologische Parameter für mRNA-basierte Anwendungen unerlässlich, bevor diese in die klinische Anwendung übergehen.
Das Problem ist: Sie sind bereits in klinischer Anwendung. Hier steht kodiert, dass sie nie hätten auf den Markt kommen dürfen.
Was die Autoren nicht adressieren (Danke an Geoff):
In ihren Studien, die sich auf zellfreie Systeme stützen, zeigen sowohl Petruk et al. als auch Petrlova et al., dass das Spike-Protein von SARS-CoV-2 in Gegenwart von LPS hochmolekulare Aggregate bilden kann.
Geoff meint, dass Endotoxin von 85°C nicht beeinträchtigt wird. Wenn dem so ist, würde das bedeuten, dass die Mulitmere auf Verunreinigungen durch Lipopolysaccharide (LPS) = Endotoxine zurückzuführen wären, die in den Produkten enthalten sind. Das wäre auch in der klinischen Anwendung ein Problem.
Dafür spricht meine eigene Erfahrung, dass normale Proteinmultimere bei 85°C Vorbehandlung auf dem SDS-Gel in Monomere zerfallen müssten. Das ist wirklich extrem auffällig.
Mein Fazit:
Man vergleicht in dieser Publikation BNT162B2 und mRNA-1273 nach Verfahren 2 mit selbst hergestellten Kontrollen nach Verfahren 1. Damit hat man ein zusätzliches Problem mit Endotoxin/LPS Artefakten, die klar in den SDS-Gelen erkennbar sind, weil Multimere bei 85°C zerfallen müssten, es sei denn, man hätte es mit einem extremophilen Protein zu tun und das wäre auch sehr schlecht, weil die gerne kältedenaturieren.
Man kann somit ehrlicherweise nicht sagen, dass Probleme wirklich nur vom Spike-Protein verursacht werden. Es kann die Kombination aus LPS und Spike-Protein sein. Man hätte prüfen müssen, ob das Problem auch mit selbst hergestelltem BNT162B2 und mRNA-1273 nach Verfahren 1 vorhanden sind.
Man hätte überhaupt auf LPS testen müssen, wenn man das Problem schon erwähnt.
Das heißt nicht, dass das Spike-Protein harmlos ist, das heißt jedoch, dass die Autoren eigentlich nicht schließen können, dass die beobachteten Schäden nur durch das Spike-Protein zustande kommen sondern auch durch die Herstellung mit Prozess 2 verursacht oder verschlimmert sein können.
Wie auch immer, die Produkte nach Prozess 2 sind auf dem Markt und verursachen die beobachteten Schäden. Warum das so ist, ist leider auch nach dieser Publikation von Schreckenberg und Co nicht geklärt.
Update:
23.02.2026 Corrigendum: Ich habe es erst falsch verstanden, dass die Autoren auch BNT162B2 und mRNA-1273 selbst nachgebaut haben, weil entsprechende Primer in S1 angegeben waren. Danke an Geoff für die Korrektur.
Streng genommen hätte man diese tatsächlich auch herstellen müssen um einen Vergleich zu haben zu den anderen selbst hergestellten Produkten, weil man sonst Verfahren 1 mit Verfahren 2 vergleicht und nicht zwangsläufig Spike-Protein mit Glühwürmchen-Luciferase. Man hat Glühwürmchen Luciferase nach Verfahren 1 mit Spike-Protein nach Verfahren 2 verglichen und das unter Umständen mit unterschiedlich zusammengesetzten LNPs im Vergleich zum Originalprodukt.
Höhere Nebenwirkungsrate bei ungenauer Zusammensetzung der LNPs?
Bangaru S, Ozorowski G, Turner HL, Antanasijevic A, Huang D, Wang X, Torres JL, Diedrich JK, Tian JH, Portnoff AD, Patel N, Massare MJ, Yates JR 3rd, Nemazee D, Paulson JC, Glenn G, Smith G, Ward AB. Structural analysis of full-length SARS-CoV-2 spike protein from an advanced vaccine candidate. Science. 2020 Nov 27;370(6520):1089-1094. doi: 10.1126/science.abe1502. Epub 2020 Oct 20. PMID: 33082295; PMCID: PMC7857404.https://pubmed.ncbi.nlm.nih.gov/33082295/
Bitounis D, Jacquinet E, Rogers MA, Amiji MM. Strategies to reduce the risks of mRNA drug and vaccine toxicity. Nat Rev Drug Discov. 2024 Jan 23. doi: 10.1038/s41573-023-00859-3. Epub ahead of print. PMID: 38263456. https://pubmed.ncbi.nlm.nih.gov/38263456/