Auf der EMA Webseite findet man einen Vortrag zu mRNA “Impfstoffen” der es in sich hat.
Der “EMA virtual workshop on myocarditis post COVID-19 vaccination” fand am 16 Januar 2023 statt.
Es gab diverse Präsentationen, die man sich mal aus juristischer Sicht durchschauen sollte.
Auf Folie 13 findet man das kleine schmutzige Geheimnis der modRNA-Technologie
Die Produktionsrückstände funktionieren in dieser Technologie vielleicht als beabsichtigte Adjuvantien. Daher muss man diese Produkte immer ein wenig schmutzig halten, weil die doppelsträngige RNA das Immunsystem aktiviert, wie ein Adjuvanz.
Die “Produktionsrückstände” könnten also theoretisch beabsichtig sein und eine funktionelle Rolle in der Lipidtechnologie spielen.
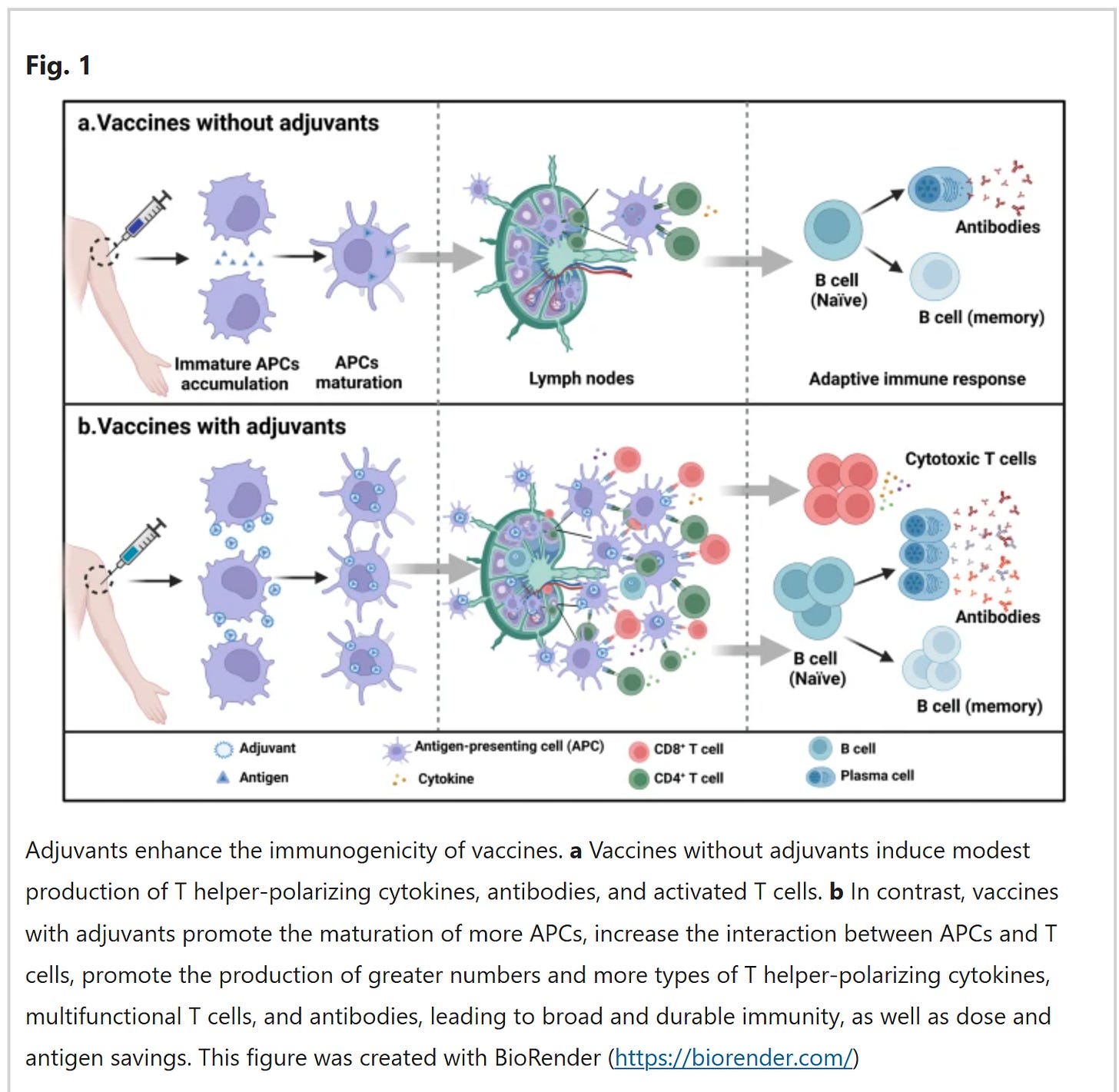
“Adjuvanzien verstärken die Immunogenität von Impfstoffen. a Impfstoffe ohne Adjuvanzien induzieren eine mäßige Produktion von T-Helfer-polarisierenden Zytokinen, Antikörpern und aktivierten T-Zellen. b Im Gegensatz dazu fördern Impfstoffe mit Adjuvanzien die Reifung von mehr APCs, verstärken die Interaktion zwischen APCs und T-Zellen, fördern die Produktion einer größeren Anzahl und mehr Arten von T-Helfer-polarisierenden Zytokinen, multifunktionalen T-Zellen und Antikörpern, was zu einer breiten und dauerhaften Immunität sowie zu Dosis- und Antigenersparnissen führt.”
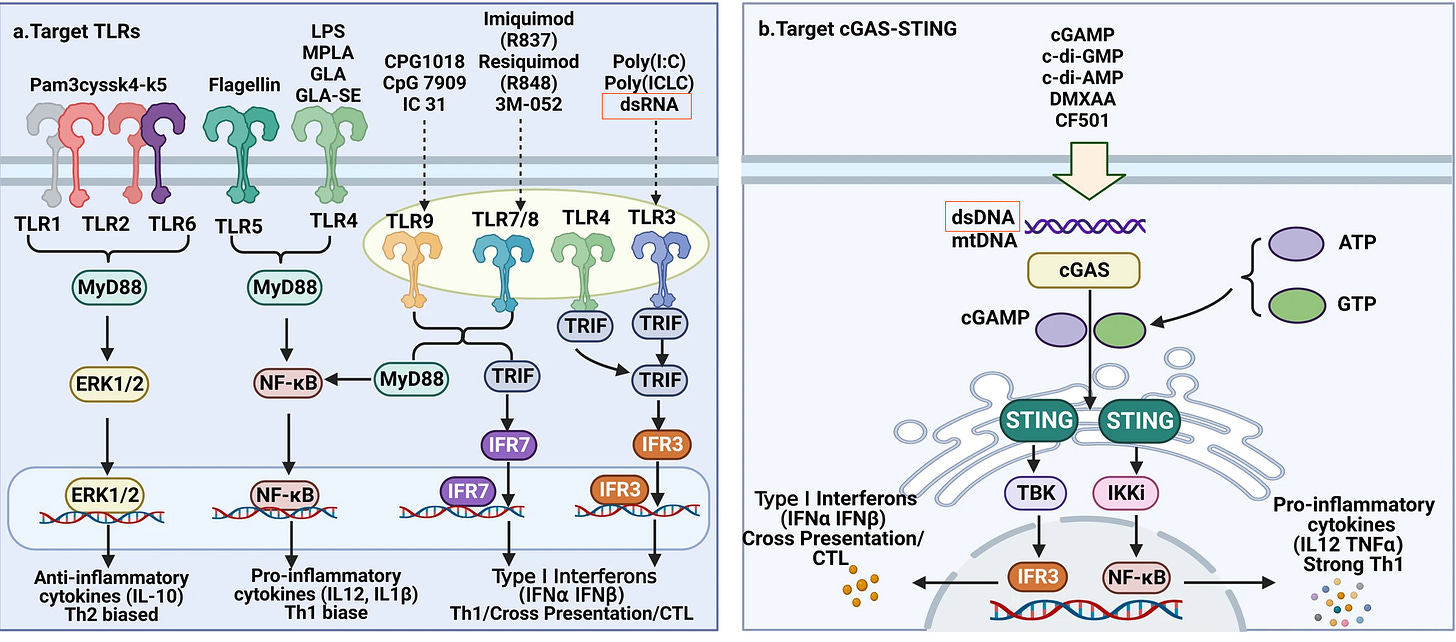
“Vereinfachtes Diagramm von Immunstimulanzien, die adaptive Immunantworten durch Aktivierung von PRRs regulieren. Verschiedene Arten von Immunstimulanzien senden Signale über unterschiedliche PRRs, was zu einer unterschiedlichen Zytokinsekretion führt und dadurch unterschiedliche adaptive Immunantworten induziert. Immunstimulanzien induzieren und modulieren adaptive Immunantworten, indem sie a TLRs, b cGAS-STING”
Aktivierung cGAS-STING macht viele gesundheitliche Probleme und kommt daher in einigen meiner Artikel mit als Schadmechanismus vor.
Was wäre wenn die Produktionsrückstände einen Zweck erfüllen würden und gewünscht wären, also kein Bug sondern ein Feature wären?
Wie reagiert das Immunsystem auf DNA:modRNA-Hybride?
Dazu hat BioNTech eine Hypothese, welche z. Bsp. die Aktivierung des Inflammasoms umfasst:
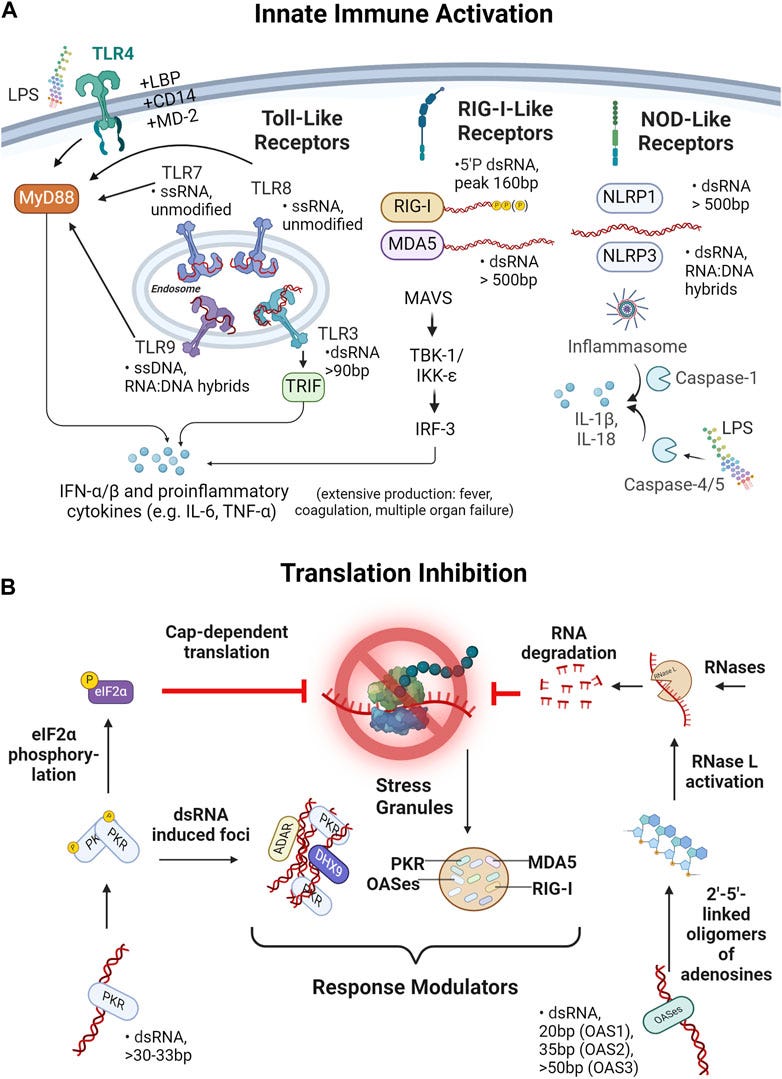
“Abbildung 2. IVT-Reaktionsnebenprodukte und Verunreinigungen und deren Auswirkungen auf transfizierte Zellen. (A) Die Auswirkungen von IVT-Reaktionsnebenprodukten und Verunreinigungen auf die Aktivierung des angeborenen Immunsystems sind dargestellt. Dargestellt sind drei Rezeptorfamilien, nämlich Toll-like-Rezeptoren (TLRs), Retinsäure-induzierbare Gen-I-ähnliche Rezeptoren (RIG-I-ähnliche Rezeptoren) und NOD-ähnliche Rezeptoren (NLRs), von denen bekannt ist, dass sie ssRNA, dsRNA und RNA:DNA-Hybride unterschiedlicher Länge erkennen. Die Aktivierung von TLR4, 7, 8 oder 9 führt über den MyD88-Signalweg und TLR3 über TRIF zur Sekretion von IFN-α/β und proinflammatorischen Zytokinen wie IL-6 oder IFN-γ. Ebenso führen die RIG-I-ähnlichen Rezeptoren MDA5 und RIG-I über MAVS, TBK-1/IKK-ε und IRF-3 zur Sekretion proinflammatorischer Zytokine. Im Gegensatz dazu lösen die NOD-ähnlichen Rezeptoren NLRP1 und NLRP3 die Bildung von Inflammasomen aus und führen über Caspase-1 zur Freisetzung von IL-1β und IL-18. Neben der immunstimulierenden Aktivität von IVT-Nebenprodukten „nuklearer Natur” löst der Nachweis von bakteriellem Lipopolysaccharid (LPS) über TLR4 oder Caspase-4/5 und die anschließende Aktivierung von Inflammasomen die Aktivierung des angeborenen Immunsystems aus. (B) Mechanismen der Translationshemmung durch die Wirkung von dsRNA-Nebenprodukten sind dargestellt. dsRNA kann durch Proteinkinase R (PKR) oder 2′-5′-Oligoadenylatsynthetasen (OASes) erkannt werden. Zwei PKR-Moleküle können bei Bindung an dsRNA autophosphorylieren, wodurch die Phosphorylierung des Transkriptionsinitiationsfaktors eIF2 ermöglicht wird. eIF2 spielt eine zentrale Rolle bei der Initiierung der Translation, sodass die Phosphorylierung von eIF2 die cap-abhängige Translation von RNA hemmt. OASes hingegen wirken durch die Verknüpfung und Oligomerisierung von ATP, was zur Aktivierung von RNase L und damit zum Abbau von ssRNA (d. h. dem Arzneimittel) führt. Sowohl PKR und OASes als auch die RIG-I-ähnlichen Rezeptoren MDA5 und RIG-I sind an der Bildung von dsRNA-induzierten Foci beteiligt, den sogenannten Stressgranula, von denen angenommen wird, dass sie die dsRNA-Sensorik verstärken oder kontrollieren.”
Auch das sieht mir nach einer heftigen Immunreaktion aus, die man euphemistisch vielleicht als Adjuvanzreaktion beschreiben könnte.
EMA virtual workshop on myocarditis post COVID-19 vaccination | European Medicines Agency (EMA). (2023, January 31). European Medicines Agency (EMA). https://www.ema.europa.eu/en/events/ema-virtual-workshop-myocarditis-post-covid-19-vaccination
Zhao T, Cai Y, Jiang Y, He X, Wei Y, Yu Y, Tian X. Vaccine adjuvants: mechanisms and platforms. Signal Transduct Target Ther. 2023 Jul 19;8(1):283. doi: 10.1038/s41392-023-01557-7. PMID: 37468460; PMCID: PMC10356842. https://pubmed.ncbi.nlm.nih.gov/37468460/
Zhao T, Cai Y, Jiang Y, He X, Wei Y, Yu Y, Tian X. Vaccine adjuvants: mechanisms and platforms. Signal Transduct Target Ther. 2023 Jul 19;8(1):283. doi: 10.1038/s41392-023-01557-7. PMID: 37468460; PMCID: PMC10356842. https://pubmed.ncbi.nlm.nih.gov/37468460/
Lenk R, Kleindienst W, Szabó GT, Baiersdörfer M, Boros G, Keller JM, Mahiny AJ, Vlatkovic I. Understanding the impact of in vitro transcription byproducts and contaminants. Front Mol Biosci. 2024 Jul 10;11:1426129. doi: 10.3389/fmolb.2024.1426129. PMID: 39050733; PMCID: PMC11266732. https://pubmed.ncbi.nlm.nih.gov/39050733/