Nicht nur die EMA diskutiert, wie modRNA-LNP-Produkte zu prüfen wären. In USA geht man bereits in die dritte Runde und ein Ende ist nicht abzusehen.
USP Version 2
Kommentare zu den Vorschlägen gibt es teilweise als preprint.
Wahrscheinlich wäre es sinnvoller, wenn sich die EMA in diesem Fall einfach an USP ran hängt, die sind fachlich bereits DEUTLICH weiter.
Es gibt eine PowerPoint Präsentation von USP, über den Stand 2024.
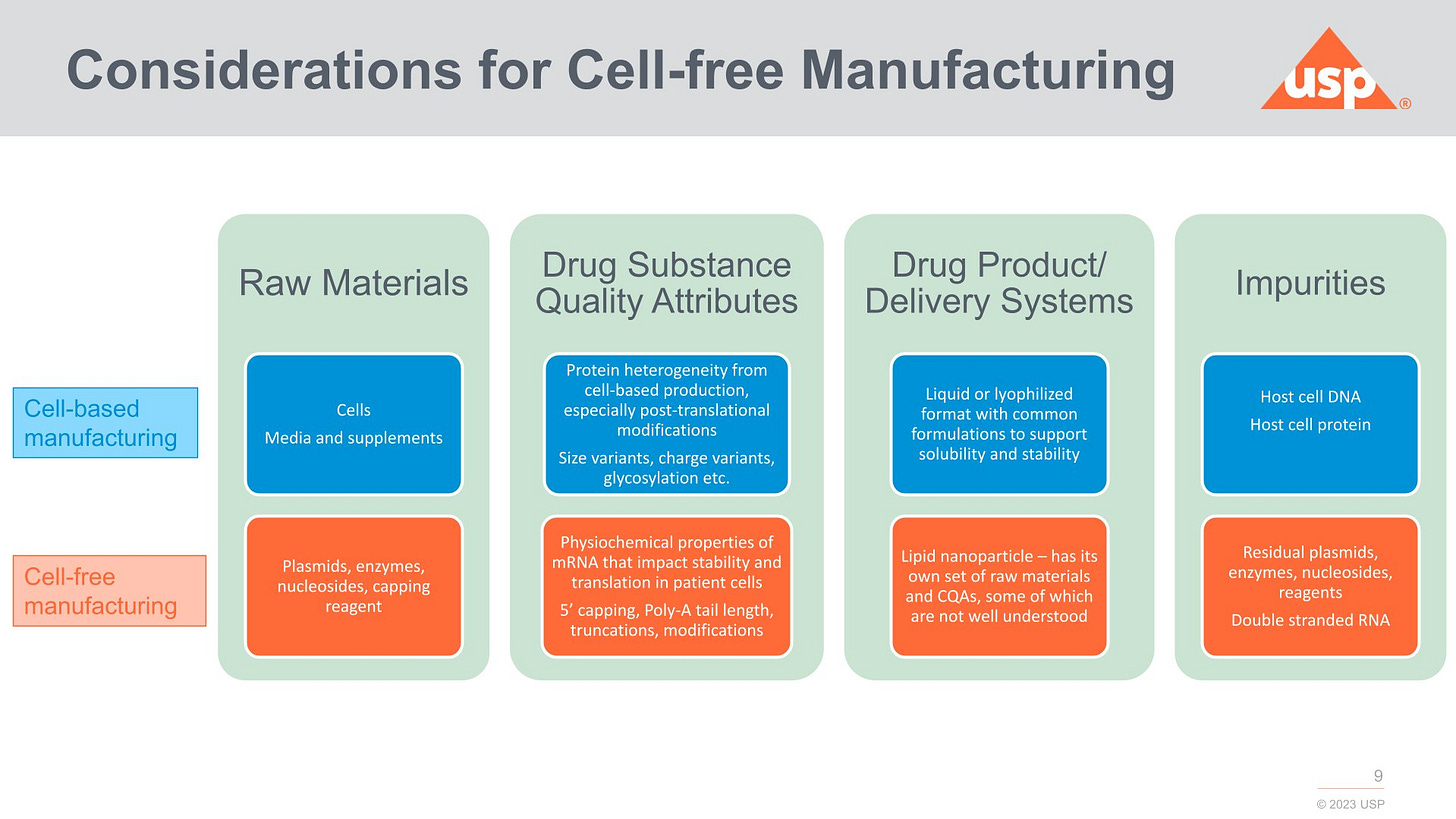
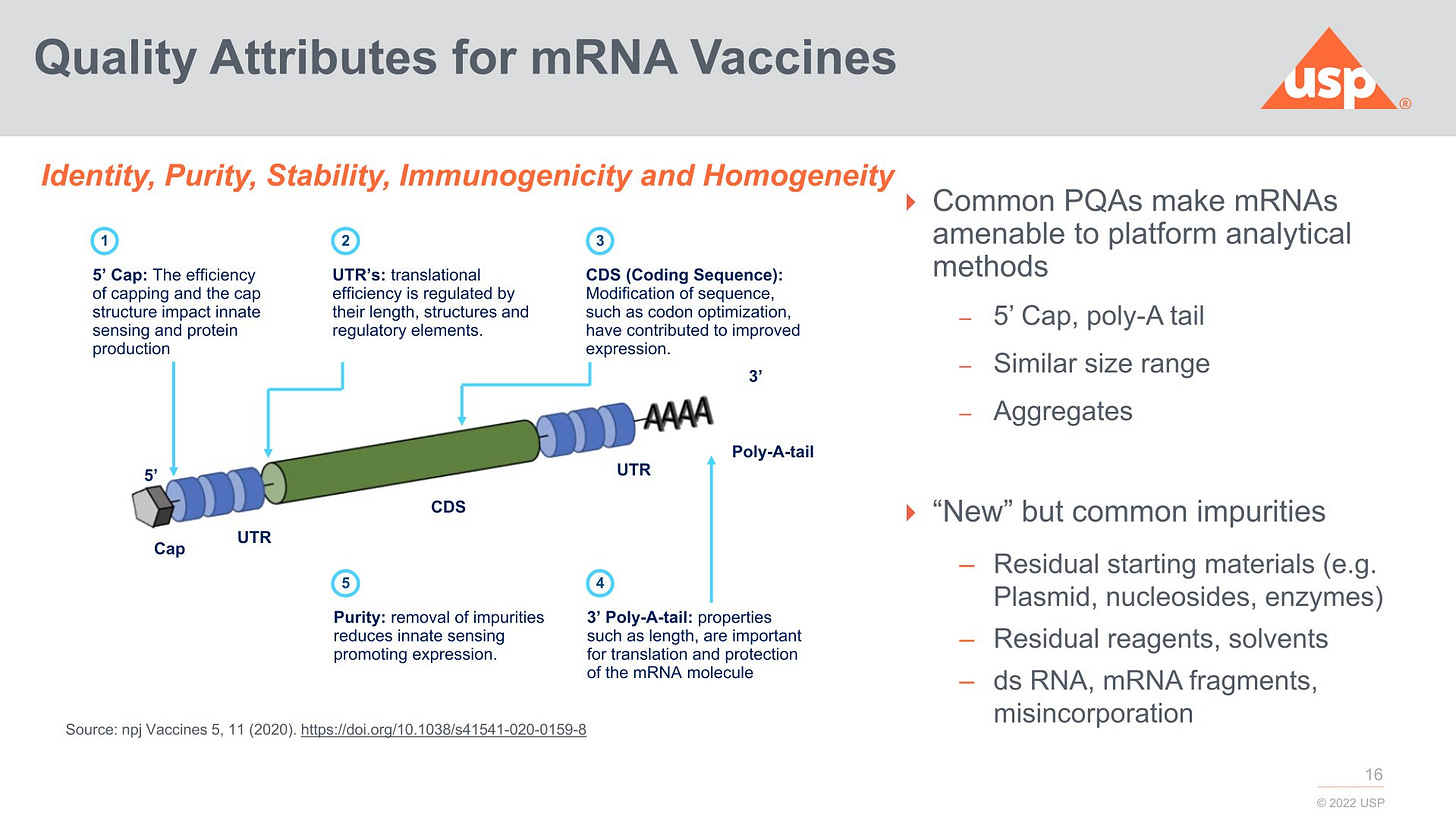
Man listet die ganzen Problemzonen:
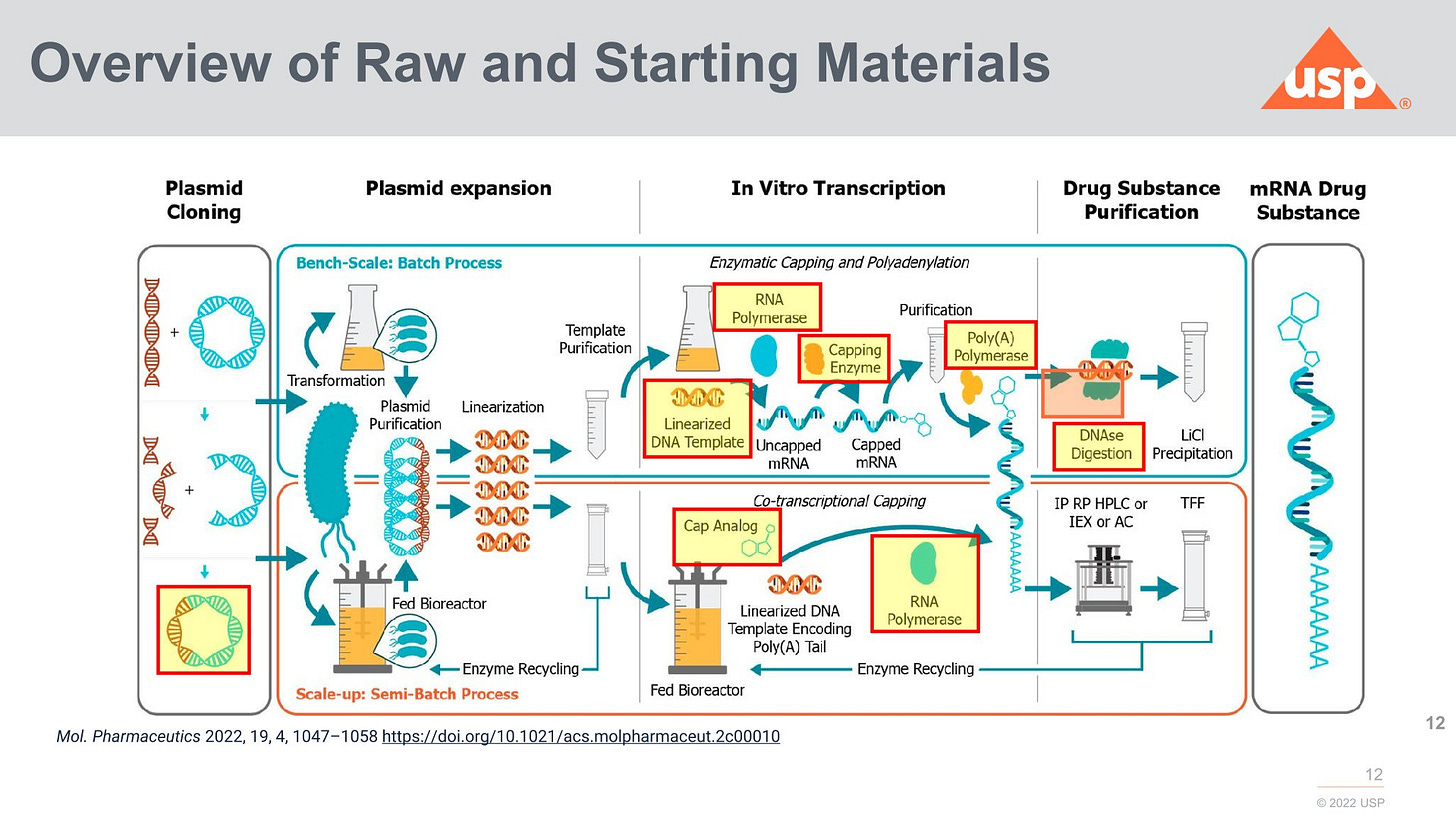
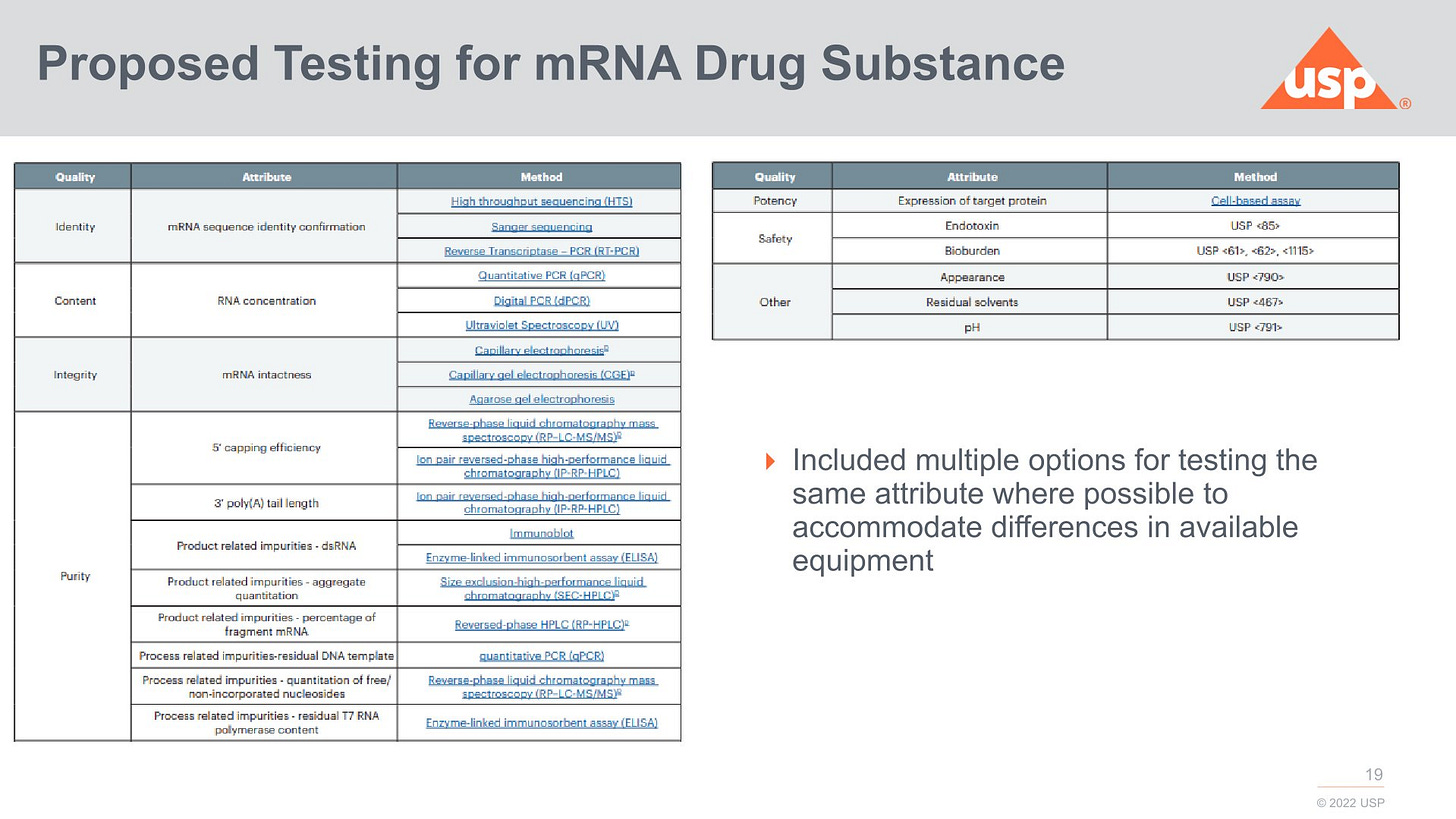
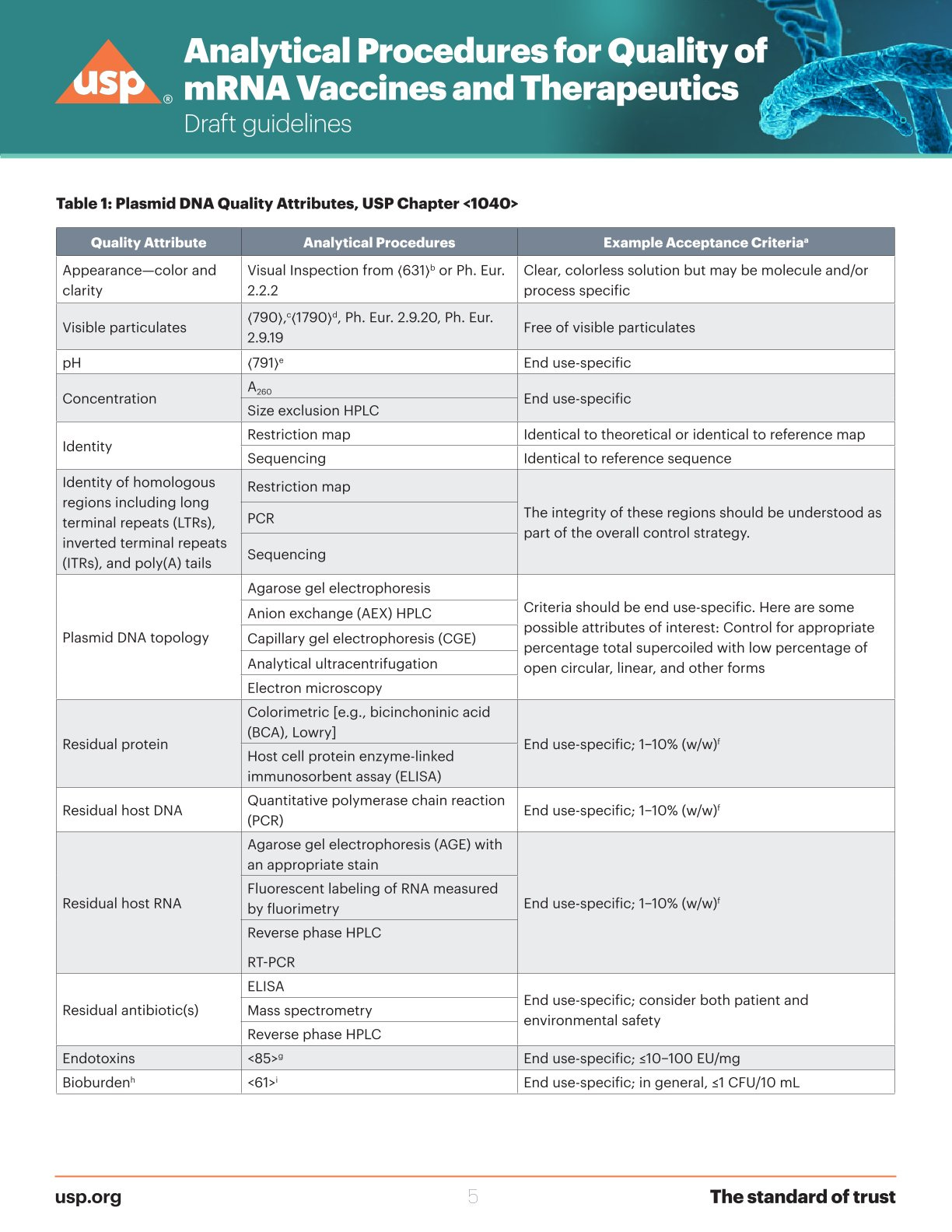
USP unterscheidet direkt zwischen zell-basiert (Prozess 2) und zell-frei (PCR, Prozess 1)
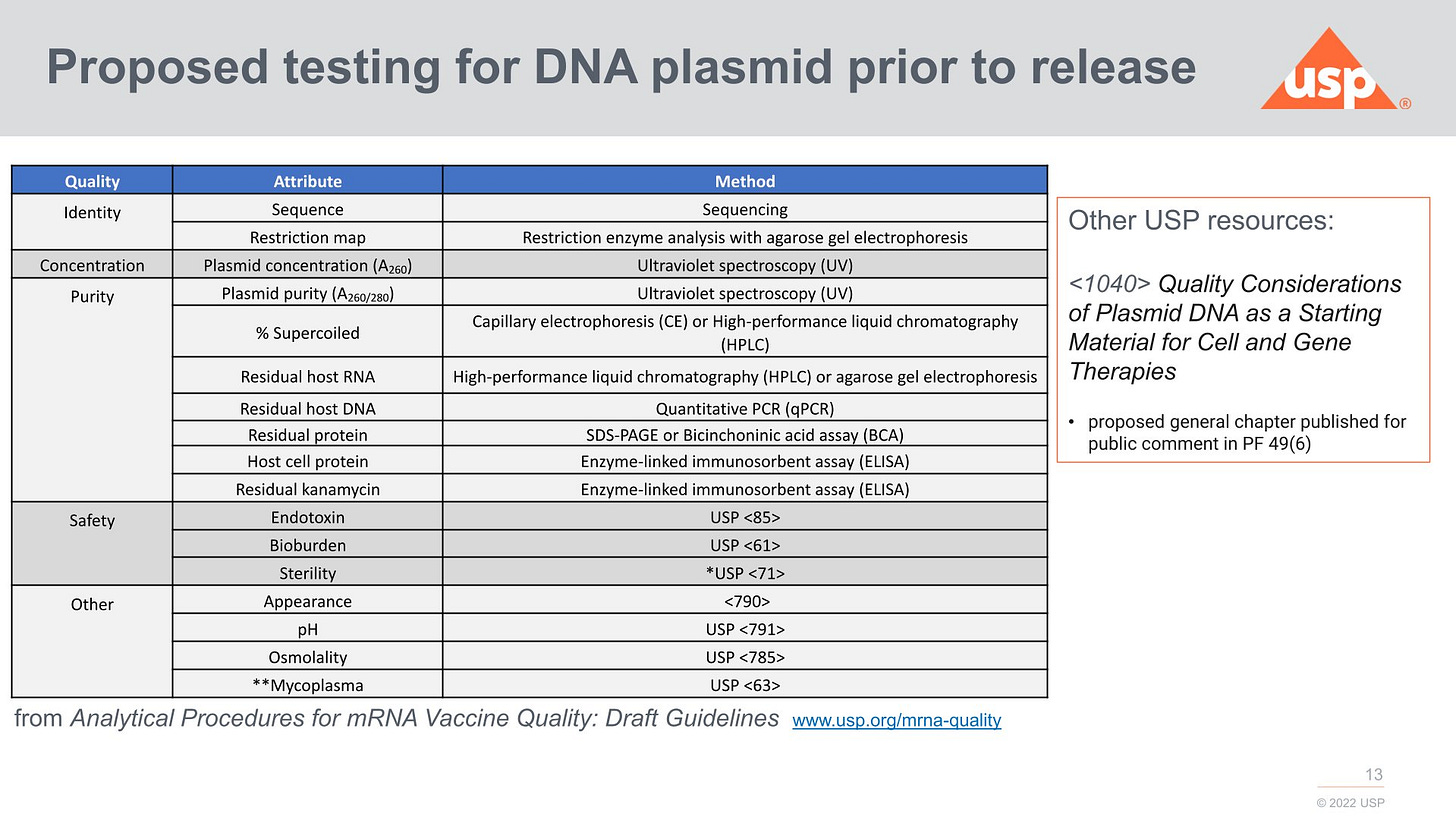
2024 schlug man folgende Analysen vor:
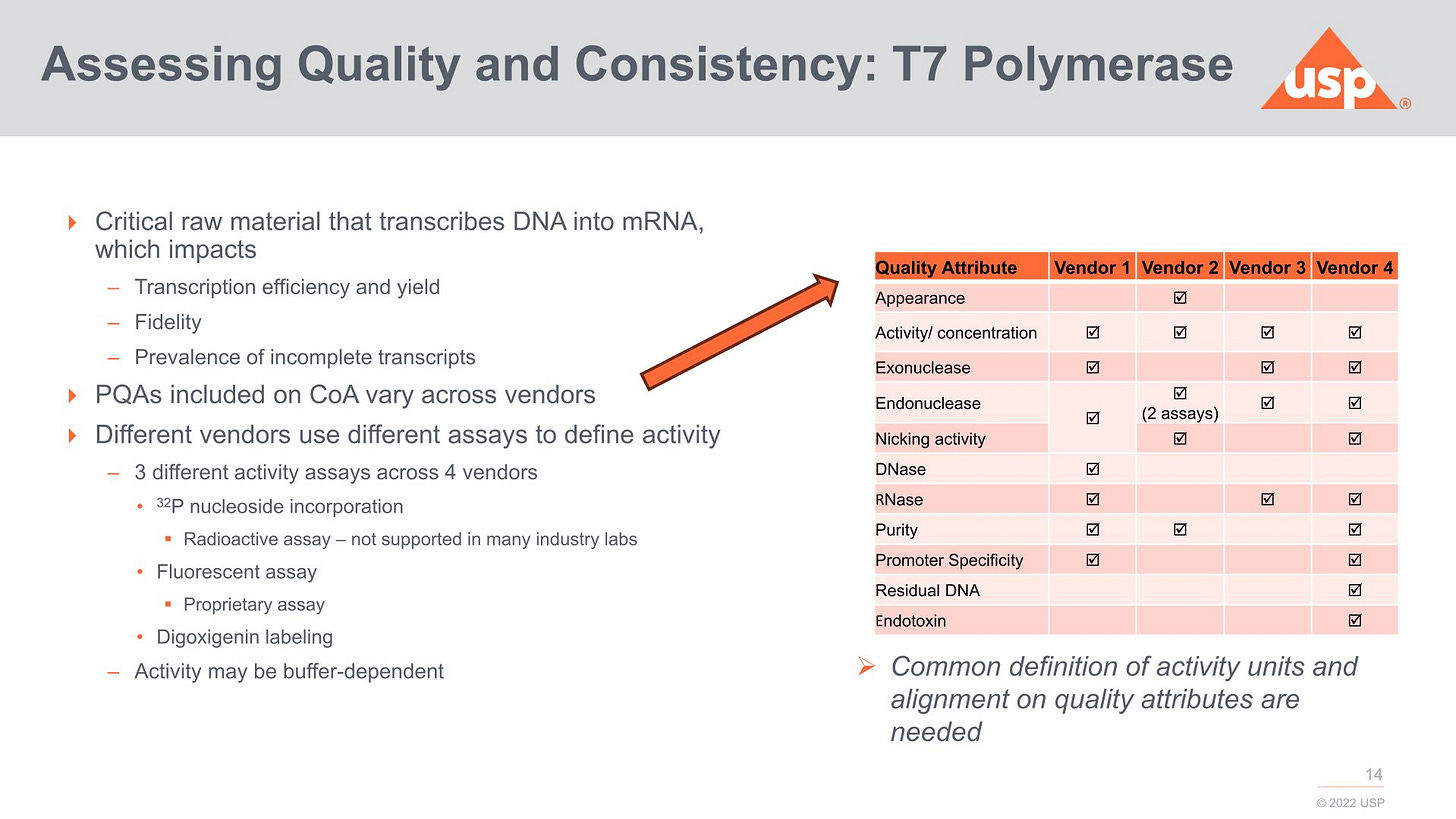
Man kennt das Problem mit normaler T7-Polymerase und dass diese auch template switching und dergleichen machen kann. Streng genommen kann man gar keine normale T7 nehmen, wie man sie aktuell im Katalog bekommt, und müsste die aktuellen Varianten erst optimieren, wie es Moderna gemacht hat.
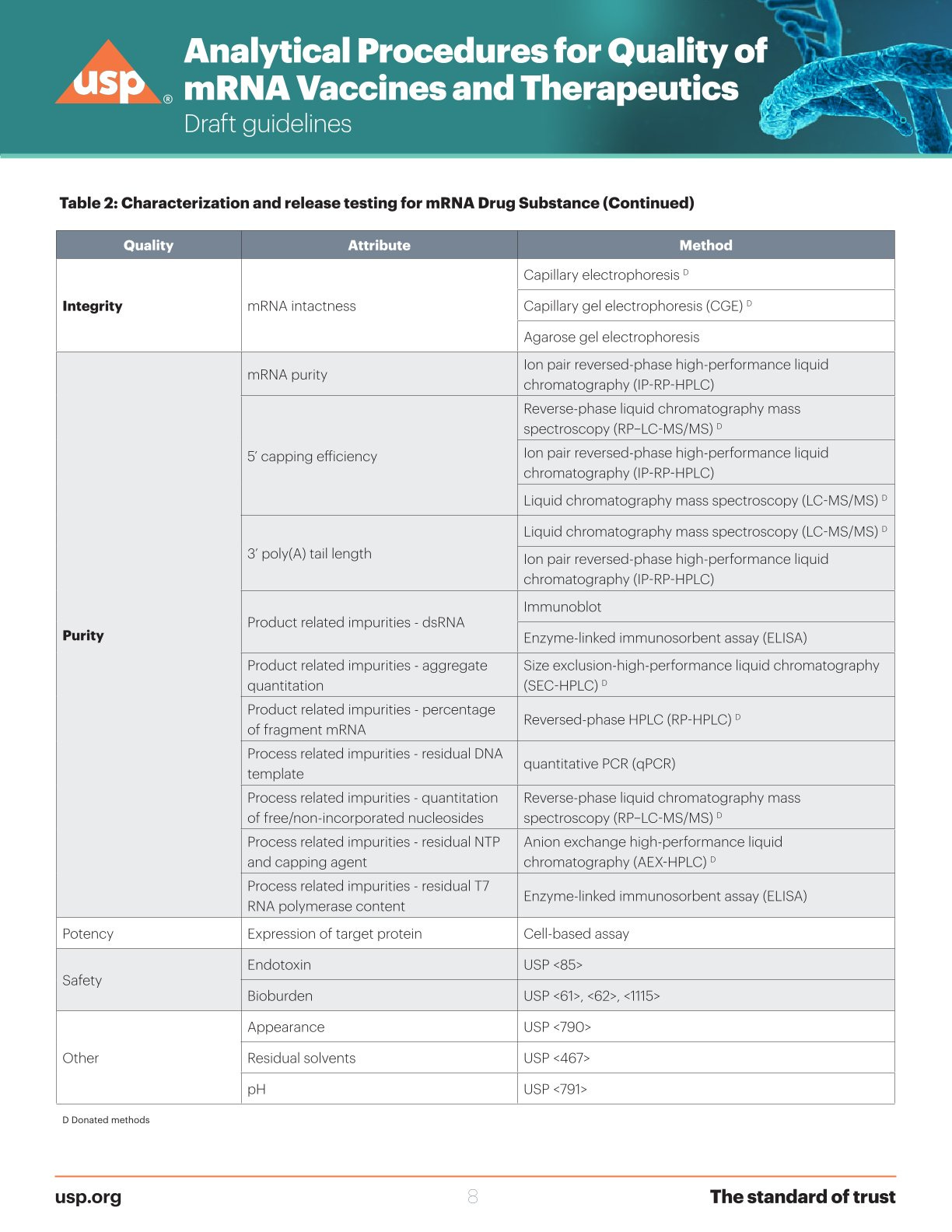
Was die kritischen RNA-Eigenschaften angeht, sieht man das ähnlich wie die EMA. Der mRNA-Impfstoff BNT162b2 (Comirnaty) von BioNTech/Pfizer besitzt einen sogenannten segmentierten (oder gespaltenen) Poly-A-Schwanz. Dieser besteht aus einer Sequenz von 30 Adenosin-Resten (A), gefolgt von einem 10 Nukleotide langen Linker (Spacer) und weiteren 70 Adenosin-Resten (insgesamt ca. 110 Nukleotide). Damit wird die Halbwertszeit massiv verlängert. CureVac beanspruchte ebenfalls Pionierpatente für segmentierte Poly-A-Schwänze und wurde einfach von BioNTech gekauft/geschluckt.
Wie auch immer, es geht nicht nur um die Länge des Poly-A-Schwanzes, man muss auch die Halbwertszeit dieser modifizierten modRNA/mRNA bestimmen. Das fehlt mir.
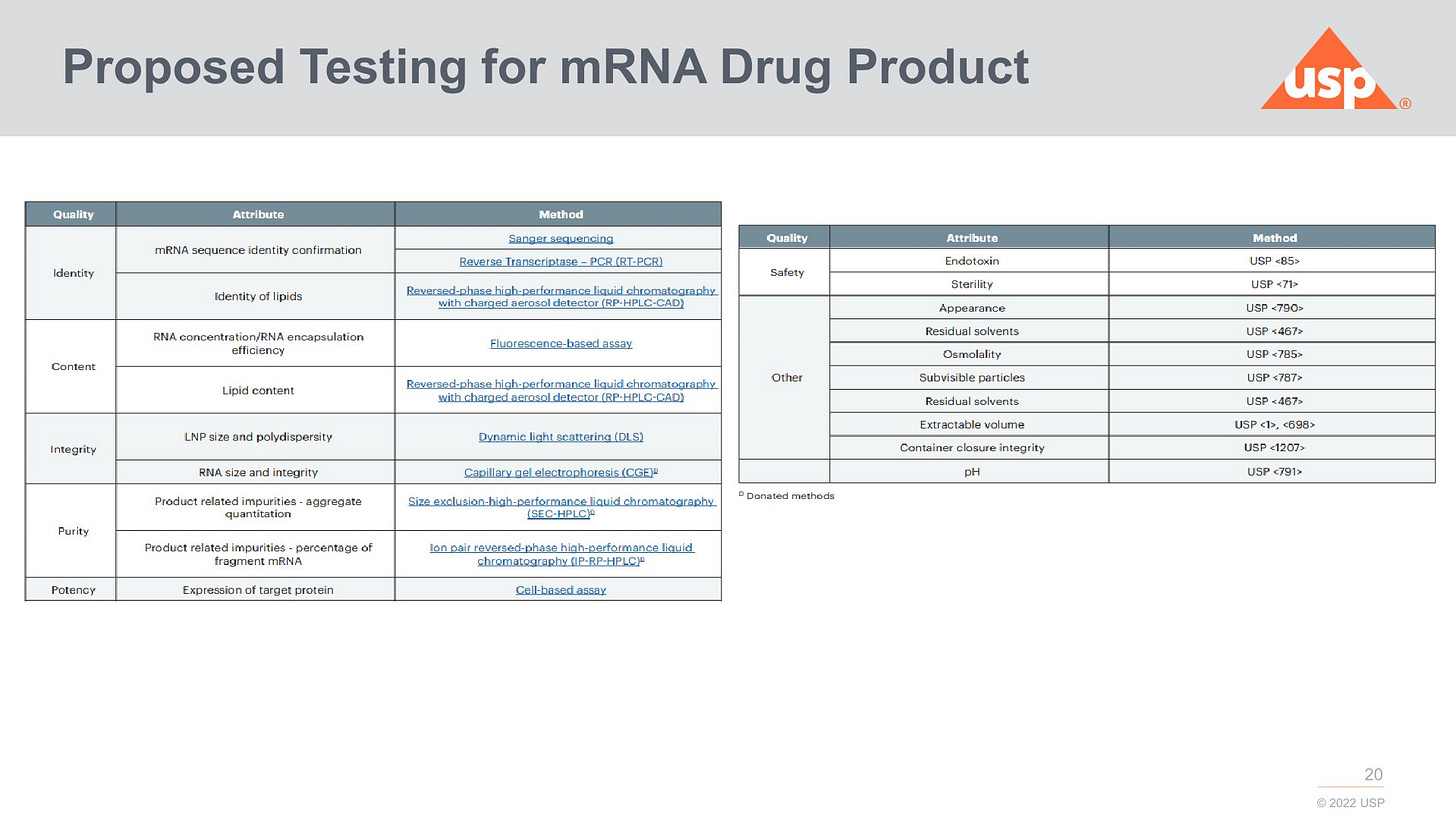
Wie die modRNA getestet werden soll, da ist man bei USP DEUTLICH weiter als bei der EMA
Die Sauberkeit und wie man die Lipide testen soll (HPLC und MS) fehlt mir auch bei USP. Auch in USA scheint man die LNP als inerte Hilfsstoffe anzusehen. Selbst wenn das so wäre, muss man dennoch saubere Hilfsstoffe einsetzen und keine Biotech Chemikalien und keine Mischung verschiedener 3D Varianten (Stereoisomerengemisch). Addukte scheint man nicht erfasst zu haben.
BioNTechs Vorschläge an USP
Neben
Wiseman, D., Mckernan, K. J., Gutschi, L. M., & Rose, J. (2023). Comments on USP Draft Guidelines: Analytical Procedures for mRNA Vaccine Quality, 2nd edition v2. Esearchgate. https://doi.org/10.13140/rg.2.2.33586.99526
musste natürlich BioNTech auch Vorschläge machen, wie man ihr Produkt testen sollte.
Jahn Michael Falcke ist neu dabei bei BioNTech seit 2024. Also niemand, den man verklagen könnte.
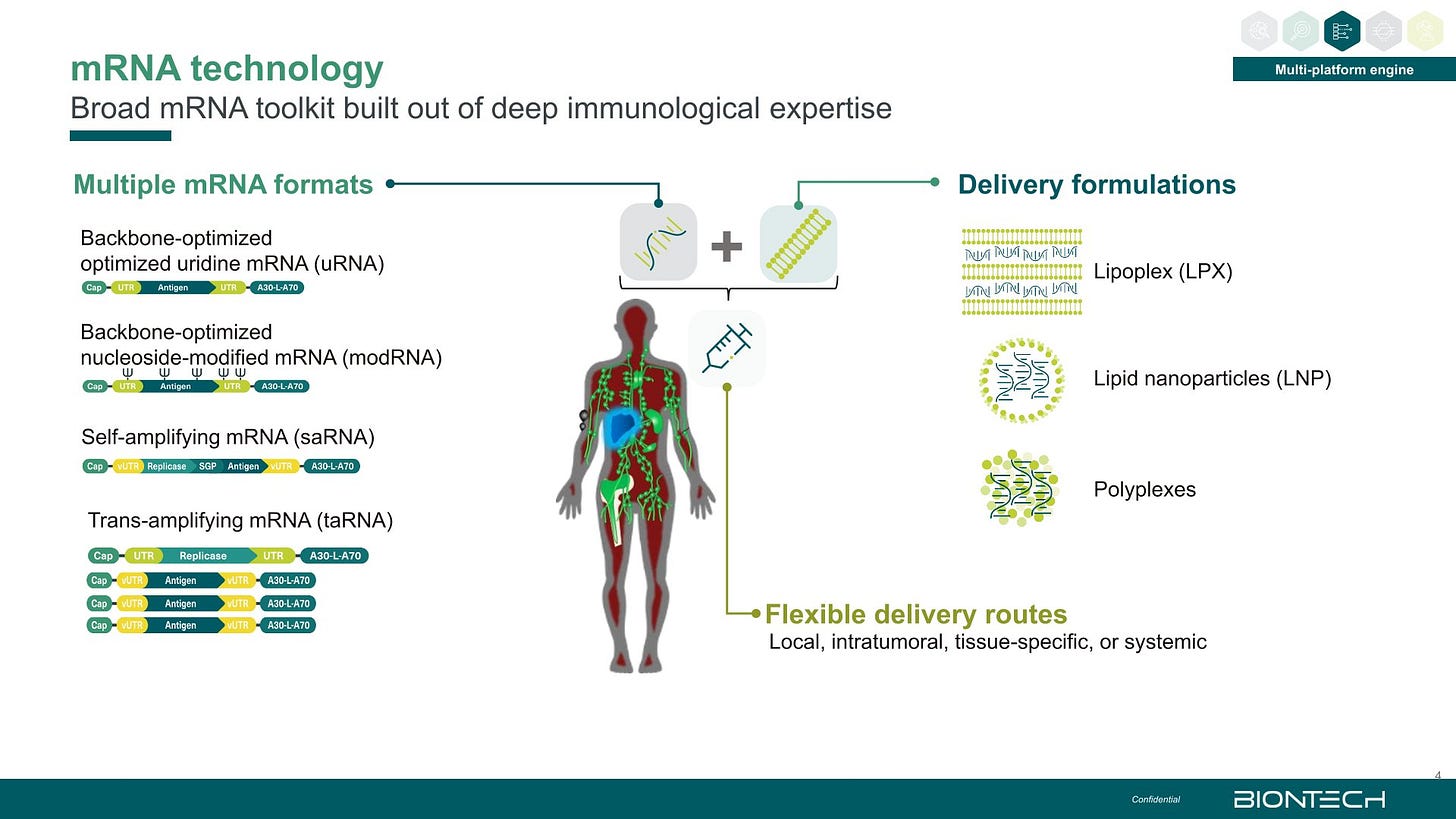
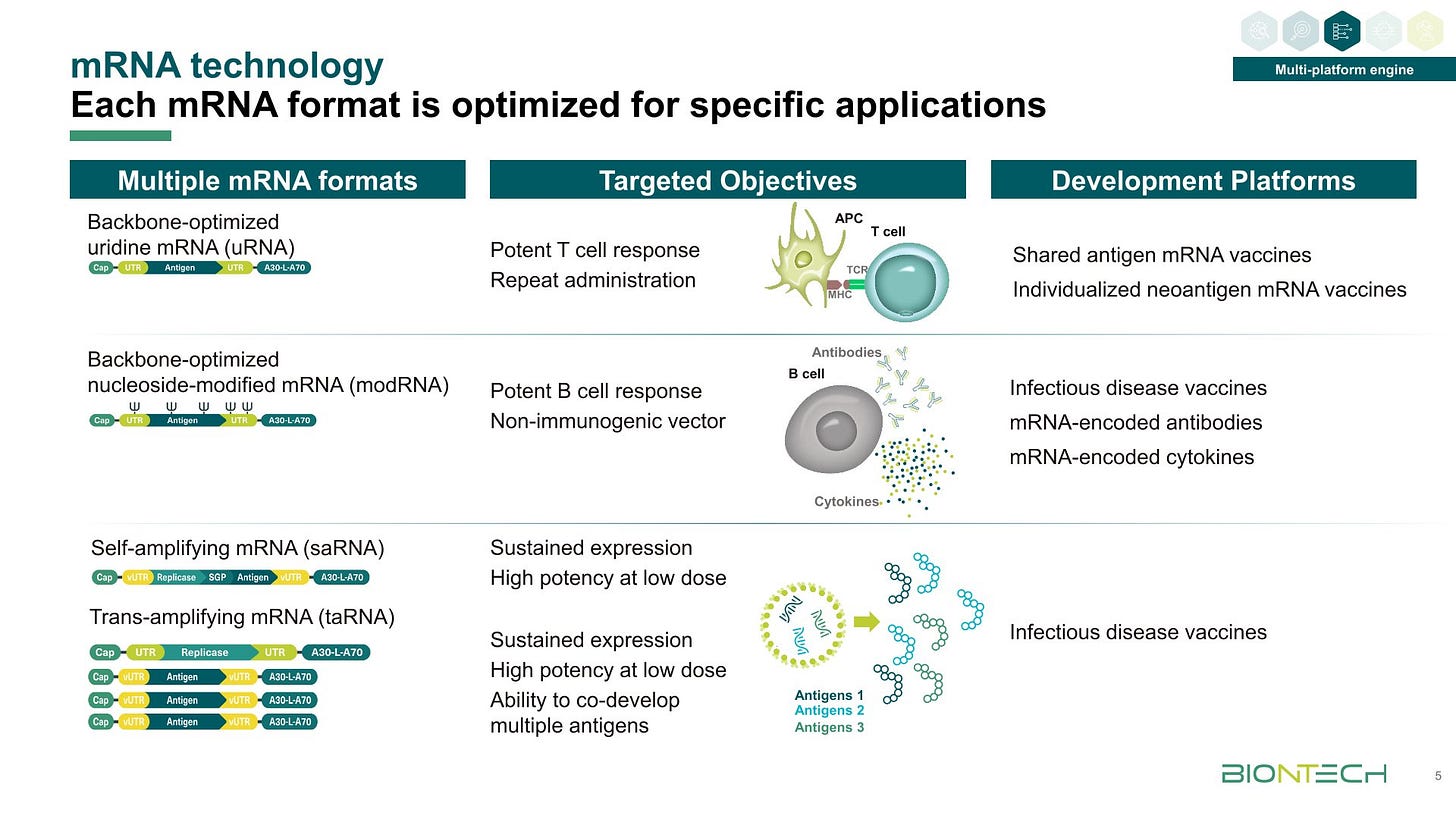
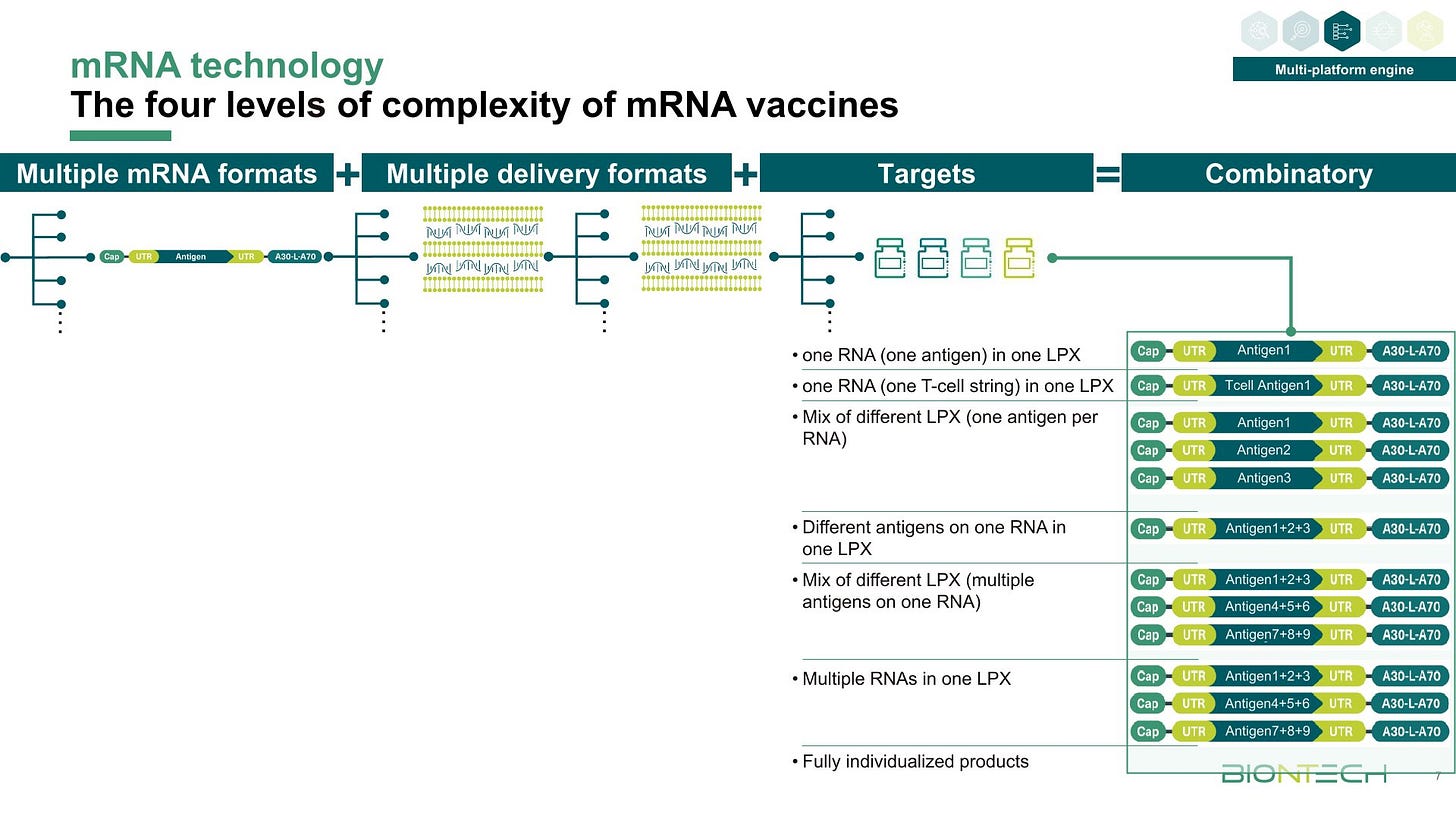
Die Präsentation gibt einen schönen Überblick über die verschiedenen mdRNA und mRNA Varianten an den BioNTech forscht:
Man beachte dass saRNA für anhaltende Expression gedacht ist, nicht für schnell mal ein paar Proteine. Das Zeugs, dass einem als COVOD-”Impfung” untergejubelt wurde soll laut dieser Folie B-Zellen aktivieren, während man früher behauptet hat, es würde dendritische Zellen als Ziel haben.
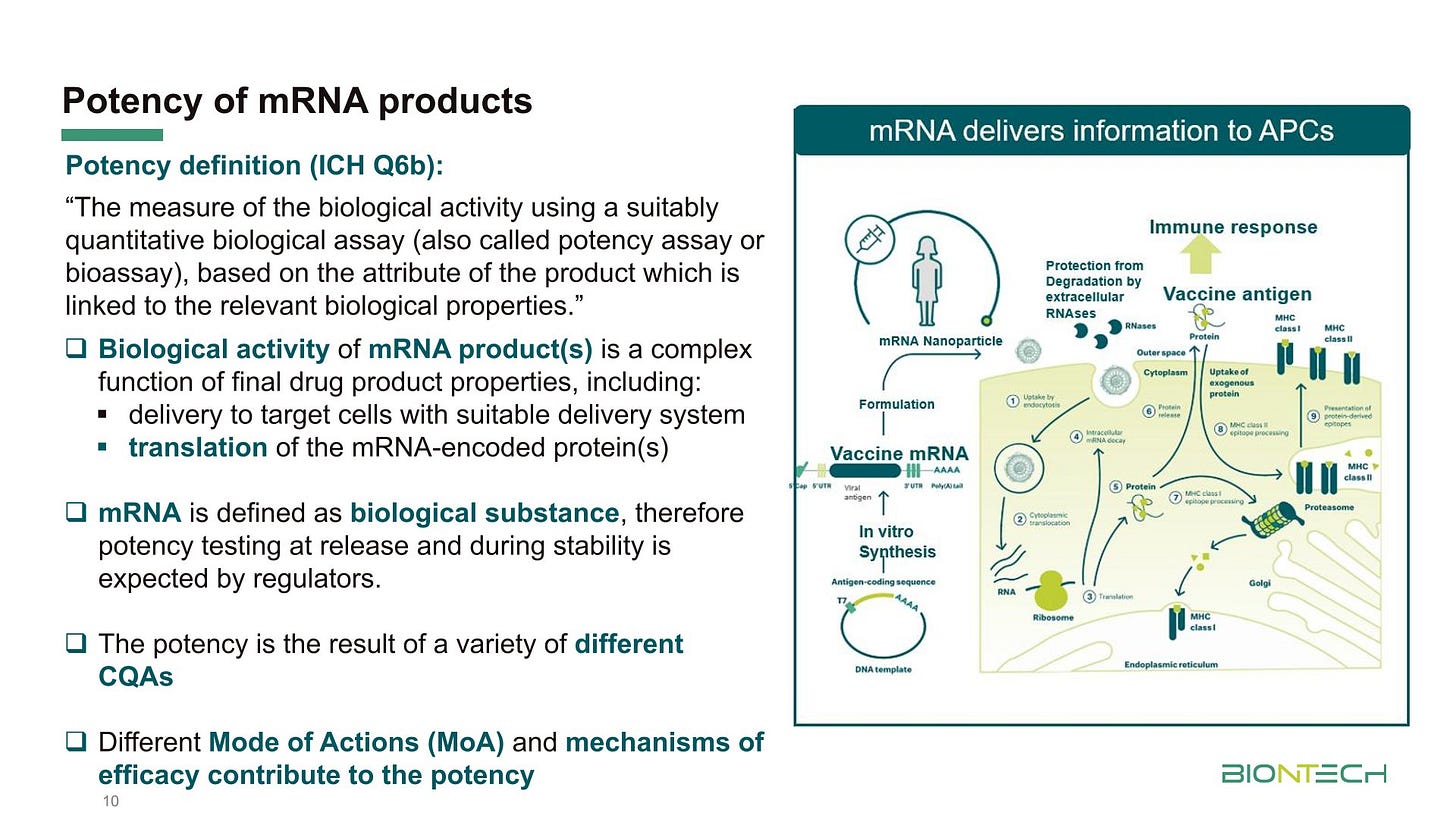
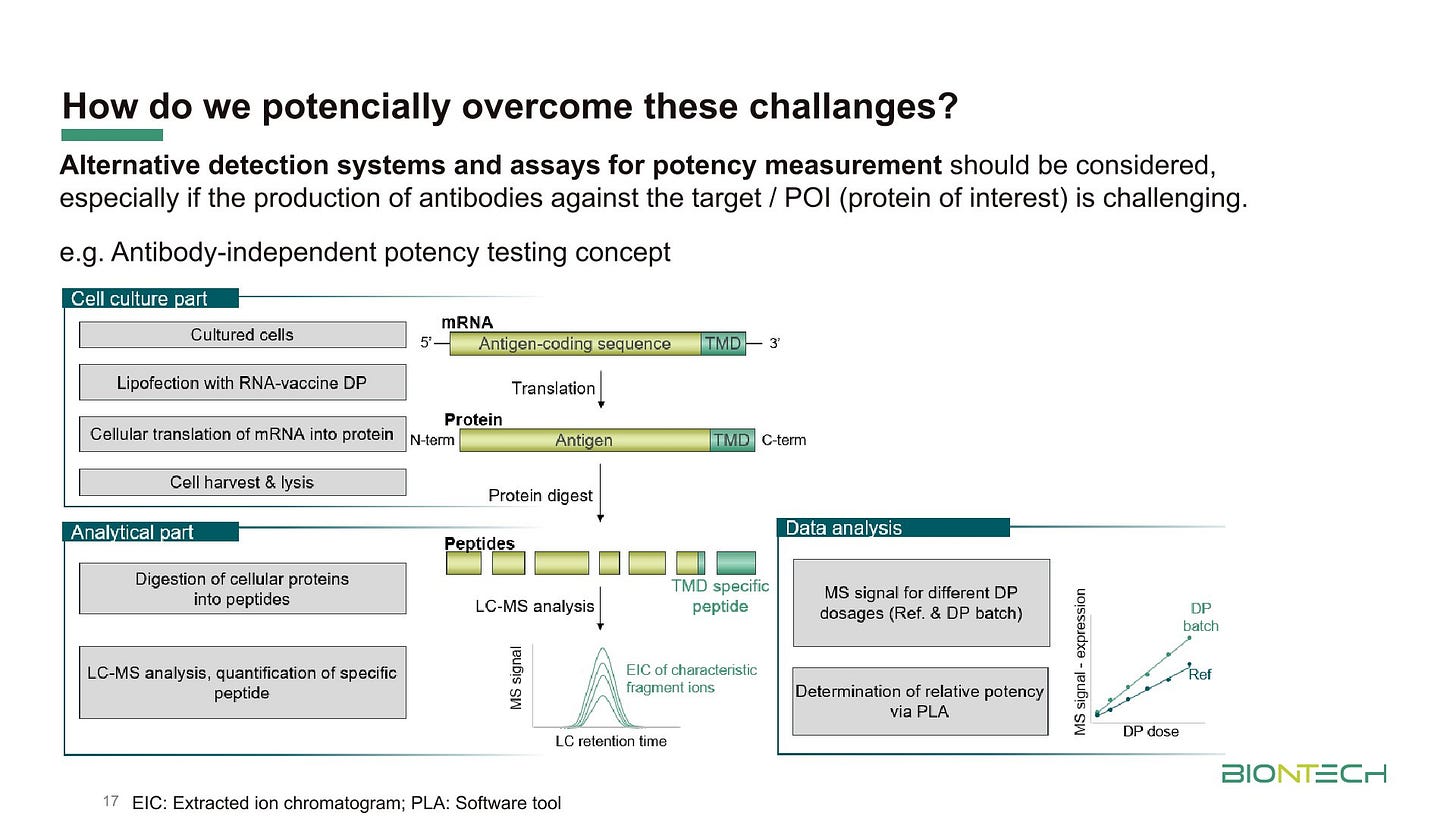
Wie BioNTech aktuell die Wirksamkeit (potency) testet:
Da die Anwendung der mRNA-Technologie relativ neu ist, befinden sich die behördlichen Richtlinien und Branchenstandards noch in der Entwicklung.
Es besteht Bedarf an einem kontinuierlichen Dialog zwischen Industrie und Aufsichtsbehörden, um auftretende Fragen zu klären.
Derzeit laufen mehrere Initiativen, um nicht nur analytische Aktivitäten/Verfahren und die Qualitätskontrolle (einschließlich Wirksamkeit) für mRNA-Impfstoffe zu erörtern und zu harmonisieren, z. B.:
• Die Ph. Eur.-Kommission hat eine neue Arbeitsgruppe für mRNA-Impfstoffe eingerichtet (EDQM1)
• United States Pharmacopeia – National Formulary; Entwurf einer USP-Leitlinie2 zu den analytischen Verfahren für mRNA-Impfstoffe (2. Fassung)
„Die Bestimmung der biologischen Aktivität mittels eines geeigneten quantitativen biologischen Assays (auch als Wirksamkeitsassay oder Bioassay bezeichnet), basierend auf dem Merkmal des Produkts, das mit den relevanten biologischen Eigenschaften in Zusammenhang steht.“
❑ Die biologische Aktivität von mRNA-Produkten ist eine komplexe Funktion der Eigenschaften des Endarzneimittels, darunter:
▪ die Zufuhr zu Zielzellen mittels eines geeigneten Verabreichungssystems
▪ die Translation der durch die mRNA kodierten Proteine
❑ mRNA wird als biologische Substanz definiert, daher erwarten die Zulassungsbehörden Wirksamkeitstests bei der Freigabe und während der Haltbarkeitsprüfung.
❑ Die Wirksamkeit ist das Ergebnis einer Vielzahl verschiedener CQAs
❑ Verschiedene Wirkmechanismen (MoA) und Wirkprinzipien tragen zur Wirksamkeit bei
Wie das Zeugs funktioniert. Man beachte dass die Funktionsweise eine Präsentation über HLA ist. MHC (Major Histocompatibility Complex): Das ist der allgemeine biologische Überbegriff für das System von Genen und Proteinen, die für die Immunerkennung zuständig sind. HLA ist einfach nur der Name für die menschliche Version dieses Systems…
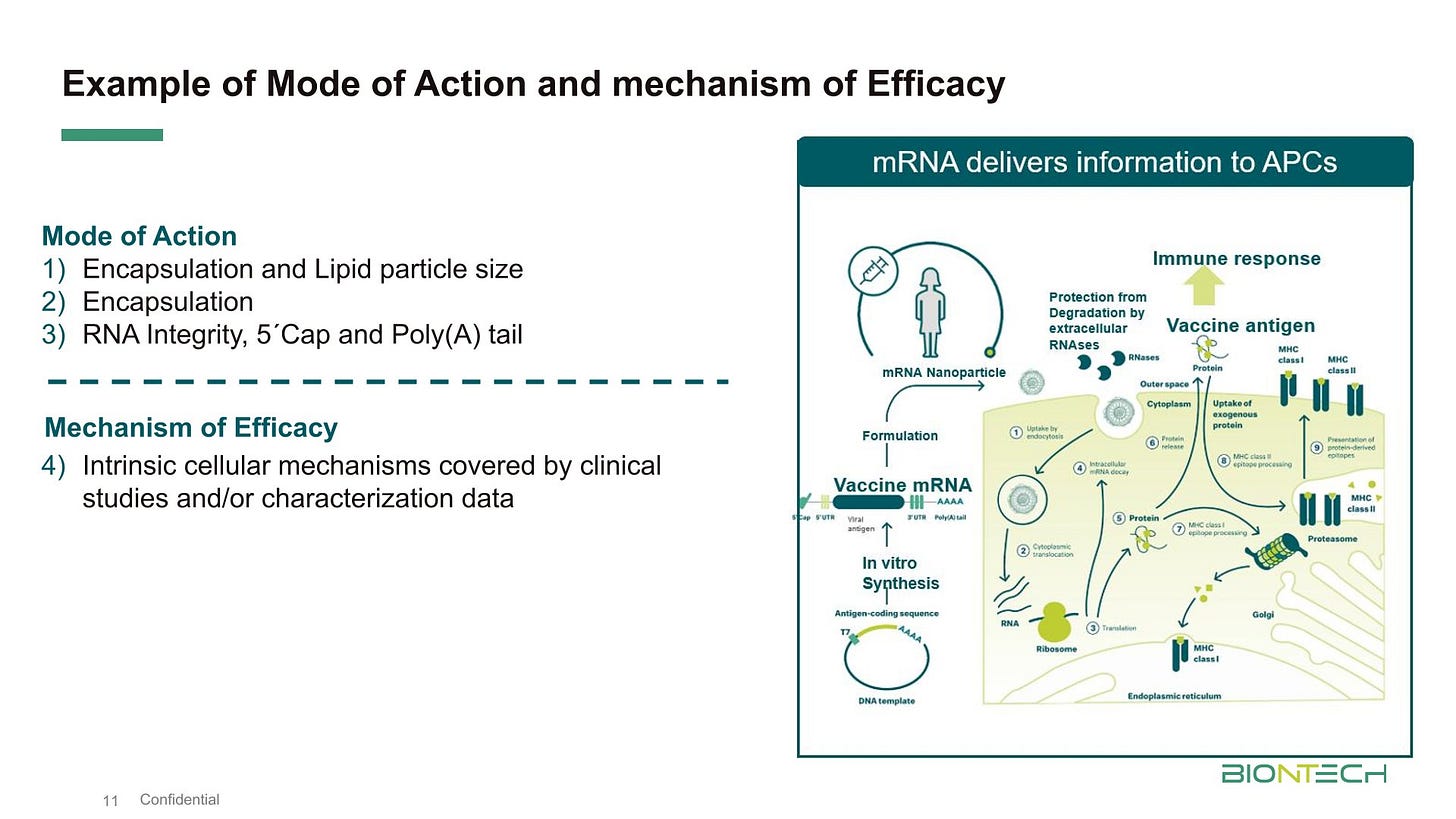
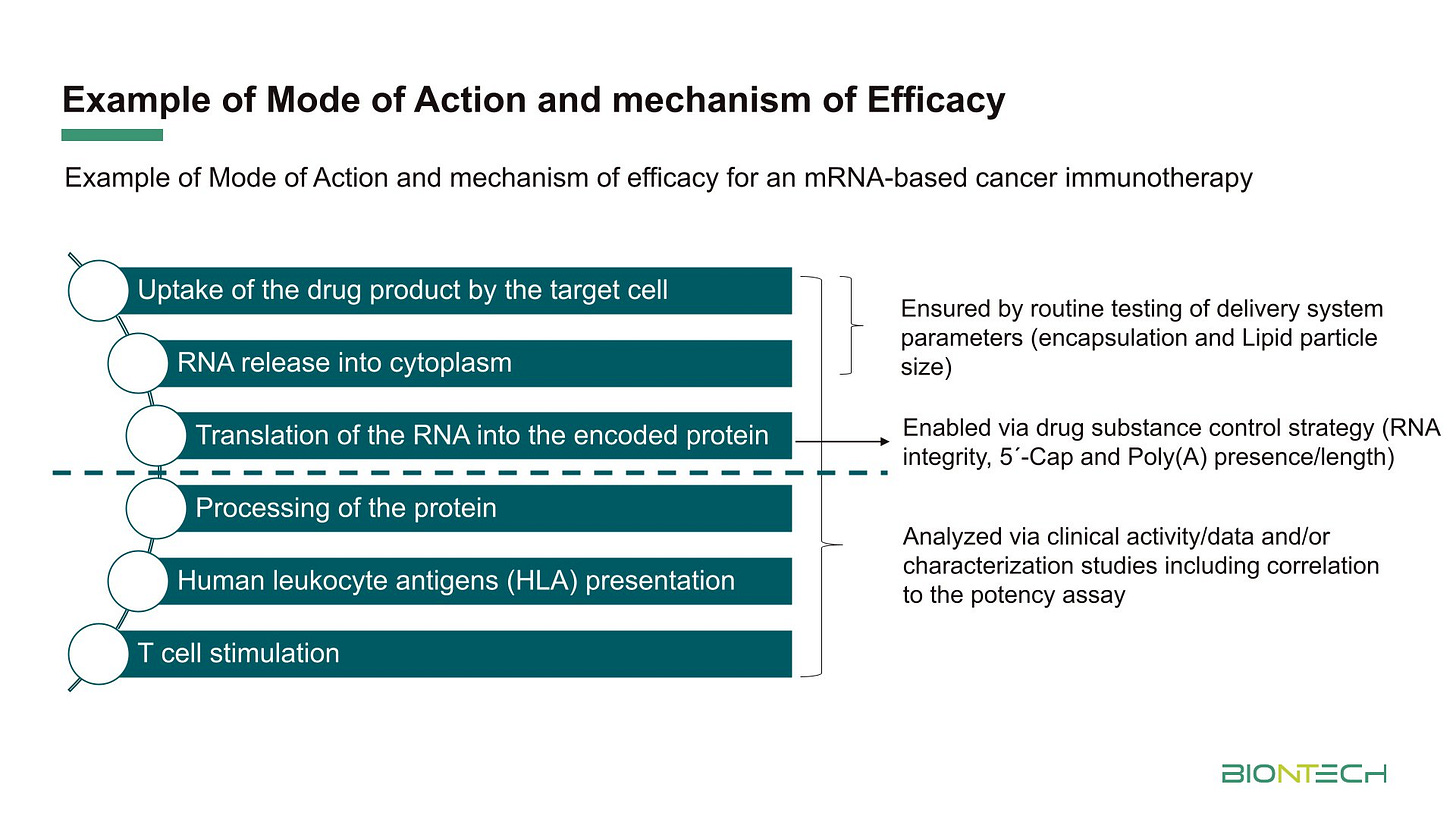
Damit wären wir wieder bei der Mittelstufenbiologie:
Qualitätsmerkmale, die selbst BioNTech als wichtig zugibt:
Bei der mRNA/modRNA hat man nur die Primästruktur im Blick, dabei ist die Tertiärstruktur das eigentlich wichtige. Das habe ich in Teil 1 besprochen.
Was BioNTech wohlweislich nicht anspricht: Sauberkeit der Lipide, Länge des PEG, Protein-Corona, Biodistribution… Die Bereiche, die vermieden werden sagen recht viel, würde ich sage.
USP Aktueller Stand, Version 3
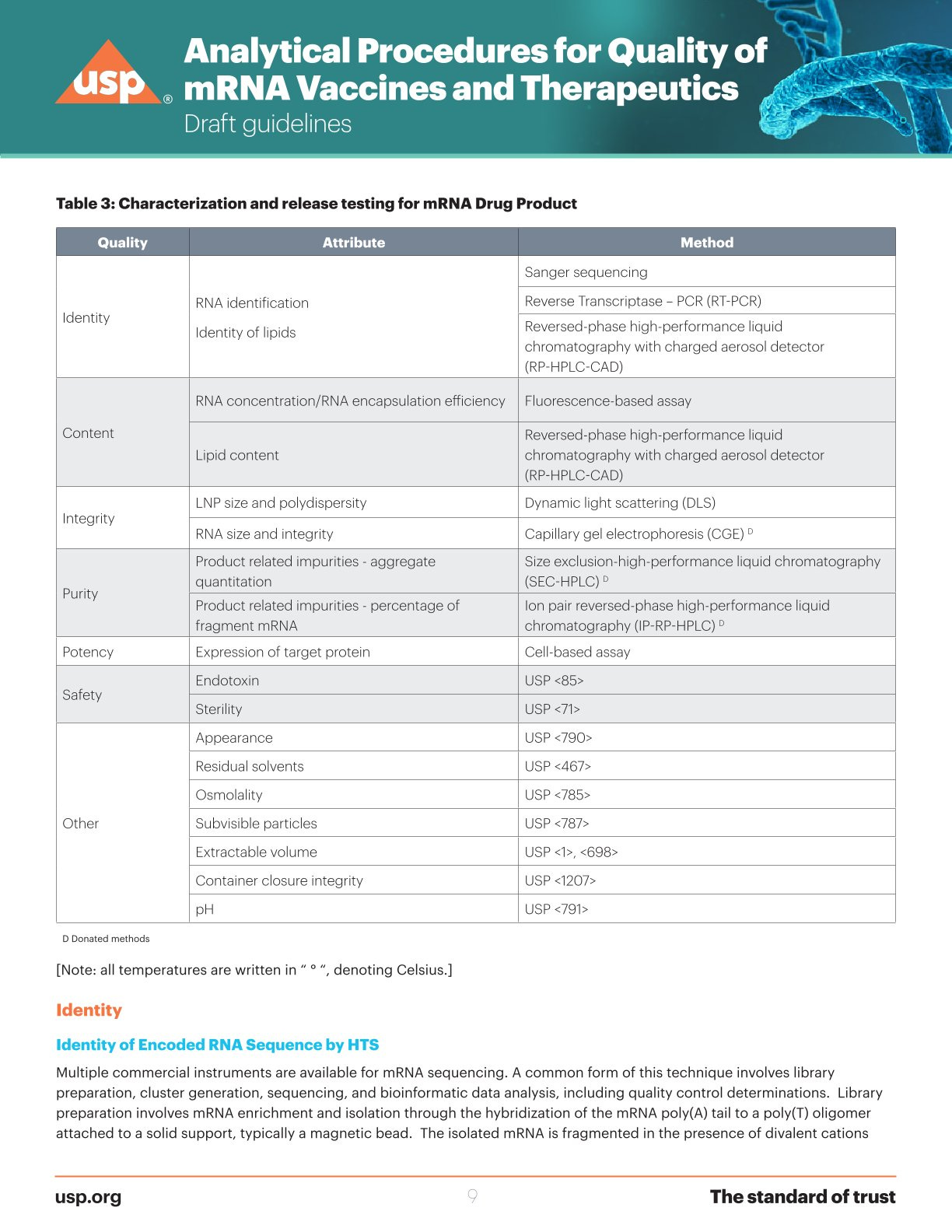
In Version 3 hat man schon Produktbedingte Rückstände und Prozessbedingte Rückstände hinzugefügt.
In Version 3 hat man die Lipide schon im Blick und muss deren Anteil per HPLC bestimmen.
USP ist hierbei sehr spezifisch, für PCR werden die Zyklen definiert, bei HPLC der Gradient, während die Dilettanten der EMA vorschlagen, dass man generell diese Methoden nehmen könnte, ohne sie genau zu definieren.
Im direkten Vergleich zu USP Version 3 wird der Dilettantismus des EMA Vorschlags sehr offensichtlich.
USP Version 3 kann man nur nach Angabe des Namens herunterladen. Edge öffnet das pdf nicht, Chrome schon.
Ich habe das Dokument daher zum Download integriert:
Mein Fazit:
BioNTech vermeidet in Sachen Qualität in der firmeneigenen PPT den Bereich der Sauberkeit der Lipide, was einiges durchblicken lässt. Das scheint keine Priorität zu haben.
Bei USP scheint mir die komplette Proteinbiochemie zu fehlen und auch die Tertiärstruktur der modRNA hat man nicht im Blick. Nur weil ein soweit identisch aussehende Protein im Essay gebildet wird, heißt es nicht, dass es sich wie der Wildtyp verhält. Zudem können, je nach Fragmentierung der Vorlage verkürzte Proteine/Peptide entstehen.
Auf der Proteineben, besonders bei hybriden Proteinen bei binären Produkten, sind sowohl EMA als auch USP blind.
Ich hoffe, es gibt eine Version 4. Version 3 ist schon deutliche besser als der EMA Entwurf, erfasst aber mitnichten die nanomedizinischen Probleme dieser Produktklasse. Die nanomedizinischen Aspekte werden sowohl von USP als auch EMA ignoriert.
Genetische Probleme durch mRNA/modRNA-Fragmente wie Oncomirs (siehe Teil 1) haben weder USP noch EMA erfasst.
Unterstützungsmöglichkeiten:
Bücherwunschzettel: https://www.amazon.de/registries/gl/owner-view/30LG3DJ4ET90L?ref_=list_d_gl_lfu_nav
Andere Unterstützungsmöglichkeiten für Holgers und meine Forschung:
Konto für Unterstützung für das Projekt Scan 2000
Dr. Merse DE34 4305 0001 0302 7851 75 Sparkasse Bochum
Horst Reissner: IBAN DE51 4401 0046 0406 4514 67
Dr. S. Stebel: https://ko-fi.com/einmalmitprofisarbeiten
mRNA Technology https://www.usp.org/mrna
Wiseman, D., Mckernan, K. J., Gutschi, L. M., & Rose, J. (2023). Comments on USP Draft Guidelines: Analytical Procedures for mRNA Vaccine Quality, 2nd edition v2. Esearchgate. https://doi.org/10.13140/rg.2.2.33586.99526
Trepotec Z, Geiger J, Plank C, Aneja MK, Rudolph C. Segmented poly(A) tails significantly reduce recombination of plasmid DNA without affecting mRNA translation efficiency or half-life. RNA. 2019 Apr;25(4):507-518. doi: 10.1261/rna.069286.118. Epub 2019 Jan 15. PMID: 30647100; PMCID: PMC6426288. https://pmc.ncbi.nlm.nih.gov/articles/PMC6426288/
Spiewla T, Czubak K, Pilch Z, Baranowski MR, Krawczyk PS, Affek K, Antczak W, Szulc-Gasiorowska M, Chmielinski S, Mroczek S, Brouze M, Nowis D, Golab J, Dziembowski A, Jemielity J, Kowalska J. PolyA tail segmentation improves the stability of the template DNA and increases the translatability of in vitro transcribed mRNA. Nucleic Acids Res. 2026 Jan 14;54(2):gkaf1412. doi: 10.1093/nar/gkaf1412. PMID: 41538312; PMCID: PMC12805897. https://pmc.ncbi.nlm.nih.gov/articles/PMC12805897/
Eberle, F., Sahin, U., Kuhn, A., Vallazza, B., Diken, M., gGmbH, T. T. O. a. D. U. D. J. G. U. M., & GmbH, B. R. P. (2014b, July 11). WO2016005324A1 – Stabilization of poly(a) sequence encoding dna sequences – Google Patents. https://patents.google.com/patent/WO2016005324A1
Eberle, F., Sahin, U., Kuhn, A., Vallazza, B., Diken, M., gGmbH, T. T. O. a. D. U. D. J. G. U. M., & GmbH, B. R. P. (2014, July 11). US10717982B2 – Stabilization of poly(A) sequence encoding DNA sequences – Google Patents. https://patents.google.com/patent/US10717982B2/
Thess, A., Schlake, T., Grund, S., & Ag, C. (2014, December 12). EP3708668A1 – Artificial nucleic acid molecules for improved protein expression – Google Patents. https://patents.google.com/patent/EP3708668A1/en
(13) Jan Michel Falcke | LinkedIn https://www.linkedin.com/in/jan-michel-falcke-7b2b1aa8/