Die Schweizer Verträge unterscheiden sich von den EU Verträgen, soweit ich sie gelesen habe.
In den ersten beiden Artikeln habe ich mir die Verträge von Pfizer angesehen.
In diesem Teil widme ich mich einem ungeschwärzen Vertragswerk, jenem von Moderna. Das ist insofern spannend, weil zu Moderna nicht viele Daten vorliegen, obwohl auch dieser Hersteller alle Studiendaten herausgeben muss.
Memorandum of Understanding
Laut Vertrag wollte auch Moderna natürlich GMP konform arbeiten.
Der Liefervertrag sieht vor, dass Moderna und das BAG gemeinsam einen Plan ausarbeiten, um die entsprechende beschleunigte behördliche Zulassung (d. h. die Marktzulassung) für den Moderna-Impfstoff zu erlangen. Moderna (oder ein von Moderna benannter Kooperationspartner) wird wirtschaftlich angemessene Anstrengungen unternehmen, um diese Aktivitäten zu leiten und die entsprechenden Genehmigungen zu erwirken, wobei diese Anstrengungen jedoch nicht dazu führen dürfen, dass Moderna zusätzliche Studien oder klinische Prüfungen durchführen muss. Ungeachtet dessen trägt das BAG alle Kosten im Zusammenhang mit der Erlangung der erforderlichen behördlichen Zulassung für den Vertrieb des Moderna-Impfstoffs in der Schweiz. Es ist die Absicht von Moderna, dass eine Moderna-Einheit der Inhaber der Marktzulassung für den Moderna-Impfstoff in der Schweiz sein wird, sofern dies nicht nach den vor Ort geltenden Gesetzen unzulässig ist, und dass Moderna die üblichen Kosten für diese Marktzulassung trägt (zur Vermeidung von Zweifeln: ausgenommen sind die Kosten für zusätzliche Studien oder klinische Prüfungen, die von Swissmedic verlangt werden). Zu diesem Zweck unternimmt Moderna wirtschaftlich angemessene Anstrengungen, um der zuständigen Schweizer Zulassungsbehörde auf eigene Kosten alle Datenpakete und sonstigen Informationen/Dokumente zur Verfügung zu stellen, die von dieser im Zusammenhang mit der Zulassung des Moderna-Impfstoffs in der Schweiz vernünftigerweise verlangt werden; vorausgesetzt jedoch, dass (i) diese Anstrengungen von Moderna keine Durchführung zusätzlicher Studien oder klinischer Prüfungen erfordern, und (ii) vorbehaltlich des anwendbaren Rechts die zuständige Schweizer Zulassungsbehörde alle diese Daten, Informationen und Dokumente gemäß den Geheimhaltungspflichten, an die sie bei einer solchen Einreichung gesetzlich gebunden ist, vertraulich behandelt.
Es ist schon dreist, dass Moderna von der BAG verlangt bei der Zulassung Druck zu machen, um eine beschleunigte Zulassung zu bekommen.
Was die klinischen Prüfungen angeht und dass man keine weiteren Studien machen will, dazu muss man wissen wie die Zulassung bei allen, außer Pfizer, gelaufen ist.
Pfizer hat alleine sein eigenes Ding gemacht bei den Studien. Moderna, J&J und AstraZeneca hingegen durchliefen mit ihren Studien ein zentralisiertes System. Es gab ein “Safety Monitoring Board” (DSMB), welches die Studienprotokolle dieser drei Hersteller aufeinander abstimmte, damit die Studien soweit parallel liefen. Dieses Board durfte jederzeit entblinden und die Studien stoppen, was auch mehrfach passiert ist.
AstraZeneca / Oxford (AZD1222) Studie wurde am 8. Sept. 2020 unterbrochen, weil es einen Verdacht auf eine schwerwiegende Nebenwirkung (Transverse Myelitis) bei einer Probandin in Großbritannien gab.
Johnson & Johnson (Ad26.COV2.S) wurde am 12. Okt. 2020 wegen einer „Unerklärliche Erkrankung“ eines Teilnehmers in der Phase-III-Studie (ENSEMBLE) pausiert und am 23. Okt. 2020 wieder aufgenommen da kein Hinweis auf einen ursächlichen Zusammenhang gefunden wurde.
Moderna beschreibt das Vorgehen des DSMB in Buch “The Messenger” in Kapitel 12 wie folgt.
Die Phase-3-Studien wurden von einem wenig bekannten Ausschuss namens Data Safety and Monitoring Board (DSMB) überwacht. Die meisten Arzneimittelstudien verfügen über ein DSMB, um eine unabhängige Aufsicht zu gewährleisten. Im Juni 2020 hatte das NIAID ein einziges DSMB für alle Covid-Impfstoffstudien ernannt (mit Ausnahme von Pfizer, das nicht vollwertiger Teilnehmer an „Warp Speed“ war und daher über ein eigenes, separates DSMB verfügte). Eine einzige Gruppe, die mehrere Studien überwachte, war zwar eher untypisch, würde den Prozess hier jedoch beschleunigen, da sie besser in der Lage wäre, Wirksamkeitsdaten schnell zu vergleichen, als separate, für jeden Impfstoff spezifische DSMBs.
Das DSMB für Covid-Impfstoffe bestand aus elf Mitgliedern mit unterschiedlichem Hintergrund, darunter Experten für Impfstoffkunde, Immunologie, Biostatistik, Epidemiologie, öffentliche Gesundheit und Ethik. Bei allen wurde davon ausgegangen, dass sie keine finanziellen Verbindungen zu den Unternehmen hatten, die Covid-19-Impfstoffe entwickelten. Jedes Mitglied erhielt vom NIAID ein Honorar von 200 Dollar pro Sitzung.
Über dieses DSMB war kaum mehr bekannt, außer der Tatsache, dass sein Vorsitzender Richard Whitley war, ein erfahrener Spezialist für pädiatrische Infektionskrankheiten an der University of Alabama in Birmingham. Whitley war bereits in DSMBs für mehrere klinische Studien tätig gewesen und hatte zuvor im Vorstand des Arzneimittelherstellers Gilead Sciences gesessen. […]
Alle Diskussionen und Unterlagen des DSMB waren vertraulich, was bedeutete, dass diese elf Personen die einzigen auf der Welt waren, die wussten, was in den Studien vor sich ging. Manchmal trat das DSMB kurzfristig zusammen, wenn eine rasche Überprüfung wichtiger Daten erforderlich war. Das DSMB konnte einen Blick auf die „entblindeten“ Daten werfen, beispielsweise wenn die vorab festgelegten Schwellenwerte für positive Fälle erreicht wurden – bei Moderna waren das 53, dann 106 und schließlich das Endziel von 151. Das Team traf sich per Videokonferenz, um die Daten zu prüfen und Infektionen, Reaktionen und gemeldete Nebenwirkungen zu untersuchen.2 Sie wussten, wer den Impfstoff und wer das Placebo erhalten hatte und wie es den Probanden ergangen war. Je nach den Zahlen konnten sie an jedem dieser Meilensteine eine Entscheidung über die Wirksamkeit treffen.
Moderna musste seine Studienpolulation auf Anweisung des DSMB der ethnischen Verteilung in den USA anpassen, was die Firma Zeit und Geld kostete.
Das NIAID hat Moderna praktisch zur zentralisierten Studie gezwungen. Moderna wollte das erst nicht (ähnlich wie Pfizer) musste letztendlich jedoch klein beigeben wie man in Kapitel 9 von “The Messenger” nachlesen kann.
Seit mehreren Jahren arbeitete Moderna mit einer in Wilmington, North Carolina, ansässigen Auftragsforschungsorganisation mit dem unscheinbaren Namen Pharmaceutical Product Development (PPD) zusammen, um die klinischen Studien für seine Impfstoffe und Medikamente durchzuführen. PPD war eine feste Größe für führende Pharmaunternehmen und sorgte für die Vermittlung der Ärzte, Kliniken, Patienten und Freiwilligen, die für die Durchführung einer Studie benötigt wurden. Obwohl Moderna noch nie eine so große Studie mit PPD durchgeführt hatte, ging das Unternehmen davon aus, bei diesem Vorhaben weiterhin mit dem Unternehmen zusammenzuarbeiten.
Die Bundesbehörden hatten andere Vorstellungen. Sie wollten, dass das NIAID, das Institut von Anthony Fauci, an der Durchführung der Moderna-Studie beteiligt wird. Das NIAID beabsichtigte, die für seine groß angelegten HIV-Impfstoffstudien genutzten Studienzentren nicht nur für die Impfstoffe von Moderna, sondern auch für andere, von Warp Speed unterstützte Impfstoffe wiederzuverwenden.
Bundesbeamte hatten erkannt, dass ihre Idee einer einzigen großen Studie für alle Impfstoffe nicht funktionieren würde, aber sie wollten dennoch eine gewisse Standardisierung über die Studien hinweg, um die Ergebnisse zuverlässig vergleichen zu können. Wenn sie über mehrere Studien hinweg ähnliche Designs schaffen könnten, würde dies spätere Entscheidungen darüber leiten, welche Impfstoffe gekauft werden sollten oder wer welche Impfstoffe erhalten sollte. Sollte sich beispielsweise der Impfstoff von Moderna bei älteren Erwachsenen als wirksamer erweisen als der von J&J, könnten Regierungsbeamte dessen Einsatz in dieser Bevölkerungsgruppe empfehlen.
[…] Moderna hatte erwartet, mehr Kontrolle über sein eigenes Schicksal zu haben, aber was konnte das Unternehmen schon tun? Ohne einen finanzstarken Partner aus der Pharmabranche wie Pfizer war es auf die Regierung als Partner angewiesen. Schließlich hatten Regierungsforscher bei der Entwicklung des Impfstoffs mitgeholfen, sie organisierten die erste Studie am Menschen, und die BARDA hatte eine halbe Milliarde Dollar in das Unternehmen gesteckt. Wie Tony Fauci später in Erinnerung rief: „Moderna verließ sich stark auf uns, weil sie nicht viel Erfahrung hatten.“ Es war zu diesem Zeitpunkt für Moderna schwer oder unmöglich zu sagen: „Ab hier übernehmen wir.“
Dass man die Einmischung von weiteren Staaten in seine Studienplanung daher vermeiden wollte, ist an dieser Stelle verständlich, zumal die Zulassung über das zentrale DSMB einen sauberen und koordinierten Eindruck machen sollte.
Das BAG orderte, genau wie bei Pfizer, 6 Millionen Dosen à 100 mg
Nur, Moderna schreibt selbst, dass noch nicht klar ist, welche Dosis es wird, ob 50 oder 100 µg war eigentlich noch gar nicht getestet.
Es scheint daher schon seltsam, dass die Schweiz sich direkt auf 100 µg festlegt. Später im Vertrag kommt aber, dass man das Recht zum Verdünnen hat, falls sich 50 µg aus der Dosierungsstudie ergibt und der Preis bei 200 µg der gleiche bleibt. 50 µg waren letztendlich tatsächlich die Dosis beim bei Booster.
Die Schweiz leistete eine Anzahlung von 25% des Kaufpreises. Das ist insoweit OK, weil Moderna Material kaufen musste und für die Mengen nicht das Kapital hatte. Die Kapazitäten am Stammsitz mussten zudem erst gebaut werden.
Eine Injektion kostete 30 USD, benötigt wurden für die Grundimmunisierung 2 Injektionen zu einem Gesamtpreis von 60 USD.
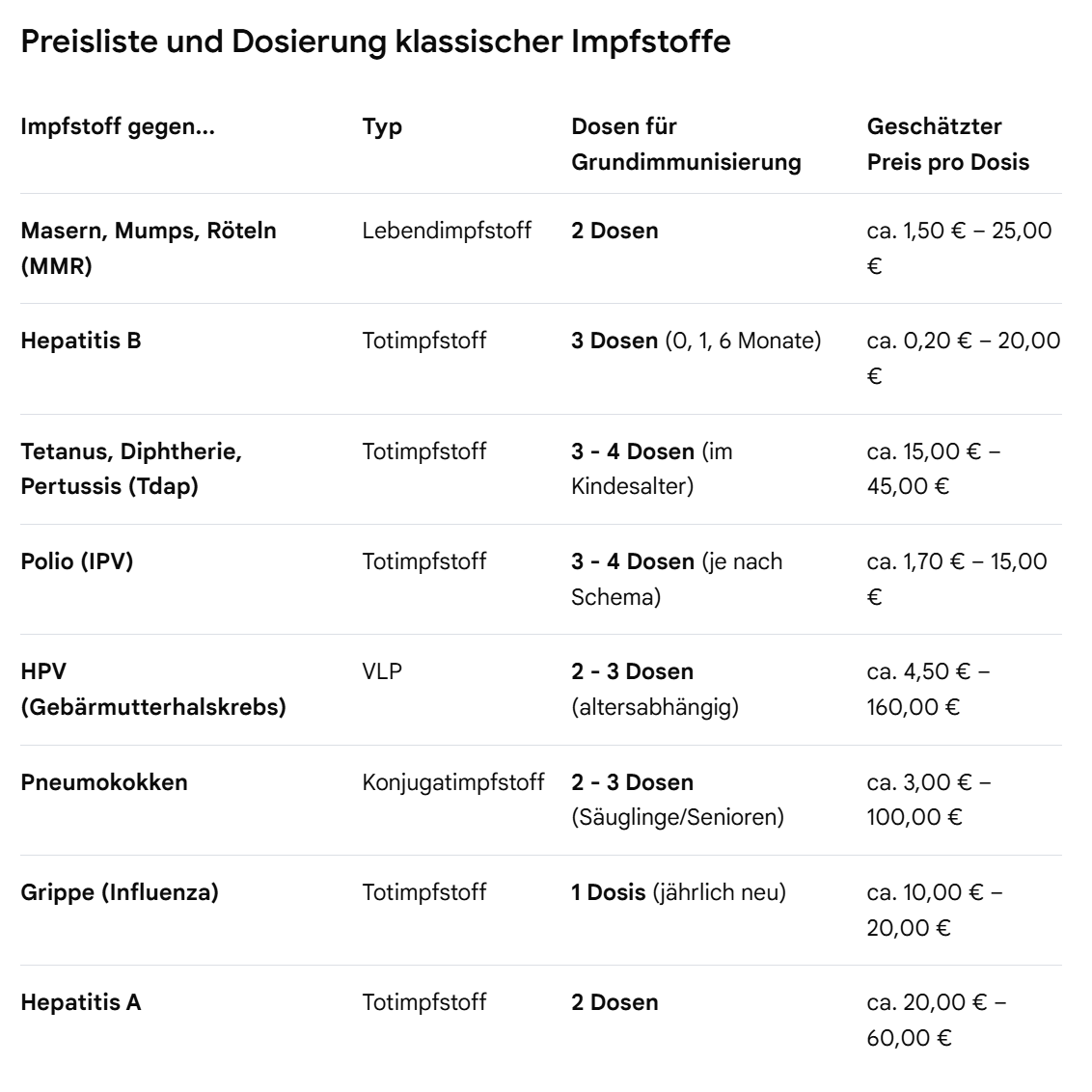
basierend auf Daten von Organisationen wie der UNICEF und dem CDC hat mir die google KI als Referenz die Preise klassischer Impfstoffe zusammengefasst. Die Preise variieren natürlich, je nach dem wie eine Krankenkasse mit dem Hersteller die Rahmenverträge vereinbart hat. Dennoch gibt diese Liste eine Orientierung, ob der Preis, dem Moderna verlangt hat, überzogen war.
Wenn man die KI den Durchschnittspreis der Immunisierungen aus der Liste errechnen lässt, ist der Preis, den Moderna für eine Grundimmunisierung verlangt hat, mit 60 USD, vollkommen im Rahmen des Üblichen.
Diese Vereinbarung ermöglicht dem Federal Office of Public Health (FOPH) nach einer Anzahlung bis Mitte Juni 2020, die Impfstoffbestellung bei Moderna bis zum 30. Juni 2020 um bis zu 75 % zu reduzieren oder eine Erhöhung anzufragen. Vor Vertragsunterzeichnung muss Moderna Produktionsstätten, Dosierung und Zusatzkosten offenlegen, wobei das FOPH nicht zum Kauf verpflichtet ist. Das klingt durchaus fair.
Moderna verspricht, sich „nach besten Kräften“ darum zu bemühen, dass mindestens 20 % des Geldes, das die Schweiz an Moderna zahlt, wieder in der Schweiz investiert werden.
Moderna hat sich daran gehalten. Lonza wurde als Lohnfertiger unter Vertrag genommen und hat dort alle Moderna Chargen für Europa produziert.
Moderna beschreibt das selbst in “The Messenger” Kapitel 14 wie folgt:
Moderna und Lonza hatten eine separate Lieferkette aufgebaut, um Impfdosen für andere Länder herzustellen. Dazu gehörten das Werk von Lonza in Visp in der Schweiz, in dem das Impfstoff-Grundprodukt hergestellt wurde, sowie ein spanisches Unternehmen namens Rovi, das für die Abfüllung der Fläschchen und die Endverpackung zuständig war. Die Lieferkette außerhalb der USA lag einige Monate hinter der US-amerikanischen zurück.
Lonza schätzte, dass für jede der drei geplanten Produktionslinien in Visp etwa siebzig Mitarbeiter benötigt würden, und das Unternehmen begann mit der Rekrutierung in der Schweiz, Italien, Deutschland und Frankreich. Doch als die Linien in Betrieb gingen, stellte das Unternehmen fest, dass siebzig Mitarbeiter pro Linie nicht ausreichten. „Wir haben während des Hochlaufs dieser Linien erkannt, dass wir mehr Personal benötigen“, sagte Albert Baehny, der Vorsitzende von Lonza, im April 2021. „Wir suchen nach weiteren Fachkräften. Was heute weltweit am meisten fehlt, sind qualifizierte Fachkräfte.“
Die Presseerklärung über die Zusammenarbeit vom 1. Mai 2020 findet man hier: Moderna and Lonza Announce Worldwide Strategic Collaboration to Manufacture Moderna’s Vaccine (mRNA-1273) Against Novel Coronavirus
Die Zusammenarbeit wurde erst in Q3 2023 runtergefahren.
Da entsprechende Pläne für die Produktion in der Schweiz seit März 2020 beschlossen waren (Moderna selbst hat kaum eigene Produktionskapazitäten), konnte man so ein Versprechen an die Schweiz natürlich problemlos machen.
Eine etwaige Erhöhung der pro Behandlungsplan erforderlichen Mikrogramm-Dosis führt nicht dazu, dass sich die Verpflichtung des FOPH gemäß dieser Absichtserklärung zur Zahlung einer Vorauszahlung von mehr als 45 Millionen US-Dollar erhöht; jedoch verpflichtet keine Bestimmung dieser Absichtserklärung das FOPH zum Abschluss des Liefervertrags.
Sollte die zu injizierende Dosis 200µg statt 50 µg oder 100 µg sein, bleibt der Preis für das BAG identisch. Das Risiko der höheren Materialkosten trägt Moderna selbst. Das ist fair und auch so im Buch “The Messenger” beschrieben.
In Übereinstimmung mit den geltenden gesetzlichen Bestimmungen kann das BAG oder die zuständige(n) Schweizer Behörde(n) gegebenenfalls beschließen, den Moderna-Impfstoff in der Schweiz tatsächlich in einer Dosis zu verabreichen, die von 100 Mikrogramm abweicht, wobei eine solche Entscheidung keine Änderung des im Rahmen des Pandemic Access Pre-Purchase vereinbarten Preises pro 100 Mikrogramm-Dosis, vorausgesetzt, dass nichts in dieser Absichtserklärung Moderna dazu verpflichtet, spezielle Abfüll- oder Veredelungsarbeiten durchzuführen, um etwaigen Abweichungen der von der BAG oder den schweizerischen Behörden angeforderten oder ausgewählten Dosierungen gerecht zu werden.
Die Schweiz entscheidet über die Dosis pro Spritze selbst, zahlt aber den vereinbarten Wirkstoff-Preis und Moderna muss dafür nichts an ihrer Produktion ändern. Die Schweiz hätte also die 100 µg Dosis auf 2×50µg strecken können und so den Preis für sich um 50% reduzieren können. Moderna hätte nichts dagegen unternommen.
Im Dezember 2020 unterzeichnete der damalige US-Präsident Donald Trump die Executive Order 13962. Die Verordnung legte fest, dass die US-Regierung sicherstellen muss, dass amerikanische Bürger vorrangigen Zugang zu Impfstoffen erhalten, die mit US-Steuergeldern entwickelt oder gekauft wurden. Erst wenn genügend Impfstoff für alle Amerikaner vorhanden ist, die sich impfen lassen wollen, dürfen die Behörden andere Länder bei der Beschaffung unterstützen oder Impfstoffe exportieren. Trump drohte zudem damit, ein altes Gesetz aus der Zeit des Koreakriegs (den Defense Production Act) einzusetzen, um US-Unternehmen rechtlich dazu zu zwingen, die Aufträge der US-Regierung vor allen anderen Aufträgen (auch aus dem Ausland) zu bedienen.
Das war mit ein Grund, war Moderna einen Teil der Produktion in nicht US Länder verlegt hat, um so auch nicht US-Kunden beliefern zu können. Da Trumps Drohungen bekannt waren, ist man so fair und versichert den Schweizern, dass sie mit den USA in der ersten Reihe sitzen.
Moderna verspricht, dass die Schweiz (das FOPH) bevorzugt beliefert wird. Das bedeutet: Wenn Impfstoff aus Fabriken außerhalb der USA fertig wird, bekommt die Schweiz zeitgleich mit anderen wichtigen Kunden ihren Anteil (pro rata – also anteilsmäßig). Die Schweiz hat sich einen Platz ganz vorne in der Schlange gesichert. Moderna darf niemanden, der später kommt, einfach „vordrängeln“ lassen.
Im Gegenzug garantiert die Schweiz Moderna, dass es in der Schweiz wie unter dem US Prep. Act behandelt wird.
Die Schweiz (das FOPH) garantiert Moderna und allen beteiligten Firmen (Zulieferern, Herstellern etc.) einen gesetzlichen Schutz vor Haftung. Das bedeutet, dass Moderna normalerweise nicht für Schäden verklagt werden kann, die durch die Herstellung oder Anwendung des Impfstoffs entstehen. Dieser Schutz orientiert sich am US-amerikanischen PREP Act. Er gilt also nur so weit, wie es dieses spezielle Gesetz zulässt. Die Schweiz darf den Impfstoff nur dann verwenden, wenn sichergestellt ist, dass dieser rechtliche Schutz für Moderna lückenlos greift.
Wer sich darüber aufregt sollte bedenken, dass das auch in Deutschland der Fall ist ABER nicht über den Vertrag mit den Herstellern, sondern über die Spahn Verordnungen:
Das wäre ein schönes juristisches Paper, wenn man den Prep. Act. mit den Spahn Verordnungen vergleichen würde.
ABER auch hier ist Moderna fair:
Ungeachtet anderslautender Bestimmungen in dieser Absichtserklärung oder im Liefervertrag (einschließlich, aber nicht beschränkt auf die beiden unmittelbar vorangehenden Absätze dieses Abschnitts) ist das BAG gemäß den Bestimmungen des Liefervertrags weder verpflichtet, den Auftragnehmern von Moderna in der Lieferkette des Moderna-Impfstoffs Immunität zu gewähren noch diese schadlos zu halten:
(i) im Falle vorsätzlichen Fehlverhaltens; oder
(ii) für Modenas Vertragspartner außerhalb der USA im Falle grober Fahrlässigkeit, sofern die Haftung für grobe Fahrlässigkeit nach dem Recht des Landes, in dem diese Vertragspartner ihren Sitz haben, nicht ausgeschlossen oder beschränkt werden kann; oder
(iii) bei Nichteinhaltung der GMP und/oder GDP infolge vorsätzlichen Fehlverhaltens oder grober Fahrlässigkeit des Vertragspartners.
In Bezug auf Auftragnehmer außerhalb der USA gewährt das BAG weder Immunität noch entschädigt es Moderna für Schäden, die durch grobe Fahrlässigkeit dieser Auftragnehmer verursacht wurden, sofern Moderna vertraglich oder anderweitig den Ausschluss oder die Beschränkung der Haftung der Auftragnehmer für grobe Fahrlässigkeit akzeptiert hat (sofern die Haftung für grobe Fahrlässigkeit nach dem Recht des Sitzlandes dieser Auftragnehmer nicht ausgeschlossen oder beschränkt werden kann).
Wenn Moderna jedoch mit Absicht Schaden angerichtet hat oder einer seiner Vertragspartner, greift auch in USA der Prep Act nicht. Man verlangt von der Schweiz nichts, was nicht auch das Heimatland Moderna bietet. Das ist durchaus fair.
Bei Problemen will man nach New Yorker Recht verhandeln
Obwohl die Schweiz und Moderna (ein US-Unternehmen) den Vertrag schließen, wird bei Streitigkeiten das Recht des US-Bundesstaates New York angewendet. Das ist im internationalen Wirtschaftsverkehr sehr verbreitet, da das New Yorker Recht als sehr wirtschaftsfreundlich, präzise und durch jahrzehntelange Urteile im Finanzsektor als „vorhersehbar“ gilt. Schweizer oder deutsches Recht spielt für die Auslegung des Vertrags also keine Rolle. Das Schiedsverfahren findet physisch in Paris statt. Das ist oft ein Kompromiss zwischen USA und Europa. Paris ist zudem einer der weltweit wichtigsten Standorte für internationale Schiedsgerichtsbarkeit.
Wenn die Schweiz Moderna verklagen wollte (oder umgekehrt), müssten sie teure spezialisierte Anwälte für New Yorker Recht engagieren und sich in Paris vor einem privaten Expertengremium hinter verschlossenen Türen streiten. Ein Urteil eines solchen Schiedsgerichts ist endgültig – eine Berufung bei einer höheren Instanz ist fast unmöglich.
Falls die Zusammenarbeit scheitert und kein finaler Vertrag zustande kommt, ist das finanzielle Risiko für die Schweiz begrenzt.
Maximal 45 Millionen Dollar: Das ist die absolute Obergrenze, die die Schweiz zahlen muss (das entspricht der bereits geleisteten Anzahlung, dem “Upfront Payment”).
Die Ausnahme: Wenn die Schweiz sich nicht an die Regeln dieser Absichtserklärung hält (Vertragsbruch), könnte es teurer werden. Aber solange alles normal läuft, sind die 45 Millionen Dollar das Maximum, das die Schweiz verlieren kann.
Mein Fazit:
Der Vorvertrag scheint mir fair, teils sogar idealistisch, was die Übernahme des Produktionsrisikos bei höherer Dosis angeht, das Moderna komplett selbst übernimmt, aber wenn sich die geringere Dosis als besser herausstellt, der Preis gleich bleibt und der Käufer das Produkt strecken darf.
Die Bedingungen sind fair. Man will in der Schweiz die gleiche rechtliche Sicherheit wie man sie aus den USA kennt. Gleichzeitig schafft man Arbeitsplätze im bestellenden Land. Dennoch überzieht man den Bogen nicht und schließt absichtlichen Schaden aus der Haftungsbefreiung aus, wie man das auch beim Prep Act kennt. Diese Absicht nachzuweisen dürfte allerdings nicht einfach sein.
Der Preis für eine Grundimmunisierung ist im Rahmen einer durchschnittlichen Immunisierung für klassische Impfungen und damit weder billig noch überzogen teuer.
Phmptadmin. (2025, August 28). Pfizer 12-15 and Moderna Court documents – Public health and medical professionals for transparency. Public Health and Medical Professionals for Transparency. https://phmpt.org/pfizer-12-15-and-moderna-court-documents/
Robbins, R., Feuerstein, A., & Branswell, H. (2023, July 25). AstraZeneca Covid-19 vaccine study put on hold due to suspected adverse reaction in participant in the U.K. STAT. https://www.statnews.com/2020/09/08/astrazeneca-covid-19-vaccine-study-put-on-hold-due-to-suspected-adverse-reaction-in-participant-in-the-u-k/
Mahase, E. (2020). Covid-19: Johnson and Johnson vaccine trial is paused because of unexplained illness in participant. BMJ, 371, m3967. https://doi.org/10.1136/bmj.m3967
Hüttemann, D. (2021, September 6). Covid-19: Moderna beantragt EU-Zulassung für Auffrischimpfung mit halber Dosis. Avoxa – Mediengruppe Deutscher Apotheker GmbH. https://www.pharmazeutische-zeitung.de/moderna-beantragt-eu-zulassung-fuer-auffrischimpfung-mit-halber-dosis-127829/
Moderna Ramps Down Mrna Drug Substance Production For Its Covid-19 Vaccine At Lonza https://investors.modernatx.com/statements-perspectives/moderna-ramps-down-mrna-drug-substance-production-for-its-covid-19-vaccine-at-lonza
Executive Order on Ensuring Access to United States Government COVID-19 Vaccines – The White House https://trumpwhitehouse.archives.gov/presidential-actions/executive-order-ensuring-access-united-states-government-covid-19-vaccines/